
Cara Menghitung pH Garam dari Asam Kuat dan Basa Lemah Materi hidrolisis garam Kimia SMA Kelas
Pengertian basa kuat ialah jenis senyawa yang melepaskan proton (deprotonasi) pada asam sangat lemah secara sederhana dalam reaksi asam basa. Adapun contoh basa kuat yang paling umum ialah Hidroksida pada logan alkali, misalnya Ca(OH)2 maupun NaOH. Selain itu adapula beberapa contoh lain yang termasuk larutan basa kuat yaitu meliputi:
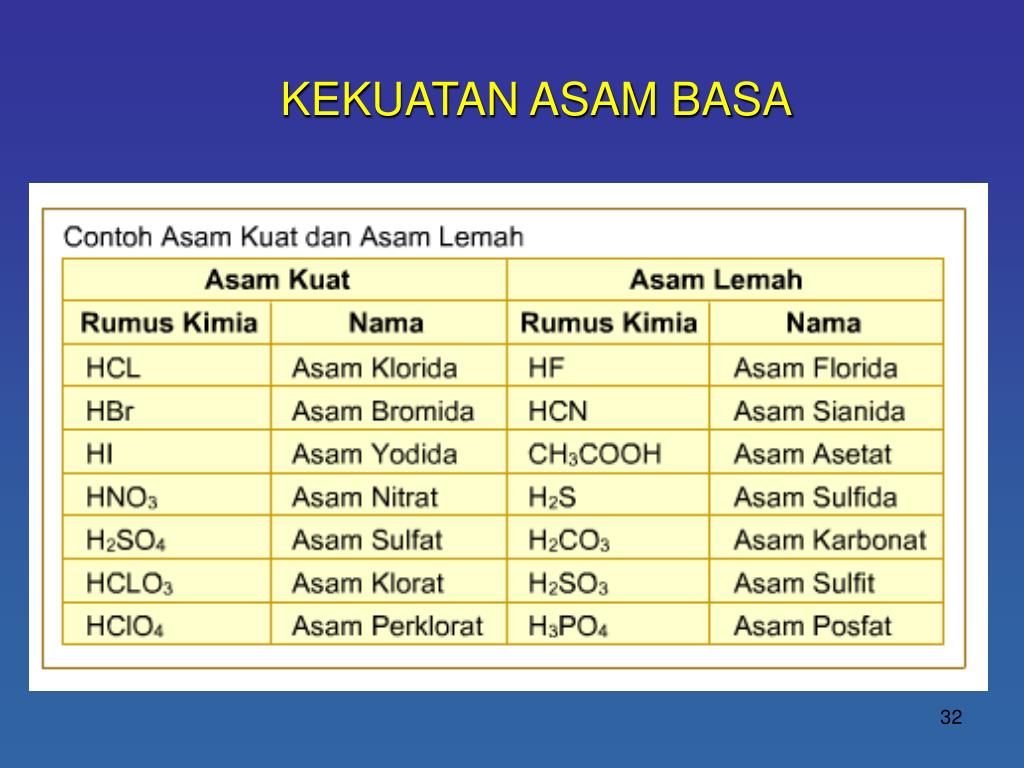
Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah Berbagai Contoh
Titrasi basa kuat oleh asam kuat, artinya: Titran (larutan standar pada buret) → asam kuat. Titrat (larutan sampel pada labu erlenmeyer) → basa kuat. Titrasi basa kuat oleh asam kuat akan menghasilkan kurva sebagai berikut. 3. Titrasi Asam Lemah oleh Basa Kuat.

Larutan di atas yang termasuk asam lemah dan basa lemah berturut turut adalah nomor YouTube
Pengertian basa lemah adalah senyawa basa yang tidak sempurna proses pelarutan atau terurainya jika ada dala air. Misalnya pada senyawa basa NaHCO3, NH4OH. - Manfaat senyawa basa dalam kehidupan: 1. Sodium hidroksida (NaOH) berguna untuk pembersih lemak dan bahan dasar sabun keras. 2. Kalium hidroksida (KOH) untuk bahan dasar sabun toilet dan.

Detail Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah Koleksi Nomer 34
Di artikel Kimia kelas 11 ini, kita akan belajar mengenai macam-macam indikator asam basa dan cara menggunakannya. Yuk, baca sampai habis! Teman-teman, di artikel sebelumnya, kamu sudah mengenal apa itu zat asam-basa dan cara membedakannya, ya. Senyawa asam akan mengandung ion H +. Contohnya buah-buahan kaya vitamin C, cuka, minuman bersoda, dsb.

PERHITUNGAN pH ASAM LEMAH DAN BASA LEMAH YouTube
Beberapa Contoh Basa Lemah Dan Kegunaannya Dalam kimia, basa dapat didefinisikan sebagai zat yang berdisosiasi dalam larutan berair untuk membentuk ion Hidroksida (OH−). Basa lemah adalah basa yang tidak sepenuhnya terdisosiasi menjadi ion penyusunnya ketika dilarutkan dalam larutan. Beberapa bagian dari basa lemah terdisosiasi menjadi ion hidroksida, sementara beberapa tetap tidak.
Daftar Asam Basa Kuat Dan Lemah
Basa kuat adalah adam love Valen sederhana yang dapat mendeprotonasi asam sangat lemah di dalam reaksi asam-basa. Contoh paling umum dari basa kuat adalah hidroksida dari logam alkali dan logam alkali tanah seperti NaOH dan Ca(OH) 2. Berikut ini adalah daftar basa kuat: Kalium hidroksida (KOH) Barium hidroksida (Ba(OH) 2) Cesium hidroksida (CsOH)

20+ Contoh Soal Hidrolisis Asam Lemah Dan Basa Kuat Contoh Soal Terbaru
Basa lemah adalah senyawa basa yang sulit melepaskan ion OH - dalam air dan mengalami disosiasi sebagian dalam larutannya. Contoh basa lemah yaitu NaHCO 3 dan NH 4 OH. Itu tadi pembahasan kita tentang asam basa, mulai dari sifat atau cirinya, cara membedekan, hingga klasifikasinya.

Tabel Asam Lemah dan Basa Lemah
Jawabannya adalah basa lemah. Basa lemah adalah larutan yang menghasilkan sedikit ion dan sedikit terurai saat dilarutkan dalam air. Derajat ionisasi (0<α<1) Contoh basa lemah selain NH4OH adalah NaHCO3, Al(OH)3, AgOH.. Larutan KOH merupakan basa kuat, sedangkan Al(OH)3 dan NH4OH termasuk basa lemah. ———-Demikian pembahasan mengenai.

Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah Berbagai Contoh
2. Asam Lemah dan Basa Lemah. Asam lemah merupakan senyawa yang sedikit terurai pada waktu dilarutkan didalam air. Contohnya: H 3 PO 4, H 2 SO 3, HNO 2, CH 3 COOH. Basa lemah merupakan senyawa yang cuma sedikit terurai pada waktu dilarutkan kedalam air. Contohnya: NaHCO 3, NH 4 OH. Lalu berdasarkan bentuk ionnya, asam basa diklasifikasikan menjadi:

(DOC) Berikut ini Daftar Nama Asam Kuat Asam Lemah Basa Kuat Basa Lemah Nurhadi Prayogi
Contoh basa lemah adalah amonia. Ia tidak mengandung ion hidroksida, tetapi bereaksi dengan air untuk menghasilkan ion amonium dan ion hidroksida. [4] Posisi keseimbangan bervariasi dari satu basa ke basa lain ketika basa lemah bereaksi dengan air. Semakin jauh ke kiri itu, semakin lemah basanya.

Soal Pembahasan Larutan Penyangga Buffer Reaksi Asam Basa Lemah Dan Hot Sex Picture
Ilustrasi Asam-Basa Kuat dan Asam-Basa Lemah ( Freepik.com) Sonora.ID - Dalam pelajaran Kimia, kita mengenal larutan asam, basa, dan garam, sesuai dengan pH yang ditunjukkan oleh larutan tersebut. Asam sendiri adalah zat yang menghasilkan ion Hidrogen (H+) dalam larutan, sedangkan basa menghasilkan ion Hidroksida (OH-) dalam larutan.

Teori Asam Basa
Termasuk larutan basa kuat adalah : NaOH, Mg (OH)2, KOH, Ca (OH)2, Sr (OH)2. Sedangkan yang dimaksud larutan basa lemah adalah yang memiliki ciri-ciri : Larutan tersebut sulit terion. Memiliki ikatan antar ion yang sulit lepas. Ikatan antar ion sulit lepas karena jarak antar inti atom pada molekul yang sangat dekat.

Mencari nilai pH dari larutan Amonium Hidroksida /NH4OH yang termasuk basa lemah YouTube
Valensi basa adalah jumlah ion OH − yang dihasilkan per unit rumus basa. basa lemah (contoh: NH 3, CH 3 NH 2, C 6 H 5 NH 2) Dalam air, hanya sebagian basa lemah terurai menjadi ion-ionnya, sehingga derajat ionisasinya 0 < α < 1.. NH 3 termasuk basa lemah. NH 3 (aq) + H 2 O(l).
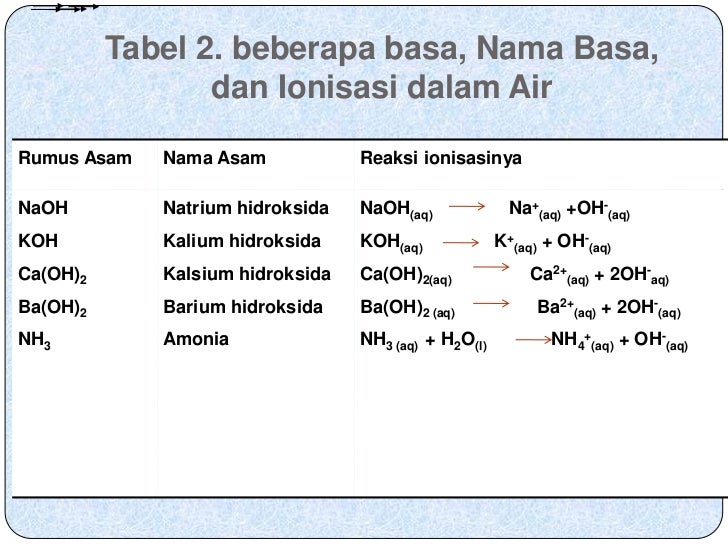
Contoh Asam Basa Kuat Dan Lemah Serta Reaksi Ionisasinya Berbagai Contoh
Sementara jika salah satu asam dan basa ada yang bersifat kuat dan lemah kemudian direaksikan, maka garam dan air yang dihasilkan akan mengikuti zat pereaksi yang kuat.. CaCO 3 dan MgCO 3 diketahui termasuk dalam kelompok basa. CaCO3 yang ditambahkan ke dalam tanah akan bereaksi dengan air membentuk Ca(OH)2,.

Mg Oh 2 Basa Kuat Atau Lemah cara bertanya yang baik kepada guru
03 Maret 2023 Lili Y. Bagikan. 28 Contoh Asam Basa Kuat dan Asam Basa Lemah Beserta Reaksi Ionisasinya - Ketika kamu menambahkan soda kue ke cuka, maka akan menyebabkan gelembung dan busa. Ini merupakan reaksi antara asam dan basa. Asam dan basa dicirikan oleh pertukaran ion hidrogen. Asam adalah molekul yang menyumbangkan satu ion hidrogen.

27+ Contoh Soal Hidrolisis Asam Lemah Basa Lemah Contoh Soal Terbaru
Berikut adalah pengertian dan contoh dari basa kuat dan basa lemah! Basa kuat. Dilansir dari Chemistry LibreTexts, basa kuat adalah basa yang terionisasi secara sempurna ke dalam air. Ketika larut dalam air, setiap molekul basa kuat akan melepaskan ion hidroksida (OH-). Basa kuat memiliki pH yang tinggi, biasanya lebih besar dari 11.