
Koleksi Asam Yang Kuat Dan Lemah Dengan Konsep Garis Besar Diagram Pendidikan Ilustrasi Stok
Jadi, titrasi asam basa adalah suatu prosedur yang dilakukan saat kita ingin menentukan kemolaran atau konsentrasi suatu as am atau basa. Titran ini merupakan larutan standar yang telah diketahui secara pasti konsentrasinya, misalnya asam kuat atau basa kuat. Nah, pada titrasi asam basa, posisi titran terletak pada buret. b. Buret

PPT TITRASI ASAM BASA PowerPoint Presentation, free download ID4806100
Asam adalah molekul atau ion yang dapat memberikan proton (ion hidrogen H +), atau, alternatifnya, dapat membentuk ikatan kovalen dengan pasangan elektron ().. Kategori pertama asam adalah donor proton atau asam Brønsted.Pada kasus khusus dalam larutan berair, donor proton membentuk ion hidronium H 3 O + dan dikenal sebagai asam Arrhenius. Brønsted dan Lowry memperumum teori Arrhenius untuk.
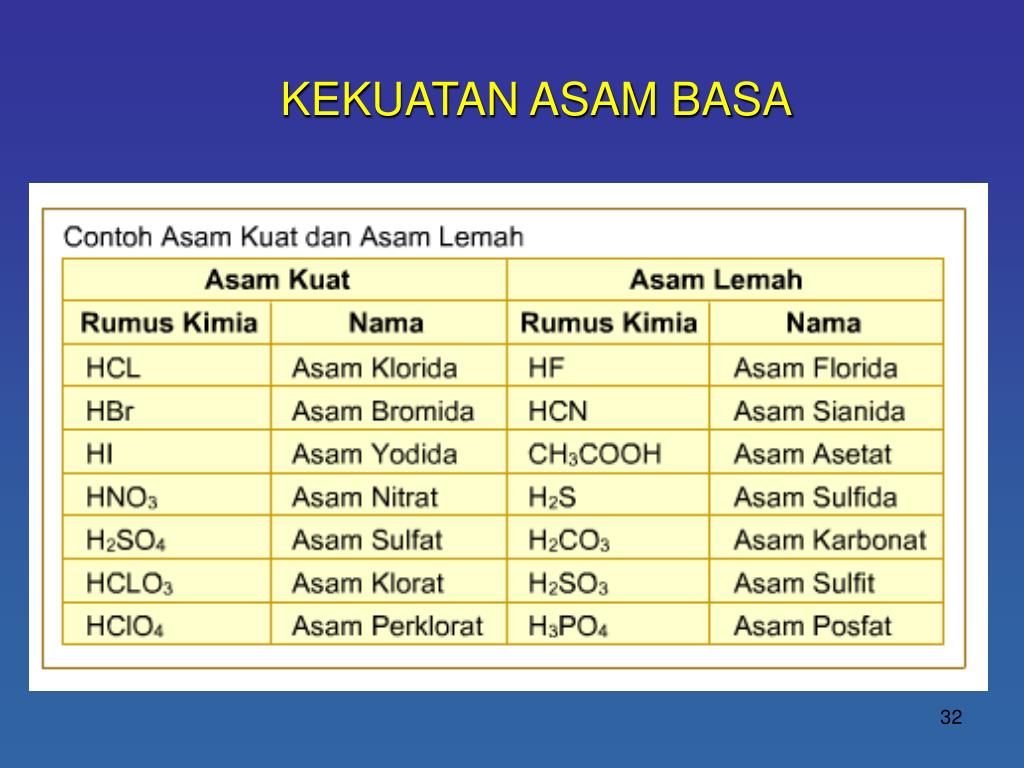
Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah Berbagai Contoh
Berikut adalah pengertian dan contohnya: Asam kuat. Asam kuat adalah larutan dengan pH rendah yang terionisasi secara sempurna dalam air. Asam kuat memiliki pH di bawah tiga, hingga kadar keasamannya sangat tinggi. Dilansir daru Chemguide, asam kuat melepaskan ion hidrogen ketika dilarutkan dalam air hingga terionisasi secara sempurna. Berikut.

Detail Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah Koleksi Nomer 25
Pengertian asam Mengutip laman emodul Kemdikbud, seorang ahli kimia Swedia bernama Svante August Arrhenius menyatakan bahwa asam merupakan senyawa elektrolit yang apabila larut dalam H2O (air) maka akan terionisasi menjadi ion hidrogen (H+) dan ion sisa asam yang bermuatan negatif. Reaksi kimianya adalah berikut: 1) HCl + air → H+ + Cl-2) CH3COOH + air → CH3COOH + H+

Daftar Asam Basa Kuat Dan Lemah
Sedangkan yang dimaksud dengan asam lemah adalah asam yang tidk dapat terinisasi secara sempurna di dalam air. Larutan asam ini biasanya memiliki tingkat pH keasaman di atas tiga. Semakin besar pH keasaman yang dimiliki akan membuat tingkat keasamannya makin rendah. Untuk asam kuat pH keasamannya berada di bawah tiga.

Menghitung PH Larutan Garam Asam Kuat Basa Lemah Tyaa
Asam kuat merupakan asam yang jika dilarutkan dalam air mudah melepaskan ion H+, larutan tersebut akan mengalami disosiasi total dalam larutan. Contoh asam kuat yaitu HCl, HNO3, H 2 SO4, dan HClO4. Sementara basa kuat adalah senyawa basa yang jika dilarutkan dalam air mudah melepaskan ion OH-, larutan basa ini juga akan mengalami disosiasi total.

Titrasi AsamBasa
Zat asam dan basa dijelaskan dalam teori oleh beberapa pakar kimia, di antaranya teori Arrhenius, Bronsted-Lowry, dan Lewis. Asam-basa adalah sifat kimiawi yang dimiliki oleh bahan makanan, minuman, obat-obatan, dan zat lainnya. Disebutkan dalam laman Sumber Belajar Kemdikbud, bahwa secara umum asam mempunyai rasa masam dan basa mempunyai rasa.

Soal Diantara kelompok asam berikut ini yang tergolong asam kuat adalah....
Contoh asam kuat yaitu HCl, HNO 3, H 2 SO 4, dan HCIO 4. Sedangkan basa kuat adalah senyawa basa yang mudah melepaskan ion OH - dalam air dan mengalami disosiasi total dalam larutannya. Contoh basa kuat yaitu NaOH, KOH, dan Ba(OH) 2. 2. Asam Lemah dan Basa Lemah. Asam lemah adalah senyawa asam yang sulit melepaskan ion H + dalam air dan.
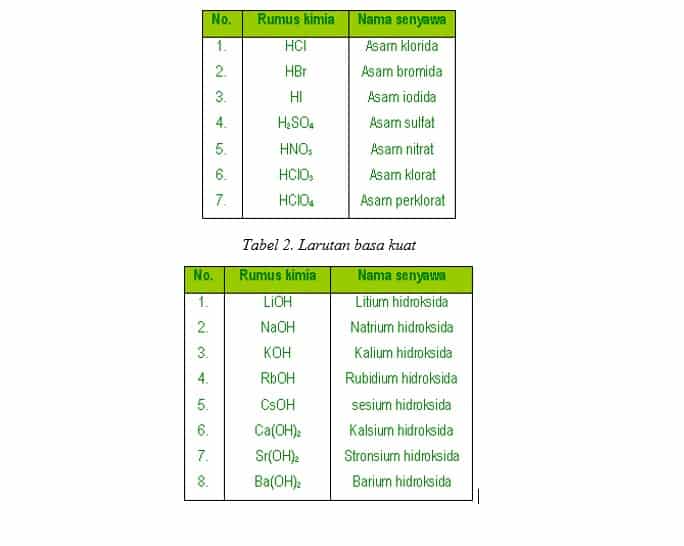
Contoh Garam Dari Asam Kuat Dan Basa Kuat Berbagai Contoh
Rasanya asam dan pahit. Salah satu sifat asam dan basa yang paling mudah dikenali adalah rasanya. Walaupun kita tidak boleh asal mencicipi larutan untuk mengetahui rasanya. Akan tetapi, paling tidak, kita sudah tahu bahwa larutan asam rasanya masam. Contohnya seperti jeruk, tomat, lemon, atau cuka. Sementara larutan basa rasanya pahit dan licin.

Detail Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah Koleksi Nomer 21
Contoh Asam Kuat, Pengertian, Ciri-ciri hingga Fungsinya. Apa itu larutan asam dan apa saja contoh asam kuat? Menurut Arrhenius, asam adalah senyawa yang jika dilarutkan dalam air akan melepaskan ion hidrogen (H+) atau ion hidronium (H3O+). Reaksi pelepasan ion H+ dan ion H3O+, yaitu HCl = H+ + Cl- atau HCl + H2O = H3O+ + Cl-, seperti dikutip.

Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah Berbagai Contoh
Walaupun reaksi asam basa disebut reaksi penetralan, tetapi hasil reaksi itu (disini yang dimaksud adalah garam) tidak selalu bersifat netral, melainkan tergantung pada kekuatan asam basa yang membentuknya. Jika larutan asam basa dicampur, maka ada tiga kemungkinan sifat garam yang terbentuk, yaitu: Asam kuat + basa kuat → garam (netral)
Dunia Dalam Berita Tentang Hno3 Asam Kuat Atau Lemah Trending
Asam kuatadalah asam yang mengalami ionisasi sempurna. Asam lemahadalah asam yang terionisasi sebagian. Basa kuatadalah basayang mengalami ionisasi sempurna. Basa lemah adalah basayang terionisasi sebagian. Jadi jawaban yang benar adalah sesuai uraian di atas.

Mengenal Asam Basa Sifat, Cara Membedakan, dan Klasifikasinya Kimia Kelas 11
Contoh asam kuat dan asam lemah - Asam (yang sering diwakili dengan rumus umum HA) secara umum merupakan senyawa kimia yang bila dilarutkan dalam air akan menghasilkan larutan dengan pH lebih kecil dari 7.Dalam definisi modern, asam adalah suatu zat yang dapat memberi proton (ion H+) kepada zat lain (yang disebut basa), atau dapat menerima pasangan elektron bebas dari suatu basa.

Detail Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah Koleksi Nomer 34
Dalam teori ini, asam kuat adalah senyawa asam yang terionisasi secara sempurna dan kemudian menghasilkan sebuah ion H+ dalam larutannya. Sedangkan untuk asam lemah, adalah senyawa asam yang tidak mengalami ionisasi secara sempurna dalam larutannya.. Sedangkan yang dimaksud dengan basa konjugasi merupakan senyawa yang ada pada bagian kanan.
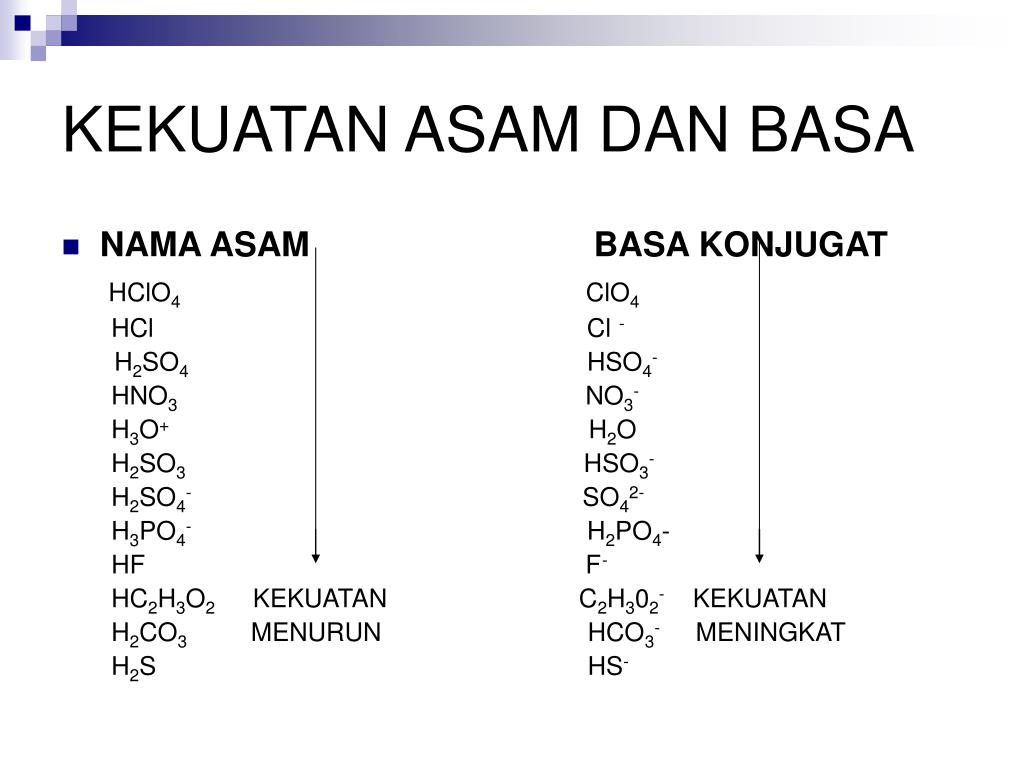
PPT ASAM DAN BASA PowerPoint Presentation, free download ID1244635
Yang Perlu Anda Ketahui Tentang Reaksi Netralisasi. Mencampur asam dan basa untuk menghasilkan larutan netral adalah netralisasi. Steve McAlister, Getty Images. Reaksi netralisasi adalah reaksi kimia antara asam dan basa yang menghasilkan larutan yang lebih netral (mendekati pH 7). PH akhir tergantung pada kekuatan asam dan basa dalam reaksi.

Cara Menghitung Ph Larutan Asam Kuat Dan Asam Lemah Panduan Kimia Riset Sexiz Pix
Asam Svante August Arrhenius, seorang ahli kimia asal Swedia yang hidup tahun 1859-1927 menjabarkan pengertian asam sebagai: semua zat atau senyawa elektrolit yang jika dilarutkan dalam air akan terurai menghasilkan ion H+ (hidrogen) dan ion sisa asam yang bermuatan negatif, demikian menurut Modul Guru Pembelajar IPA Terapan SMK. Contoh dari asam berdasarkan teori tersebut adalah hidrogen.