
Perhatikan energi ionisasi unsurunsur dalam satu periode...
Nah, kalau dilihat dari sifat nomor 1 tadi, berarti seharusnya semakin ke kanan, berarti semakin meningkat, dong, energi ionisasi setiap unsur. Tapi, uniknya di periode ketiga ini ada dua pasang unsur yang urutan energi ionisasinya terbalik, yaitu antara magnesium (Mg) dengan aluminium (Al) serta fosfor (P) dengan sulfur (S).

Sifat Unsur Sistem Periodik 3 Energi Ionisasi YouTube
Tingkatan-tingkatan EI merujuk pada urutan elektron yang dilepas. Baca rincian di bawah untuk mengetahui selengkapnya. 1. EI Pertama.. Energi ionisasi ketiga, keempat, dan seterusnya mengacu pada energi yang diperlukan untuk melepaskan elektron ketiga, keempat, dan seterusnya dari sebuah atom yang telah kehilangan elektron sebelumnya..

Energi Ionisasi dan Afinitas Elektron YouTube
Harga voltase pada saat mulai terjadinya arus listrik inilah yang didefinisikan sebagai energi ionisasi; oleh karena itu, energi ionisasi biasanya dinyatakan dalam satuan SI, elektron volt, eV (1 eV = 1,60 × 10 −19 J = 96,485 kJ.mol −1, dan sering pula disebut sebagai potensial ionisasi. Dengan batasan tersebut berarti bahwa energi.

Perhatikan grafik hubungan antara energi ionisasi dengan
Energi Ionisasi Energi ionisasi adalah energi yang diperlukan untuk melepaskan satu elektron terluar dari suatu atom atau ion dalam fase gas. Contoh: Kalsium mempunyai energi ionisasi pertama, IE1 adalah 590 kJ / mol, sebagai berikut: Ca (g) + 590 kJ → Ca+(g) + e- Sementara itu, energi ionisasi kedua (IE2) adalah jumlah energi yang.

Soal Sifat Keperiodikan Energi Ionisasi YouTube
Pengertian energi ionisasi adalah energi yang dibutuhkan oleh atom atau ion dalam keadaan gas untuk melepaskan satu buah elektron pada kulit terluarnya. Grafik energi ionisasi untuk unsur-unsur dapat dilihat sebagai berikut:. Perkirakanlah urutan jari-jari atom, EI, dan elektronegativitas unsur-unsur berikut dari yang terendah! a. $_{11}Na.

Pengertian Energi Ionisasi Unsur Kimia, Nomor Atom, Satu Golongan, Periode
Cara Mudah Menjawab Soal Energi Ionisasi Pemahaman mengenai energi ionisasi dan penjelasan mengenai cara mudah menentukan urutan unsur dan kestabilan unsur b.

Energi ionisasi kelima unsur yang terletak pada periode k...
1. Terdapat unsur-unsur AA, AB, AC, AD, AE yang berada pada satu golongan unsur. Diketahui besar energi potensial ionisasi sebesar 56 kJ/mol, 183 kJ/mol, 118 kJ/mol, 254 kJ/mol, dan 63 kJ/mol secara berturut-turut. Tentukan urutan yang sesuai dengan kenaikan nomor atom dari unsur-unsur tersebut!
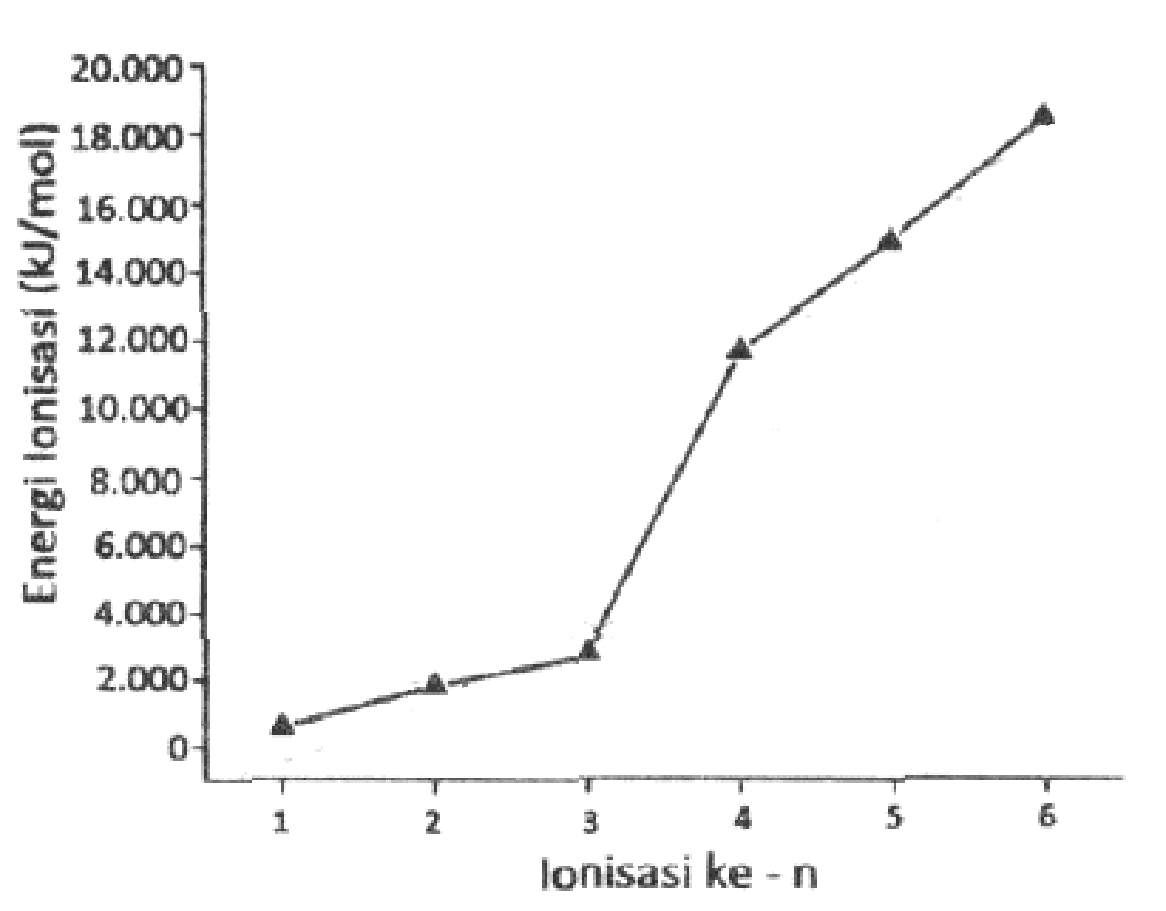
Grafik Energi Ionisasi bintangutama69.github.io
Dilansir dari ARPANSA, energi dari satu ionisasi lebih dari cukup untuk memutus ikatan kimia antara dua atom karbon. Pemutusan ikatan kimia akibat ionisasi membuat materi pecah dan menyebabkan kerusakan pada sel atau jaringan hidup. Berikut adalah urutan daya ionisasi sinar-sinar radioaktif dimulai dari yang paling lemah!
Energi Ionisasi Homecare24
Masing-masing unsur golongan VI A juga memiliki sifat yang berbeda, misalnya jari-jari atom dan energi ionisasinya . Struktur Atom Oksigen dan Sulfur (Arsip Zenius) Elo harus ingat bahwa semakin banyak elektron yang dimiliki oleh suatu unsur, semakin banyak pula kulit atomnya. Nah, kulit atom yang banyak ini bisa membuat jari-jari atomnya juga.

Pembahasan Soal Energi Ionisasi Periode Ketiga YouTube
Dilansir dari Thought Co, atom dengan energi ionisasi yang rendah memiliki keelektronegatifan yang rendah juga karena inti atomnya tidak memberikan gaya tarik menarik yang kuat terhadap elektron.. Urutan Daya Ionisasi Sinar-sinar Radioaktif Pengertian Tabel Periodik, Unsur, Klasifikasi, dan Cara Membacanya Tabel Periodik
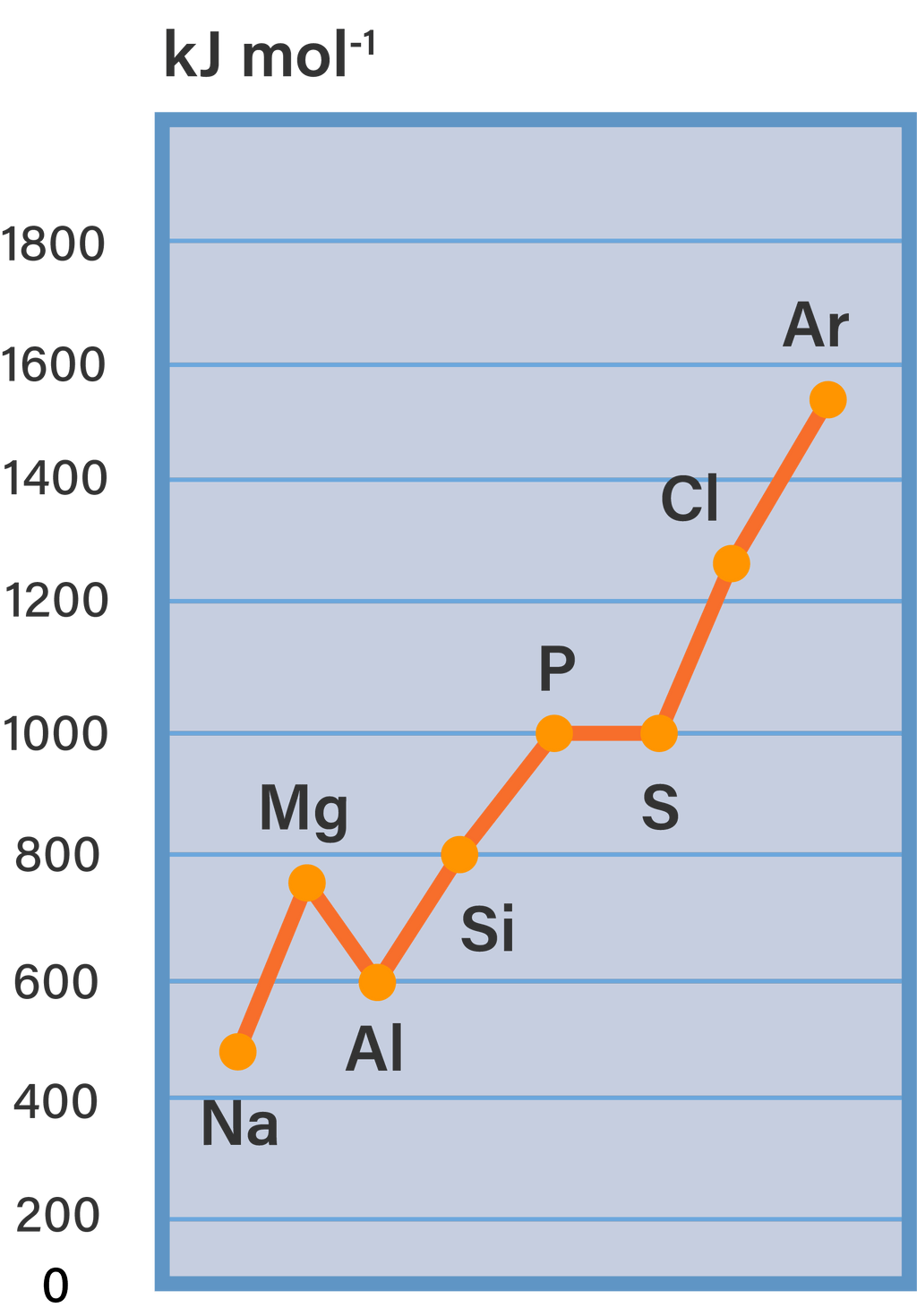
Unsurunsur pada periode ke tiga terdiridari Na, M...
Grafik Energi Ionisasi. Grafik EI pertama atom unsur-unsur fungsi dari nomor atom. Secara umum, keteraturan energi ionisasi (EI) pada suatu sistem periodik adalah sebagai berikut: Energi ionisasi (EI) yang pertama akan selalu lebih kecil dibandingkan EI yang kedua. Hal itu menunjukkan akan semakin sulit melepaskan elektron yang berikutnya.
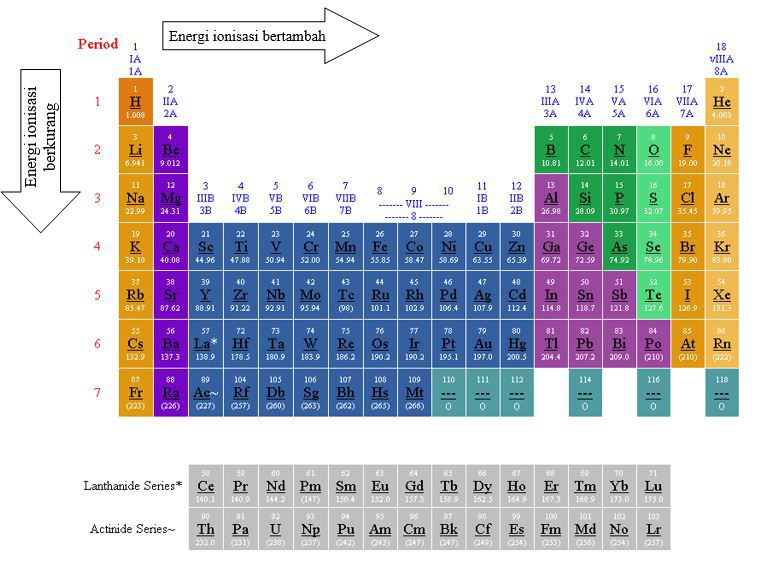
Energi Ionisasi Pengertian Energi Ionisasi &
Apa yang perlu Anda ketahui tentang energi ionisasi. Energi ionisasi atau potensial ionisasi, adalah energi yang diperlukan untuk melepaskan elektron Semakin dekat dan semakin erat ikatan elektron dengan nukleus , semakin sulit untuk melepaskannya, dan semakin tinggi energi ionisasinya. Energi ionisasi diukur dalam elektronvolt (eV).

Perhatikan tabel energi ionisasi pertama unsurunsur beri...
Pembahasan. Energi ionisiasi dari satu golongan semakin ke bawah maka semakin kecil. Hal ini karena semakin ke bawah jari-jari atom semakin besar sehingga daya tarik inti terhadap elektron terluar lebih lemah dan memudahkan elektron untuk lepas. Urutan energi ionisasi unsur halogen dari yang terkecil adalah At < I < Br < Cl < F.

Hubungan antara energi ionisasi unsurunsur periode ketig...
Energi ionisasi pertama hidrogen dapat diwakili oleh persamaan berikut: H ( g ) → H + ( g ) + e -. H ° = -1312,0 kJ/mol. Jika Anda melihat grafik energi ionisasi pertama, dua pengecualian untuk tren sudah terlihat. Energi ionisasi pertama boron lebih kecil dari berilium dan energi ionisasi pertama oksigen lebih kecil dari nitrogen.

Unsur yang memiliki energi ionisasi seperti dalam tabel b...
Energi ionisasi didefinisikan sebagai energi yang dibutuhkan untuk melepas 1 mol elektron dalam wujud gas. Pada sistem periodik unsur dalam satu golongan dari atas ke bawah energi ionisasi semakin kecil sedangkan dalam satu periode dari kiri ke kanan energi ionisasi semakin besar. Melalui konfigurasi elektron masing-masing unsur pada soal maka.

SifatSifat Keperiodikan Unsur Energi Ionisasi Secara Golongan & Periode YouTube
Unsur-unsur periode ketiga meliputi natrium (Na), magnesium (mg), alumunium (Al), silikon (Si), fosforus atau fosfor (P), belerang (S), klorin (Cl) dan argon (Ar). Perbedaan elektron valensi menyebabkan perbedaan sifat kimia. Karena sifat kimia yang berbeda dalam satu periode dari kiri ke kanan mempunyai kenaikan yang teratur sehingga sifat.