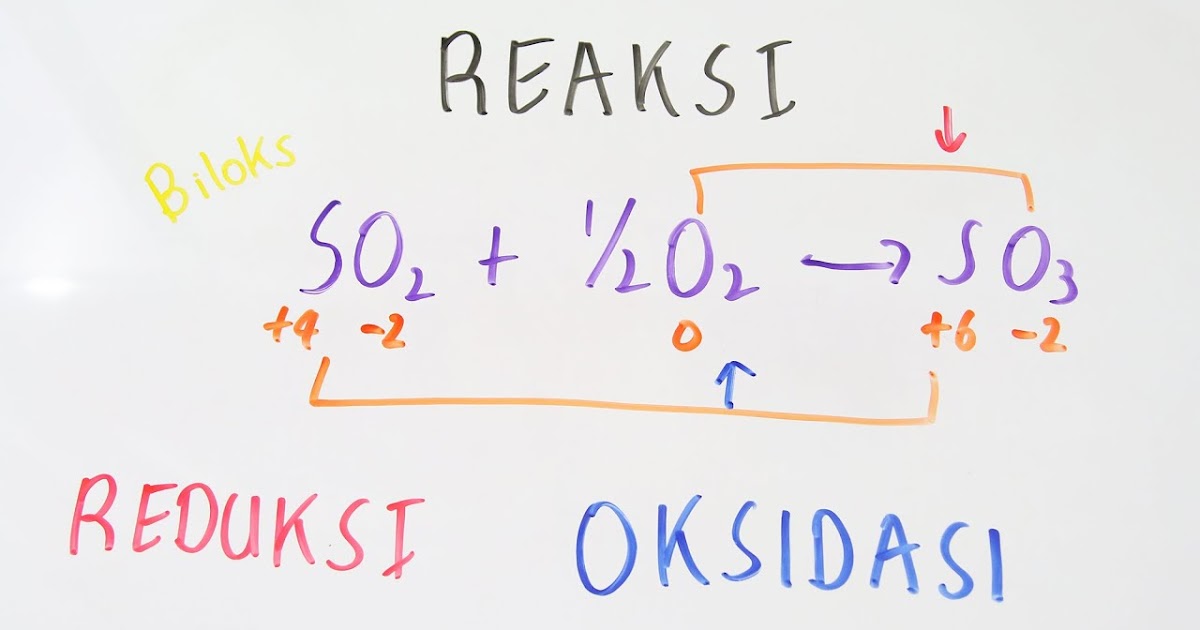
Cara Menentukan Bilangan Oksidasi Dari Unsur Yang Terdapat Di Dalam Senyawa Ion Pejuangtoga
Pada ion OH-, bilangan oksidasi O ditambah dengan bilangan oksidasi H = -1. Pada ion SO42-, bilangan oksidasi S ditambah dengan 4 kali bilangan oksidasi O = -2. Pada ion NH+4, bilangan oksidasi N ditambah dengan 4 kali bilangan oksidasi H = +1. 5. Bilangan oksidasi unsur-unsur golongan alkali (IA) dalam berbagai senyawa yang dibentuknya adalah +1

Cara Menentukan Bilangan Oksidasi Suatu Unsur Dalam Senyawa 5NChemistry
Bilangan oksidasi unsur Cl pada NaCl, KCl, MgCl 2, dan FeCl 3 adalah -1. 5. Bilangan oksidasi unsur H pada senyawanya adalah +1.' Kecuali dalam hidrida (senyawa hydrogen dengan logam), bilangan oksidasinya -1′ Alasan: dalam senyawa hidrida, hidrogen ada dalam bentuk ion hidrida, H -. Biloks dari ion seperti hidrida adalah sama dengan.

Bilangan oksidasi Mn tertinggi terdapat pada senyawa....
Lihat pula: bilangan oksidasi dalam {{kotak info unsur}} Bilangan oksidasi juga dipelihara dalam artikel suatu unsur (tentu saja), dan secara sistematis dalam tabel {{Kotak info unsur/symbol-to-oxidation-state}} Pemeliharaan & peningkatan. Untuk pemeliharaan: kedua daftar dibandingkan dalam /datacheck ini, untuk mendapatkan perbaikan bersama.

Bilangan Oksidasi Tertinggi Unsur O Terdapat Dalam Senyawa Blog Yuri
Jumlah bilangan oksidasi unsur O pada molekul unsur O 2 adalah 0. Jumlah bilangan oksidasi unsur O pada senyawa biner dengan F adalah +2. Jumlah bilangan oksidasi unsur O pada senyawa peroksidasi adalah -1. Jumlah bilangan oksidasi unsur O pada senyawa superoksida adalah -½.

Cara Menentukan Bilangan Oksidasi Unsur Dalam Senyawa Kelas 10 YouTube
Aturan Penentuan Bilangan Oksidasi. Setelah memahami pengertian, Sobat Zenius juga harus tahu aturan biloks. Aturan yang menentukan bilangan oksidasi yang benar adalah: Unsur Bebas → Biloks = 0. Contoh: Na, K, Cl 2, M 2, dan O 2. Logam yang Berikatan dengan Unsur Lain → Biloks = Positif. Contoh: Gol I: Na, K, Rb → biloks = +1
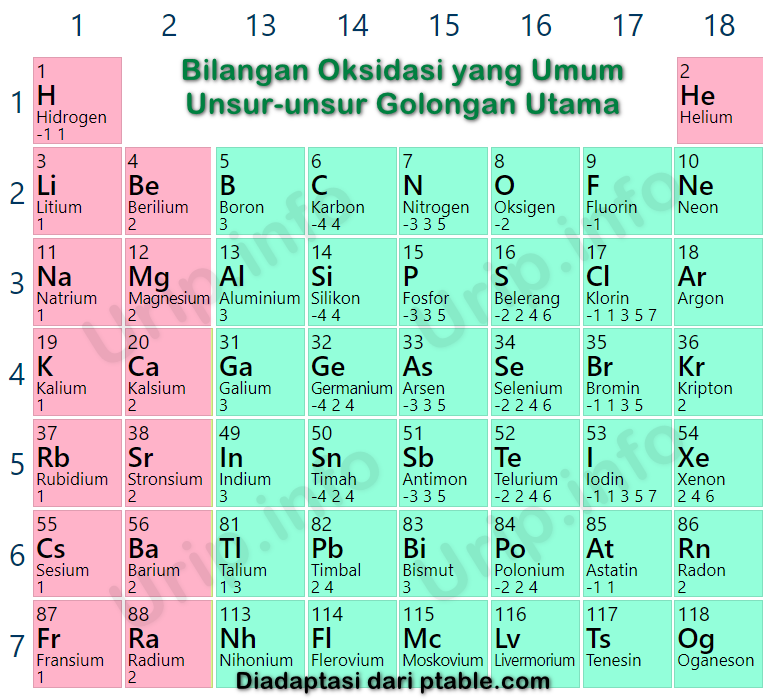
Mengapa Cl Mempunyai Bermacammacam Bilangan Oksidasi? Urip dot Info

Cara Menentukan Bilangan Oksidasi Matob
Mn 1,75 Fe 1,80 Co 1,84 Ni 1,88 Cu 1,85 Zn 1,588 Ga 1,756 Ge 1,994 As 2,211 Se 2,424 Br 2,685 Kr. Unsur dengan beberapa keadaan oksidasi Sebagian besar unsur memiliki lebih dari satu kemungkinan bilangan oksidasi.. Kolom bilangan oksidasi 0 hanya menunjukkan unsur-unsur yang diketahui berada pada bilangan oksidasi 0 dalam senyawa.

Bilangan Oksidasi Tertinggi Dari Atom Ci Terdapat Pada Senyawa Lengkap
IA = +1, gol IIA = +2 Biloks unsur H dalam senyawa = +1, kecuali senyawa hidrida = -1 Biloks unsur O dalam senyawa = -2, kecuali peroksida = -1, dan superoksida = -½ Berdasarkan aturan tersebut, biloks N dalam masing-masing senyawa dapat ditentukan sebagai berikut. Senyawa dengan biloks N terendah adalah , yaitu -3.

Bilangan Oksidasi Tertinggi Unsur O Terdapat Dalam Senyawa Blog Yuri
Pembahasan. Mn merupakan logam golongan transisi. Logam golongan transisi dapat memiliki lebih dari 1 bilangan oksidasi. Bilangan oksidasi Mn tertinggi dapat diketahui dengan menghitung bilangan oksidasi Mn pada tiap pilihan jawaban, yaitu: a. Biloks Mn dalam. b. Biloks Mn dalam. c. Biloks Mn dalam.

Bilangan Oksidasi Mn Tertinggi Terdapat Dalam Senyawa Judul Soal
Ikut Bimbel online CoLearn mulai 95.000/bulan.IG CoLearn: @colearn.id https://bit.ly/Instagram-CoLearnSekarang, yuk latihan soal ini!Bilangan oksidasi Mn ter.

Bilangan Oksidasi Mn Tertinggi Terdapat Dalam Senyawa Judul Soal
Solusi ngerjain latihan soal Kimia kelas 10 materi Bilangan Oksidasi Unsur dalam Senyawa atau Ion. Bilangan oksidasi Mn yang tertinggi terdapat dalam senyawa..a) K2 MnO4 b) MnO2 c) KMnO4 d) Mn2 O3 e) Mn(OH)2. MN + 2 X min 2 sama dengan nol maka biloks MN = + 4 selanjutnya kita ke soal yang ada pada soal D dia mirip mirip dengan soal B.

tuliskan bilangan oksidasi dari unsur besi dan mangan dari senyawa besi2 sulfat dan mangan 3
Bilangan oksidasi unsur H pada H 2 O, HCl, H 2 S, dan NH 3 ialah +1. Bilangan oksidasi unsur H pada NaH, CaH 2, dan AlH 3 ialah -1. 6. Bilangan oksidasi unsur O pada senyawanya ialah -2, kecuali :', yaitu: 1. Pada senyawa biner dengan F, bilangan oksidasinya ialah +2. 2. Pada senyawa peroksida, seperti H 2 O 2, Na 2 O 2 dan BaO 2 , bilangan.

Bilangan Oksidasi Mn Tertinggi Terdapat Pada sisi tegak pada bangun segitiga
Nah sekarang kita cari pada option a hingga e yang memiliki nilai bilangan oksidasi MN nya adalah + 6 yaitu sama dengan bilangan oksidasi CR yang ada pada K2 cr2 o7 senyawa yang pertama adalah kmno4 berlaku lagi untuk poin yang ketiga di mana jumlah biloks unsur yang membentuk senyawa adalah sama dengan nol maka di sini senyawa kmno4.

Contoh Reaksi Reduksi Dan Oksidasi Berdasarkan Perubahan Bilangan Oksidasi Sketsa
Diantara senyawa senyawa mangan berikut yang mempunyai bilangan oksidasi tertinggi adalah KMnO₄ (B) dengan bilangan oksidasi Mn = +7. Pembahasan : A. Biloks Mn dalam MnO₂ . biloks O = -2. aturan biloks : Bilangan oksidasi dalam senyawa O adalah -2 kecuali dalam peroksida (-1) dan dalam senyawa biner dengan fluor (+2).

Bilangan Oksidasi atom N= 3 terdapat pada senyawa YouTube
3. Bilangan oksidasi atom Cr yang sama dengan bilangan oksidasi atom Mn yang terdapat pada senyawa MnO₂ adalah 4. Bilangan oksidasi Ba pada bilangan Ba₂0₂ adalah 5. Bilangan oksidasi dari H₂O adalah 6. Bilangan oksidasi dari Ag₂O adalah 7. Bilangan oksidasi dari Mn³⁺ adalah 8. Bilangan oksidasi dari H₂SO₄ 9.

Bilangan Oksidasi Atom Mn YouTube
Sifat Kimia. 1. Mempunyai berbagai macam bilangan oksidasi. Unsur transisi memiliki elektron pada orbital d. Energi tiap elektron yang terdapat dalam orbital d hampir setara. Untuk mencapai kestabilan, unsur-unsur ini membentuk ion dengan cara melepaskan elektron dalam jumlah yang berbeda. Oleh karena itu unsur-unsur ini dapat mempunyai 2 macam.