
Laporan Kenaikan Titik Didih Dan Penurunan Titik Beku Reverasite
Pengertian Titik Didih dan Titik Beku. Titik Didih: Titik didih adalah suhu tertentu di mana tekanan udara sekitar zat adalah 1 atmosfer (atau sekitar 101.3 kPa). Pada titik ini, zat cair akan mengalami penguapan secara cepat sehingga berubah menjadi fase gas. Setiap zat memiliki titik didih yang unik dan dapat dipengaruhi oleh tekanan atmosfer.

Rumus titik beku larutan
Besarnya kenaikan titik didih dan penurunan titik beku bergantung pada konsentrasi zat terlarut (Syukri, S. 1999) Penurunan titik beku berbanding lurus dengan penurunan tekanan uap, atau berbandingnya lurus dengan fraksi mol dan untuk larutan encer, keseimbangan ini dapat dianggap berlaku pula terhadap molalitas.

Sulastri buku142 Tugas 131 Contoh Soal Tentukan titik didih dan titik beku 6,20 g larutan
Agar tidakterjadi pemisahan zat terlarut dan fpelarutnya ketika larutan membeku, diperlukan suhu lebih rendah lagiuntuk mengubah seluruh larutan menjadi fasa padatnya. Seperti halnya titik didih, penurunan titik beku (ΔTf) berbanding lurus dengan kemolalan larutan : ΔTf ≈ m ΔTf = Penurunan titik beku Atau ΔTf = Kf x mTf = 0°C - ΔTf Kf.
Kenaikan Titik Didih Dan Penurunan Titik Beku Riset
tentukan titik didih dan titik beku larutan yang mengandung 18 gram glukosa , Mr 180 dalam 500 gram air. jika kb dan kf diketahui. sifat koligatif larutan..
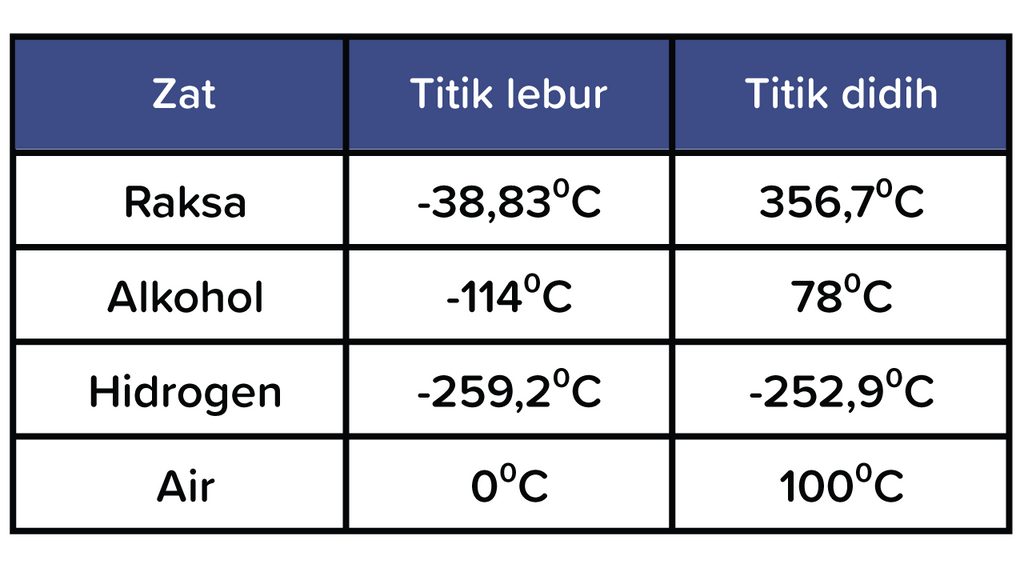
Perhatikan data titik lebur dan titik didih dari e...
Penurunan titik beku cairan pendingin membantu dalam proses pendinginan dan pemindahan panas ini. Penggunaan Baterai Dalam cuaca yang sangat dingin, penurunan titik beku dapat mempengaruhi kinerja baterai kendaraan. Suhu rendah dapat mengurangi kapasitas baterai dan menghambat reaksi kimia dalam baterai.

1 .Sifat Koligatif Larutan _ c. Kenaikkan Titik Didih dan Penurunan Titik Beku Larutan YouTube
Pengertian Titik Beku (Freezing Point) Titik beku (freezing point) adalah suhu tertentu di mana suatu zat berubah dari fase cair menjadi fase padat. Pada titik beku, molekul-molekul atau atom-atom dalam zat bergerak lebih lambat dan memiliki energi lebih rendah, sehingga zat tersebut membeku. Titik beku biasa digunakan untuk bahan yang dalam.

Konsep Mudah Menentukan Titik Didih dan Titik beku (Sifat Koligatif Larutan ) Kimia SMA YouTube
Titik beku dan titik didih adalah dua nilai penting yang digunakan dalam ilmu fisika dan kimia untuk menghitung perubahan suhu dalam zat. Titik beku adalah suhu terendah di mana zat dapat berubah menjadi padat, sedangkan titik didih adalah suhu tertinggi di mana zat dapat berubah menjadi gas. Dengan mengetahui titik beku dan titik didih, kita dapat memahami sifat dan penggunaan zat dengan.

PERHITUNGAN TITIK DIDIH DAN TITIK BEKU LARUTAN NON ELEKTROLIT (SIFAT KOLIGATIF LARUTAN) part 1
Seperti halnya titik didih, penurunan titik beku (ΔTf) berbanding lurus dengan kemolalan larutan : ΔTf ≈ m ΔTf = Penurunan titik beku Atau Kf =Tetapan kenaikan titik beku m = Molalitas ΔTf = Kf x m Tf = 0°C - ΔTf Kf disebut tetapan penurunan titik beku molal. Nilai Kf untuk benzena 5,12 °C m-1.
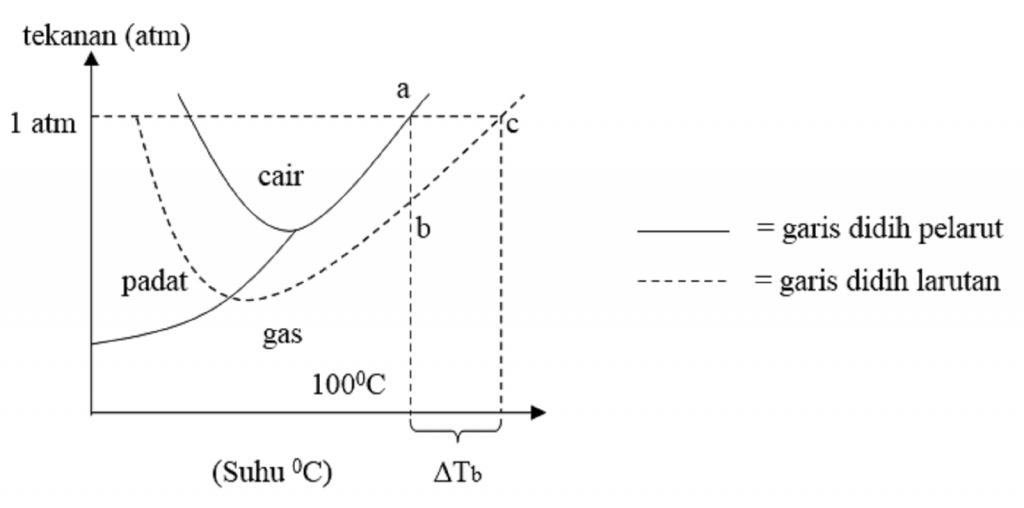
Materi Kenaikan Titik Didih Dan Penurunan Titik Beku Reverasite
T b° = titik didih pelarut murni (air) T b = titik didih larutan. Kenaikan titik didih hanya tergantung pada jenis pelarut dan molaritas larutan, tidak tergantung pada jenis zat terlarut. Jika ditambahkan zat terlarut yang tidak mudah menguap, misalnya gula, maka dibutuhkan kenaikan titik didih yang cukup besar agar dapat mendidih.

Tentukan titik didih, titik beku, dan tekanan osmotic dari larutan 0,1 mol Ba(NO3)2 dalam 500 gr
Identifikasi Miskonsepsi Penurunan Titik Beku dan K enaikan Titik Didih pada . Mahasiswa Pendidikan Kimia . Darius Agung 1, Cindy Fauziah 2, dan Hajidah Salsabila Allissa Fitri 3.

Titik Didih Dan Titik Beku
Tb = 100°C + ΔTb. = 100°C + 0,0416°C = 100,0416°C. Jadi, Tidik didih larutan tersebut yaitu 100,0416°C. Itulah ulasan mengenai √ Titik Didih : Pengertian, Kenaikan, Faktor, Rumus & Contoh Soalnya Lengkap. Semoga apa yang telah diulas dapat bermanfaat bagi pembaca. Sekian dan terima kasih.

SOAL LATIHAN KIMIA TITIK BEKU DAN TITIK DIDH Rozezisme
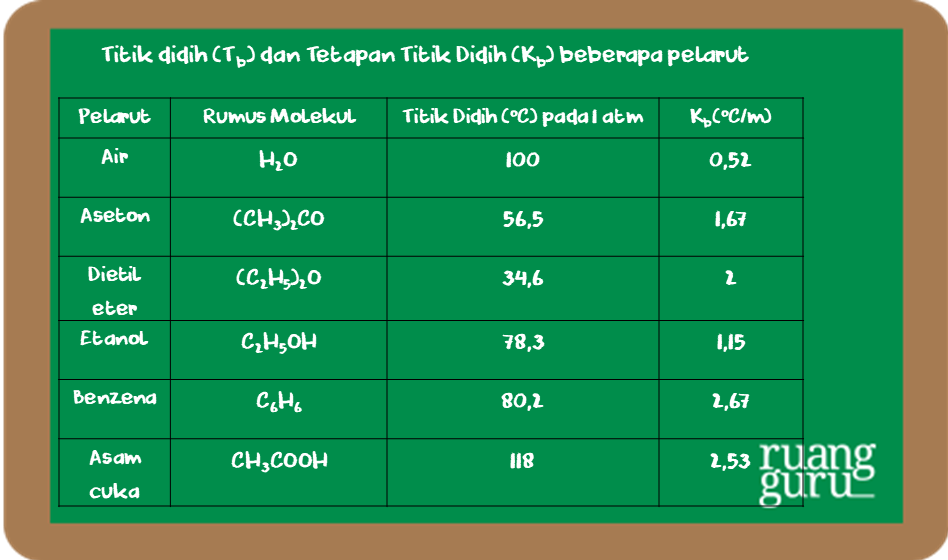
Untuk dapat membandingkan titik didih beberapa zat, di bawah ini diberikan data titik didih larutan dan tetapannya (K b). Untuk menentukan nilai kenaikan titik didih larutan dapat digunakan persamaan sebagaimana penentuan penurunan titik beku larutan. Persamaan yang digunakan adalah: ∆Tb = Tb (larutan) - Tb (pelarut) ∆Tb = m . Kb.
Melihat Proses Kenaikan Titik Didih Kimia Kelas 12
Pengertian Titik Didih. Titik didih adalah suhu tertentu di mana sebuah zat cair berubah menjadi gas ketika dipanaskan. Pada titik ini, cairan menerima energi panas dari lingkungannya, yang menyebabkan partikel-partikel dalam cairan bergerak lebih cepat dan lebih banyak bergerak secara acak. Ketika energi panas yang diberikan cukup kuat untuk.

Unduh Contoh soal titik didih dan titik beku larutan (sifat koligatif larutan) Tonton daring
Menurut Hukum Backman dan Raoult, penurunan titik beku dan kenaikan titik didih berbanding langsung dengan molalitas yang ikut terlarut di dalamnya. Berikut rumus persamaan untuk menentukan penurunan titik beku yang sebanding dengan hasil kali molalitas (m) dengan nilai penurunan titik beku molal (Kf). ΔTf = m x Kf. Keterangan:

Membaca grafik titik didih dan titik beku larutan, pelarutsifat koligatif YouTube
Titik beku menggambarkan transisi cair ke padat sedangkan titik leleh adalah suhu di mana air berubah dari padat (es) ke air cair. Secara teori, kedua suhu akan sama, tetapi cairan dapat didinginkan di luar titik bekunya sehingga tidak memadat sampai jauh di bawah titik beku. Biasanya, titik beku air dan titik leleh adalah 0 °C atau 32 °F .

Pada termometer X titik beku air 40 X dan titik didih air...
Pengertian Titik Didìh, Titik Leleh, dan Titik Beku. Angga Sopyana — September 05, 2023 3:10 pm in Kimia •Comments off. Dalam ilmu fisika ada yang disebut dengan sifat fisika seperti, Titik didih, titik leleh, dan titik beku. Nah dalam artikel kali ini kita akan membahas satu-satu mengenai pengertian dan reaksinya dalam kehidupan sehari.