
LENGKAP ‼️ MENENTUKAN OKSIDATOR, REDUKTOR, HASIL OKSIDASI DAN HASIL REDUKSI YouTube
Pasangan reduktor dan hasinya pada persamaan reaksi tersebut adalah . .. A. NaHSO4 dan Na2S B. NaOH dan Na2S C. Al dan Al2O3 D. NaOH dan H2O E. NaOH dan Al2O3. 7. Unsur N memiliki banyak bilangan osidasi yaitu dari -3 hingga +5. Ion atau molekul berikut yang tidak dapat mengalami rekasi disproporsionasi adalah . . . A. N2 dan NO2 B. N2 dan NH3.

Cara Cepat Menentukan Reduktor, Oksidator, Hasil Reduksi, dan Hasil Oksidasi Reaksi Redoks
Reduktor adalah zat yang menyebabkan zat lain mengalami reduksi dalam suatu reaksi redoks. Hasil oksidasi adalah zat hasil dari reaksi oksidasi. Hasil reduksi adalah zat hasil dari reaksi reduksi. Maka perlu ditentukan perubahan bilangan oksidasi dan reaksi redoksnya: Oleh karena itu, pada reaksi dapat disimpulkan bahwa: Oksidator = I2.
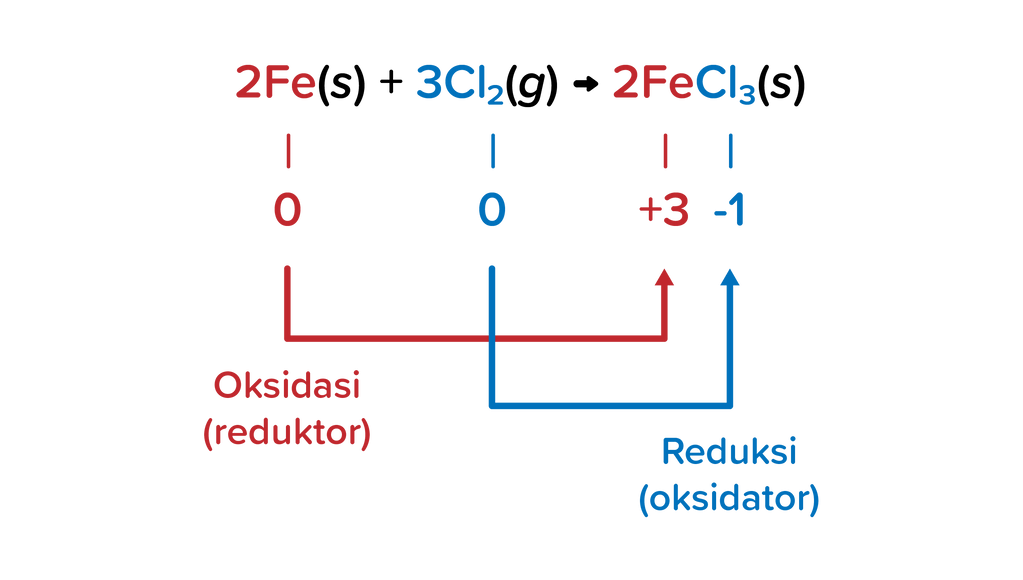
Tentukan reduktor, oksidator, hasil oksidasi, dan
Kata reduksi dan reduktor dalam reaksi kimia selalu bertemu dengan pasangan kata oksidasi dan oksidator. Oksidator dan Reduktor. Senyawa-senyawa yang memiliki kemampuan untuk mengoksidasi senyawa lain dikatakan sebagai oksidatif dan dikenal sebagai oksidator atau agen pengoksidasi. Oksidator melepaskan elektron dari senyawa lain, sehingga.
tentukan oksidator dan reduktor pada reaksi redoks...
Pada contoh diatas Fe adalah reduktor dan Cu sebagai oksidator. Reaksi redoks berdasarkan pengikatan dan pelepasan elektron. Berdasarkan biloks tersebut kita peroleh kesimpulan sebagai berikut: K mengalami kenaikan biloks dari 0 menjadi +1 sehingga menjadi reduktor sedangkan H mengalami penurunan biloks dari +1 menjadi H sehingga menjadi.

Tentukan oksidator dan reduktor dalam reaksi redoks berik...
Oksidasi menjelaskan pelepasan elektron dari sebuah molekul, atom, atau ion. Reduksi menjelaskan penambahan elektron dari sebuah molekul, atom, atau ion. Nah, itu adalah pengertian paling sederhana. Berikut di bawah pengertian yang lebih lanjut: Oksidasi adalah peningkatan bilangan oksidasi. Reduksi adalah penurunan bilangan oksidasi.
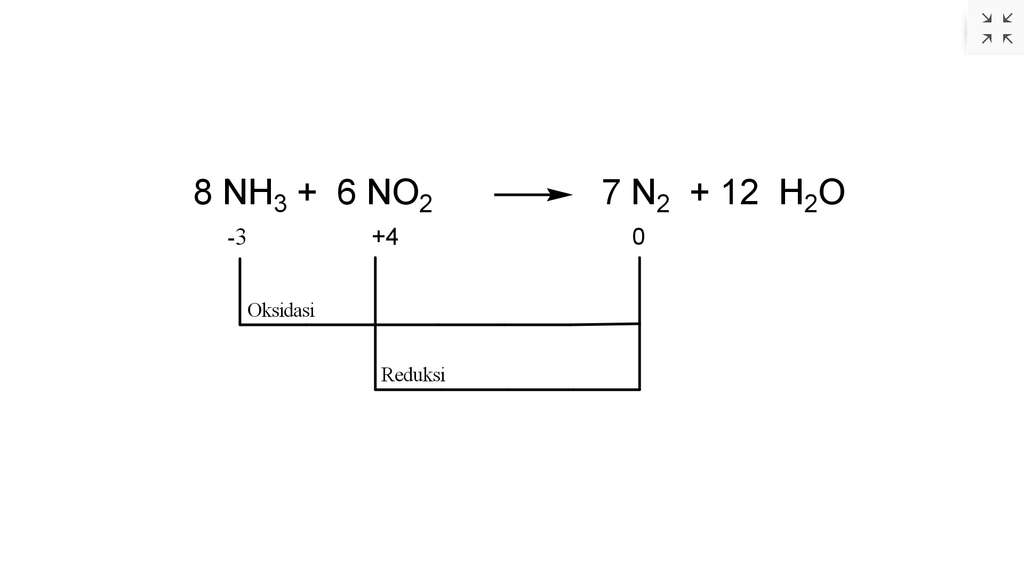
Tentukan Zat Reduktor, Oksidator serta hasilnya da...
Ikut Bimbel online CoLearn mulai 95.000/bulan.IG CoLearn: @colearn.id https://bit.ly/Instagram-CoLearnSekarang, yuk latihan soal ini!Tentukan oksidator dan r.

Latihan 4 (Menentukan Oksidator dan Reduktor)
Contoh Soal Reduktor dan Oksidator. 1. Tentukan reduktor dan oksidator, hasil oksidasi, dan hasil reduksi pada reaksi redoks berikut ini: 2KMnO4 + 5H2C2O4 + 3H2SO4 → K2SO4 + 2MnSO4 + 10CO2 + 8H2O. 2KMnO 4 + 5H 2 C 2 O 4 + 3H 2 SO 4 → K 2 SO 4 + 2MnSO 4 + 10CO 2 + 8H 2 O.

Tentukan Zat Reduktor, Oksidator serta hasilnya da...
Ikut Bimbel online CoLearn mulai 95.000/bulan.IG CoLearn: @colearn.id https://bit.ly/Instagram-CoLearnSekarang, yuk latihan soal ini!Tentukan reduktor, oksid.

tentukan reduktor, oksidator, hasil reduksi dan hasil oksidasi dari reaksi redoks berikut
Reduktor adalah kebalikan oksidator, yaitu zat yang menyebabkan zat lain tereduksi sementara dirinya mengalami oksidasi. Untuk mengetahui mana yang oksidator, reduktor, hasil oksidasi, dan hasil reduksi dari reaksi tersebut, kita tentukan biloks masing-masing unsur dan bagaimana perubahannya. Reaksi dengan perubahan biloks naik disebut reaksi.

Tentukan reduktor, oksidator, hasil oksidási, dan hasil r...
Menentukan Oksidator, Reduktor, Hasil Reduksi dan Oksidasi pada Reaksi Redoks. Selain itu disini juga dibahas cara membedakan reaksi redoks atau bukan.1. Rea.
Tentukanlah oksidator , reduktor, hasil oksidasi d...
Ikut Bimbel online CoLearn mulai 95.000/bulan.IG CoLearn: @colearn.id https://bit.ly/Instagram-CoLearnSekarang, yuk latihan soal ini!Tentukan reduktor dan ok.
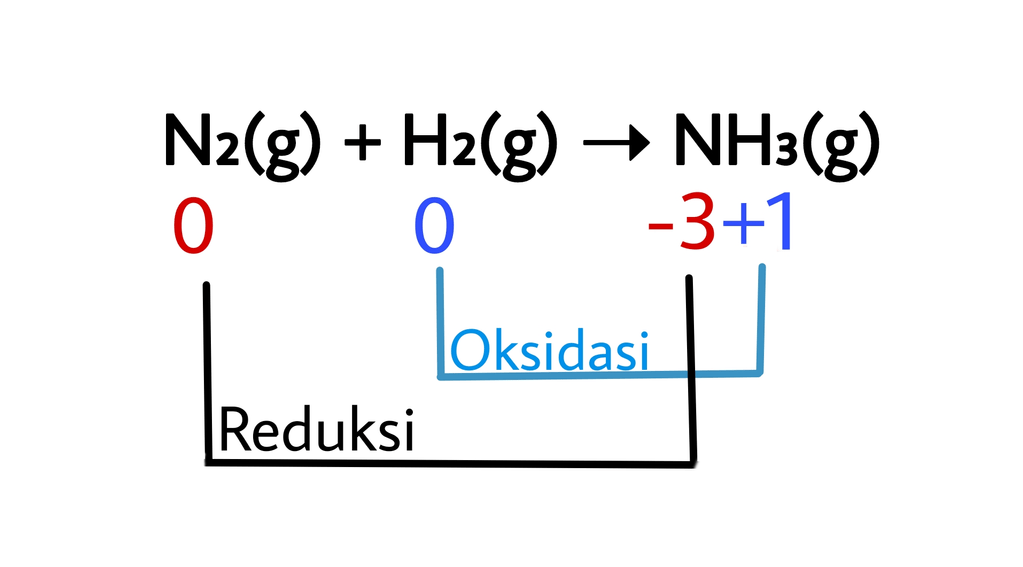
Tentukan oksidator, reduktor, hasil oksidasi, dan
Oke, kita lanjut ya bahasannya! Pada reaksi redoks, terdapat unsur-unsur yang bertindak sebagai reduktor dan oksidator. Zat yang mengalami oksidasi itu disebut reduktor, sedangkan zat yang mengalami reduksi disebut oksidator. Coba perhatikan contoh berikut ini, ya! Reaksi: Mg(s) + 2HCl -----> MgCl2(aq) + H2(g) Karena Mg merupakan unsur bebas, jadi biloks Mg = 0.

Tentukan senyawa yang berperan sebagai reduktor dan oksidator dari persamaan reaksi berikut
Dikutip dari buku Sukses UN 2019 SMA/MA Kimia, Tim Pengajar Ganesha Operation (2018:122), salah satu poin perbedaan reduksi dan oksidasi, yaitu pada reaksi reduksi terjadi penurunan bilangan oksidasi. Sedangkan pada reaksi oksidasi terjadi kenaikan bilangan oksidasi. Bilangan oksidasi merupakan muatan yang berada pada atom tertentu.

Tentukan oksidator, reduktor, hasil reduksi, dan h...
Konsep redoks berkembang, bukan lagi pengikatan dan pelepasan oksigen tetapi pengikatan dan pelepasan elektron. Reaksi oksidasi adalah reaksi pelepasan elektron. Contohnya pada pembentukan ion Na+. Na (s) → Na+(aq) + e-. Sebaliknya reaksi pengikatan elektron disebut reaksi reduksi. Contohnya pada pembentukan ion S2-.

Contoh soal menentukan oksidator dan reduktor
Selengkapnya inilah soal dan jawaban Latihan STS atau PTS dan UTS pelajaran Kimia kelas 10 SMA / SMK / MA Semester Genap dilansir dari sejumlah sumber: • Soal dan Kunci Jawaban Ekonomi Kelas 10 SMA Kurikulum Merdeka, STS PTS UTS Semester Genap. 1. Diantara reaksi rekasi berikut manakah yang merupakan reaksi redoks adalah . . . .

Tentukan oksidasi, reduksi, oksidator dan reduktor dari p...
Pengertian konsep redoks adalah ide atau pengertian yang diabstrakkan dari peristiwa konkret mengenai reaksi kimia yang melibatkan berubahnya bilangan oksidasi atom-atom yang terlibat di dalamnya.. Tuliskan setengah reaksi dari reaksi redoks berikut dan tentukan oksidator dan reduktor.$\mbox{3Mg}(s)+\mbox{N}_{2}(g)\rightarrow\mbox{Mg}{}_{3.