
Suatu Kesetimbangan Dikatakan Dinamis Apabila Dalam Keadaan Setimbang
Ke dalam wadah 1 liter dimasukkan 0,1 mol 𝐻2 dan 0,1 mol 𝑆 mencapai setimbang. Jika 𝐾𝑐 = 3 maka mol 𝐻2𝑆 terbentuk adalah… A. 0,025 B. 0,05 C. 0,075 D. 0,10 E. 0,15 Jawaban: C 7. Pernyataan yang akurat mengenai reaksi irreversible adalah. A. Reaksinya merupakan reaksi balik B. Reaksi irreversible terjadi secara terus-menerus

Koefisien reaksi atau nilai a, b, c, dan d dari persamaan...
Jika {H 3 O +} bertambah {CH 3 CO 2 H} harus bertambah dan CH 3 CO−2 harus berkurang. H 2 O dilepaskan, karena pelarut dan konsentrasinya tetap tinggi dan hampir konstan.. Versi kuantitatif diberikan oleh hasil bagi reaksi. J. W. Gibbs menyarankan pada tahun 1873 bahwa kesetimbangan tercapai saat energi bebas Gibbs dari sistem bernilai minimum (dengan anggapan reaksi dilakukan pada suhu dan.

Kelompokkan reaksireaksi berikut berdasarkan jalannya re...
12. Suatu reaksi dapat balik dikatakan mencapai keadaan setimbang jika.. a. Harga tetapan kesetimbangan Kc = 1. b. Harga tetapan kesetimbangan Kc = 0. c. Kecepatan reaksi kekanan sama dengan kekiri. d. Jumlah mol zat sebelum dan sesudah reaksi sama. e. Massa zat sebelum dan sesudah reaksi sama. Pembahasan:

Pada percobaan reaksi antara logam aluminium dan asam sul...
Halo Google di sini ada soal tentang kesetimbangan kimia suatu reaksi dikatakan mencapai kesetimbangan apabila kita memahami kesetimbangan adalah saat laju ke kanan sama dengan lajur kiri Ini adalah 4 laju pembentukan produk adalah sama dengan laju pembentukan ya kan kita memahami di sini suatu reaksi disebut dalam keadaan setimbang apabila memenuhi tiga syarat yaitu 1 reaksi berlangsung.

Makalah Statika10 Struktur dikatakan berada dalam keadaan setimbang jika dalam keadaan diam
Keadaan seperti ini dikatakan bahwa kesetimbangan bersifat dinamis. Keadaan dinamis hanya terjadi dalam sistem tertutup. Jenis Reaksi Kesetimbangan Dalam Modul Pembelajaran SMA mata pelajaran Kimia Kelas XI (2020), berdasarkan wujud zat-zat dalam keadaan setimbang, reaksi kesetimbangan kimia dibedakan menjadi dua, yaitu kesetimbangan homogen.
5 Tahapan Reaksi Kimia kabarmedia.github.io
Untuk informasi lebih jelas mengenai kesetimbangan kimia, mulai dari pengertian, jenis, rumus, hingga contoh soalnya, kamu bisa menyimaknya dalam ulasan berikut ini, ya! 1. Pengaruh volume terhadap kesetimbangan. 2. Pengaruh tekanan terhadap kesetimbangan. 3. Pengaruh suhu terhadap kesetimbangan. 4.

Sistem pada gambar berada dalam keadaan setimbang. Batang...
Iklan. Pertanyaan. Suatu reaksi dapat balik dikatakan mencapai keadaan setimbang jika. Harga tetapan kesetimbangan. Harga tetapan kesetimbangan. Kecepatan reaksi ke kanan sama dengan ke kiri. Jumlah mol zat sebelum dan sesudah reaksi sama. Massa zat sebelum dan sesudah reaksi sama.

Sistem seperti pada gambar berada dalam keadaan setimbang...
Kesetimbangan kimia adalah keadaan saat kedua reaktan dan produk bertemu dalam konsentrasi yang tidak memiliki kecenderungan lebih lanjut untuk berubah seiring waktu. Secara umum, kesetimbangan dalam reaksi kimia dapat dibagi menjadi dua.. Saat suhu mencapai 100°C, air akan berubah menjadi uap dan tertahan oleh tutup. Apabila pemanasan.

Reaksi Orde Pertama Bolak balik pada Volume Konstan YouTube
Reaksi dapat balik yang berlangsung dalam sistem tertutup akan berakhir dengan kesetimbangan. Kesetimbangan tercapai pada saat laju reaksi pembentukan produk sama dengan laju reaksi pembentukan reaktan. Pada keadaan setimbang tidak terjadi perubahan makroskopis, tetapi pada tingkat mikroskopis reaksi tetap berlangsung.
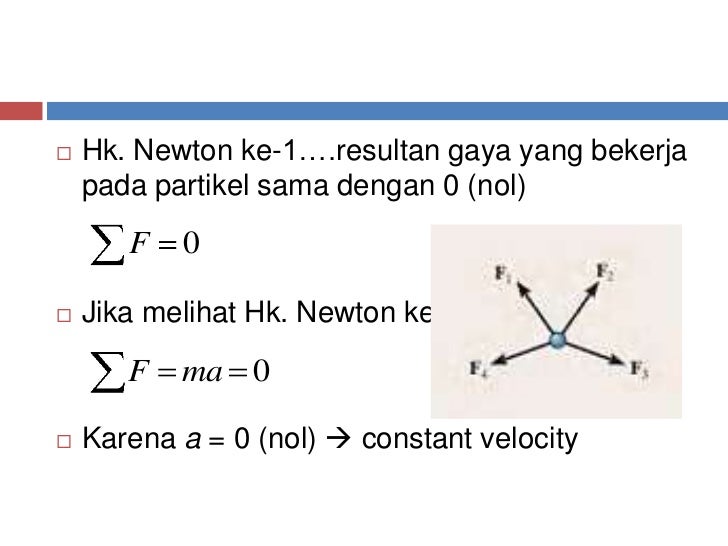
6 Kesetimbangan Partikel Fbd
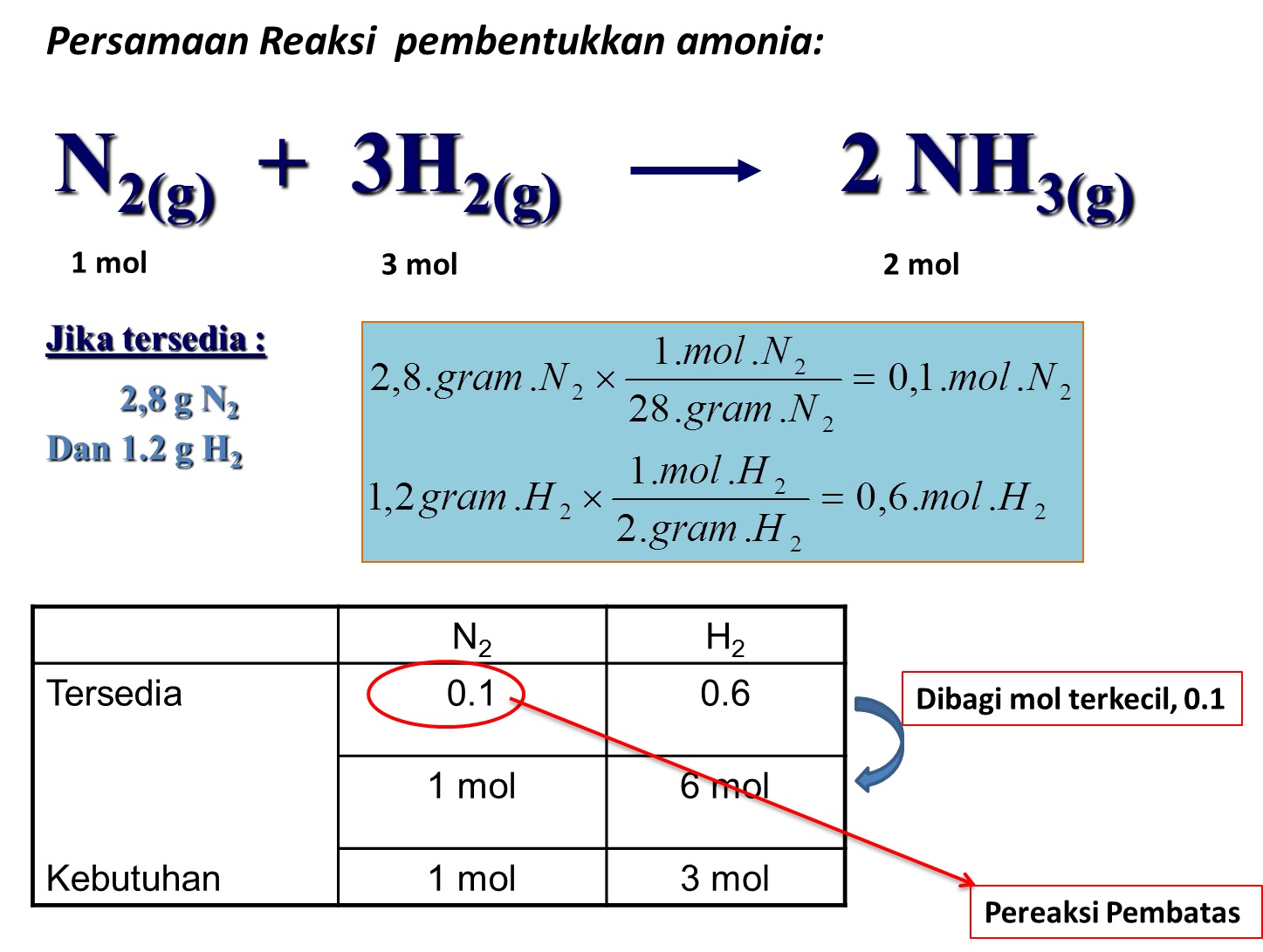
Tuliskan rumusan tetapan kesetimbangan pembentukan amoniak dari gas hidrogen dan gas nitrogen berikut. 3H2(g) + N2(g) ⇌ 2NH3(g) Hitung tetapan kesetimbangan pada soal nomor 2, jika dalam keadaan setimbang (suhu 300°C) 1 Liter campuran gas mengandung 0,15 mol gas hidrogen; 0,25 mol gas nitrogen; dan 0,1 mol gas amoniak.

Kumpulan Soal Dan Pembahasan Kimia Kesetimbangan Reaksi Kelas 11
Suatu reaksi dapat balik dikatakan mencapai keadaan setimbang jika.. Harga tetapan kesetimbangan Kc = 1. Harga tetapan kesetimbangan Kc = 0.. Suatu reaksi dapat balik dikatakan mencapai keadaan setimbang jika.. Harga tetapan kesetimbangan Kc = 1. Harga tetapan kesetimbangan Kc = 0.

Perhatikan Beberapa Contoh Reaksi Pembakaran Berikut 1 Free Nude Porn Photos
PEMBAHASAN SOAL TES HASIL BELAJAR MATERI KESETIMBANGAN KIMIA. Suatu reaksi dapat balik dikatakan mencapai keadaan setimbang jika. A. harga tetapan kesetimbangan Kc = 1 B. harga tetapan kesetimbangan Kc = 0 C. kecepatan reaksi kekanan sama dengan kekiri D. jumlah mol zat sebelum dan sesudah reaksi sama E. massa zat sebelum dan sesudah reaksi sama Pembahasan:(C.) Mula-mula reaksi A dan B.

Suatu Sistem Reaksi Dalam Keadaan Setimbang Bila YPHA.OR.ID
Contoh kesetimbangan reaksi homogen dengan komponen reaksinya gas: N 2 (g) + 3H 2 (g) <==> 2NH 3 (g) Semua komponen baik reaktan maupun produk reaksi adalah berfase gas. Reaksi Kesetimbangan Heterogen. Reaksi kesetimbangan heterogen merupakan reaksi dengan komponen reaksinya terdiri dari fase yang berbeda dapat dua atau lebih fase yang berbeda.

prediksi un kmia 2018 , paket A pembahasan no 16, kesetimbangan reaksi YouTube
Reaksi ke kanan disebut reaksi maju, sedangkan reaksi ke kiri disebut reaksi balik. Persamaan reaksi: A + B ⇌ C; Contoh: 2SO 2(g) + O 2(g) ⇌ 2SO 3(g) Jika suatu reaksi dapat balik berlangsung dalam sistem tertutup dan suhu tetap, maka sistem mencapai kesetimbangan atau keadaan dimana tidak ada perubahan (bersifat dinamis) yang terlihat.

Pada suhu tetap, perbandingan konsentrasi gas [SO2]/[SO3]...
Contoh Soal Kesetimbangan Kimia. Berikut contoh soal kesetimbangan kimia. Campuran 0,5 mol H 2 0,5 mol I 2 ditempatkan dalam sebuah botol stainless steel 1 L pada suhu 430 ℃. Tetapan kesetimbangan K c untuk reaksi. H 2 (g) + I 2 (g) ⇌ 2HI (g) adalah 54,3 pada suhu tersebut. Hitunglah konsentrasi H 2, I 2, dan HI pada saat kesetimbangan..

Pada saat kesetimbangan, dalam suatu ruangan 10 liter pad...
CaCO 3 (s) ⇌ CaO(s) + CO 2 (g). P 4 (s) + 6Cl 2 (g) ⇌ 4PCl 3 (l). Untuk mengetahui apakah reaksi telah mencapai kesetimbangan dan memprediksikan arah reaksi, ditentukan nilai dari kuosien reaksi, Q c, dengan mensubstitusikan nilai konsentrasi masing-masing substansi (produk dan reaktan) pada keadaan setimbang pada konstanta kesetimbangan kimia, K c, dengan nilai konsentrasi awal masing.