
Trik Menentukan Pasangan Asam Basa Konjugasi KIMIA OKE PINTAR
Istilah asam-basa konjugasi merupakan sentral dalam bahasan kesetimbangan asam-basa di SMA/MA, yang di dalamnya terdiri bahasan larutan penyangga atau larutan bufer serta hidrolisis garam.. melepaskan H + atau proton disebut asam, sebaliknya spesi yang dapat menerima H + atau proton disebut basa. Petunjuk cepat menentukan pasangan asam-basa.

Contoh Soal Reaksi Asam Basa Konjugasi Kumpulan Contoh Soal My XXX Hot Girl
Spesi yang merupakan pasangan asam-basa konjugasi adalah.. A. CH 3 COOH dengan HNO 2: B.. Jadi, spesi yang merupakan asam basa konjugasi sesuai dengan opsi yang ada adalah opsi (B). Soal tentang Asam dan Basa UN 2013. Larutan 100 mL H 2 SO 4 0,1 M mempunyai pH sebesar.. A. 1 − log 2: B.

Chocogreentea Keterbatasan Teori AsamBasa Bronsted Lowry
Dan ammonia (NH3) yang telah menerima donor proton berubah menjadi asam konjugasi NH4+. Sehingga pasangan asam basa konjugasinya adalah H2O dan NH3, juga OH- dan NH4+. Kita dapat menentukan mana asam konjugasi mana basa konjugasi dari reaksi kimianya. Jika melepas H+ berarti basa konjugasi, dan jika menerima H+ berarti asam konjugasi.
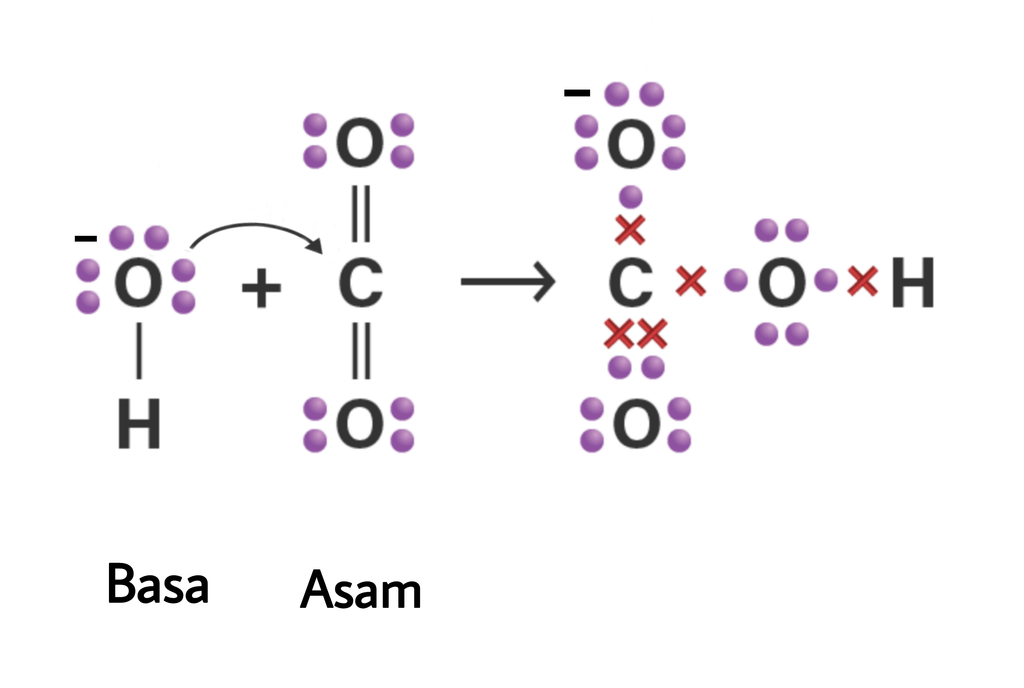
Berdasarkan teori asam basa Lewis, manakah spesi y...
Asam = donor H+. Basa = penerima H+. Reaksi kimia yang bisa dijadikan contoh berdasarkan teori Bronsted-Lowry misalnya pada asam klorida (HCL) dan air (H2O) berikut ini: HCl + H2O ⇌ H3O+ + Cl-. Penjelasannya seperti mengutip pada emodul Kemdikbud: HCL bersifat asam karena itu ia mendonorkan ion H+ nya kepada H20.

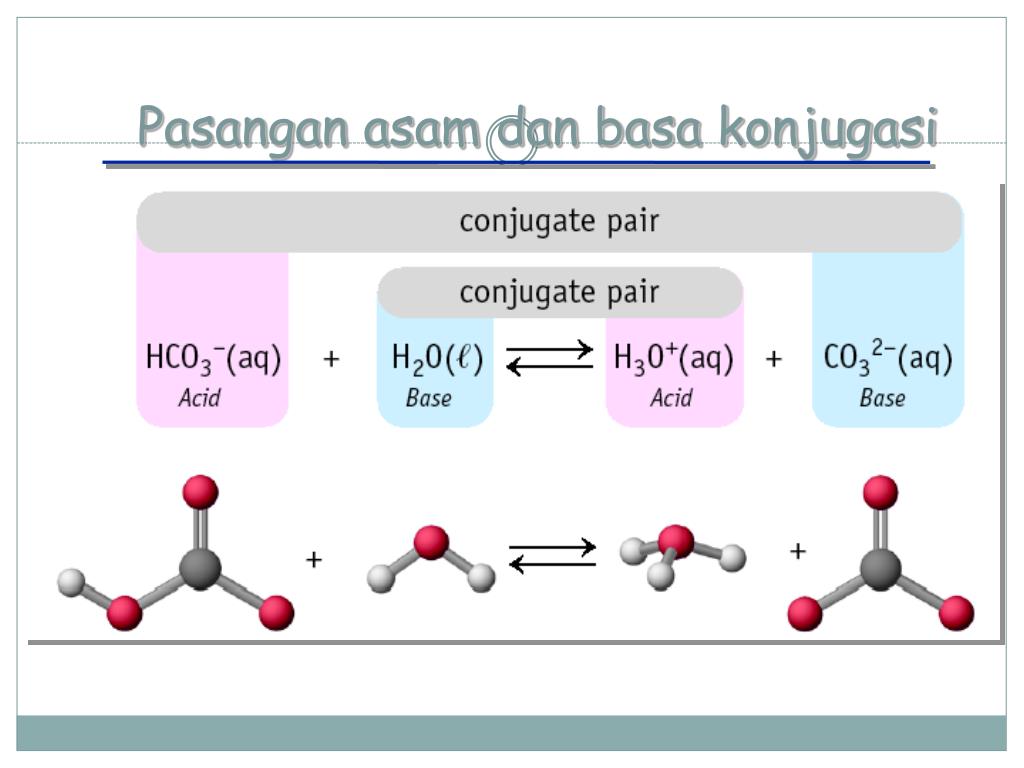
Pasangan basa konjugasi dari (HCO)_(3)^() adalah.a...
Pasangan pertama dalam contoh tersebut adalah pasangan antara asam dengan basa konjugasi merupakan spesi yang tersisa ketika proton dipindahkan dari senyawa asam. Sedangkan pasangan kedua merupakan pasangan yang terjadi antar basa dengan asam konjugasi yaitu akibat dari tambahan proton ke senyawa basa.

Menentukan Pasangan Asam Basa Konjugasi Teori Asam Basa BronstedLowry / kimia kelas 11 YouTube
PPT teori asam basa PowerPoint Presentation, free download ID78826
Asam konjugasi menurut teori asam-basa Brønsted-Lowry dibentuk oleh penerimaan proton (H +) oleh basa; dalam kata lain, asam konjugasi adalah basa yang telah memperoleh ion hidrogen.Di sisi lain, basa konjugasi adalah yang tersisa setelah asam telah memberikan proton dalam suatu reaksi kimia. Maka dari itu, basa konjugasi dibentuk oleh pelepasan proton dari suatu asam.

Tunjukkan pasangan asam basa konjugasi pada reaksi...
Menurut Brønsted-Lowry, asam adalah spesi yang bertindak sebagai pemberi (donor) proton. Menurut Brønsted-Lowry, basa adalah spesi yang bertindak sebagai penerima (akseptor). Maka, HNO 3 dan NO 3 - merupakan pasangan asam basa konjugasi. Serta, H 2 O dan H 3 O + merupakan pasangan asam basa konjugasi. [inline_ads] 3. Zat Amfoter

Teori Asam Basa
Asam menurut Bronsted-Lowry adalah spesi/zat yang mendonorkan proton atau kehilangan atom H pada reaktan, sehingga asam dalam reaksi di atas adalah NH 4 + . Basa menurut Bronsted-Lowry adalah spesi/zat yang menerima proton atau menangkap atom H pada reaktan, sehingga basa dalam reaksi di atas adalah H 2 O. Maka, pasangan asam basa konjugasi.

Spesi berikut yang berperan sebagai basa Lewis adalah.
S uatu asam setelah melepas satu proton akan membentuk spesi yang disebut basa konjugasi dari asam tersebut. Sedangkan basa yang telah menerima proton menjadi asam konjugasi. Perhatikan tabel berikut.. HCl dan Cl - merupakan pasangan asam-basa konjugasi. HCl adalah asam konjugasi dari Cl. H 2 O dan H 3 O + merupakan pasangan asam-basa.

Asam Basa Teori, Contoh, dan Sifat Asam Basa InformasainsEdu
Berdasarkan teori asam basa Bronsted-Lowry, jika dalam suatu reaksi asam dan basa, apabila asam mendonorkan protonnya, maka akan dihasilkan spesies basa konjugasi, sedangkan basa yang menerima proton akan menghasilkan spesies asam konjugasi. Nah, itulah yang dimaksud dengan pasangan asam dan basa konjugasi. Untuk lebih mudahnya, perhatikan 23 pasangan asam dan basa konjugasi berikut: No. Asam

Asam dan Basa Konjugasi
a. HCl dan Cl- merupakan pasangan asam-basa konjugasi. HCl adalah asam konjugasi dari Cl-dan Cl- adalah basa konjugasi dari HCl. b. H2O dan H3O+ merupakan pasangan asam-basa konjugasi. H2O adalah basa konjugasi dari H3O+ dan H3O+ adalah asam konjugasi dari H2O. Berikut ini contoh pasangan asam-basa konjugasi pada beberapa reaksi. a.

LENGKAP ‼️ Cara Mudah Menentukan Pasangan Asam Basa Konjugasi TeoriAsamBasa AsamBasaKonjugasi
Sedangkan, HI dan KCl bukan merupakan reaksi asam basa, melainkan asam dan garam. Sehingga, nggak akan menghasilkan garam dan H2O. Contoh Soal 2. Definisi asam basa menurut Bronsted-Lowry yang tepat adalah.. a. Basa merupakan sifat dari senyawa yang dapat menghasilkan ion OH- dalam air. b.

Asam Basa Teori, Contoh, dan Sifat Asam Basa InformasainsEdu
Asam dan basa adalah larutan elektrolit yang dikenal dengan ciri khasnya, seperti asam yang memiliki rasa masam dan basa yang memiliki rasa pahit. Asam dan basa pengertian menurut Kamus Besar Bahasa Indonesia (KBBI), asam adalah zat yang dapat memberikan proton, zat yang dapat membentuk ikatan kovalen dengan menerima sepasang elektron.

Contoh Soal menentukan pasangan asam basa konjugasi menurut BronstedLowry YouTube
Sedangkan basa yang telah menerima atau menangkap proton dari asam, disebut sebagai asam konjugasi. Berdasarkan reaksi 1. HSO₄⁻(aq) + H₂O(l) ⇌ H₃O⁺(aq) + SO₄²⁻(aq) Asam + Basa ⇌ asam konjugasi + basa konjugasi (Reaksi yang menunjukkan asam basa Bronsted Lowry terlampir) Terlihat bahwa yang merupakan pasangan asam basa.

Teori Asam Dan Basa Menurut Arrhenius Bronsted Lowry Dan Lewis Ezy Blog My XXX Hot Girl
Basa adalah spesi yang bertindak sebagai penerima (akseptor) proton ; Pernyataan yang tepat mengenai teori asam basa Arrenius ditunjukkan oleh nomor.. 1 dan 3. 1 dan 5. 2 dan 3. 2 dan 4. 34. Multiple Choice. 2 minutes. 1 pt. Diketahui rekasi berikut : HNO 3 + CH 3 COOH ↔ CH 3 COOH 2 + + NO 3 - Pasangan yang merupakan asam basa konjugasi.