
Contoh Senyawa Polar Dan Nonpolar Pelarut Polar Non Polar Dan Semi Polar Kita mengetahui
senyawa tersebut merupakan senyawa polar sehingga senyawa dengan tingkat polaritas yang lebih rendah akan berinteraksi lebih lama dengan fase diam yang juga bersifat non-polar (Lee et al., 2007; Novelina et al., 2011). Metabolomik adalah area penelitian yang berfokus pada karakterisasi senyawa metabolit dalam matriks biologis (Krastanov, 2010).

Contoh Senyawa Kovalen Polar
3. Etanol. 4. Asam asetat. · EKSTRAKSI NON POLAR. Non polar adalah senyawa yang terbentuk akibat adanya suatu ikatan antar elektron pada unsur-unsur yang membentuknya. Hal ini terjadi karena unsur yang berikatan mempunyai nilai elektronegatifitas yang sama/hampir sama. Pelarut nonpolar, hampir sama sekali tidak polar.

Senyawa Kovalen Polar Yang Dapat Menghantarkan Arus Listrik Adalah Larutan Elektrolit Dan Non
1 H = 1. 53 I = 2 8 18 18 7. Struktur Lewis HI. H-I. Karena terdapat perbedaan keelektronegatifan, maka senyawa HI termasuk senyawa polar. 3. SiCl 4. Ikatan antara 14 Si dengan 17 Cl. 14 Si = 2 8 4. 17 Cl = 2 8 7. Struktur Lewsi SiCl 4. Karena atom pusat tidak memiliki pasangan elektron bebas (PEB), maka senyawa SiCl 4 termasuk senyawa nonpolar.. 4.

15 10 Contoh Senyawa Polar Dan Nonpolar
Polaritas (kimia) Sebuah molekul air, contoh polaritas yang umum digunakan. Dua muatan hadir dengan muatan negatif di tengah (warna merah), dan muatan positif di ujungnya (biru). Dalam kimia, polaritas (atau kekutuban) adalah pemisahan muatan listrik yang mengarah pada molekul atau gugus kimia yang memiliki momen listrik dipol atau multipol. [1]
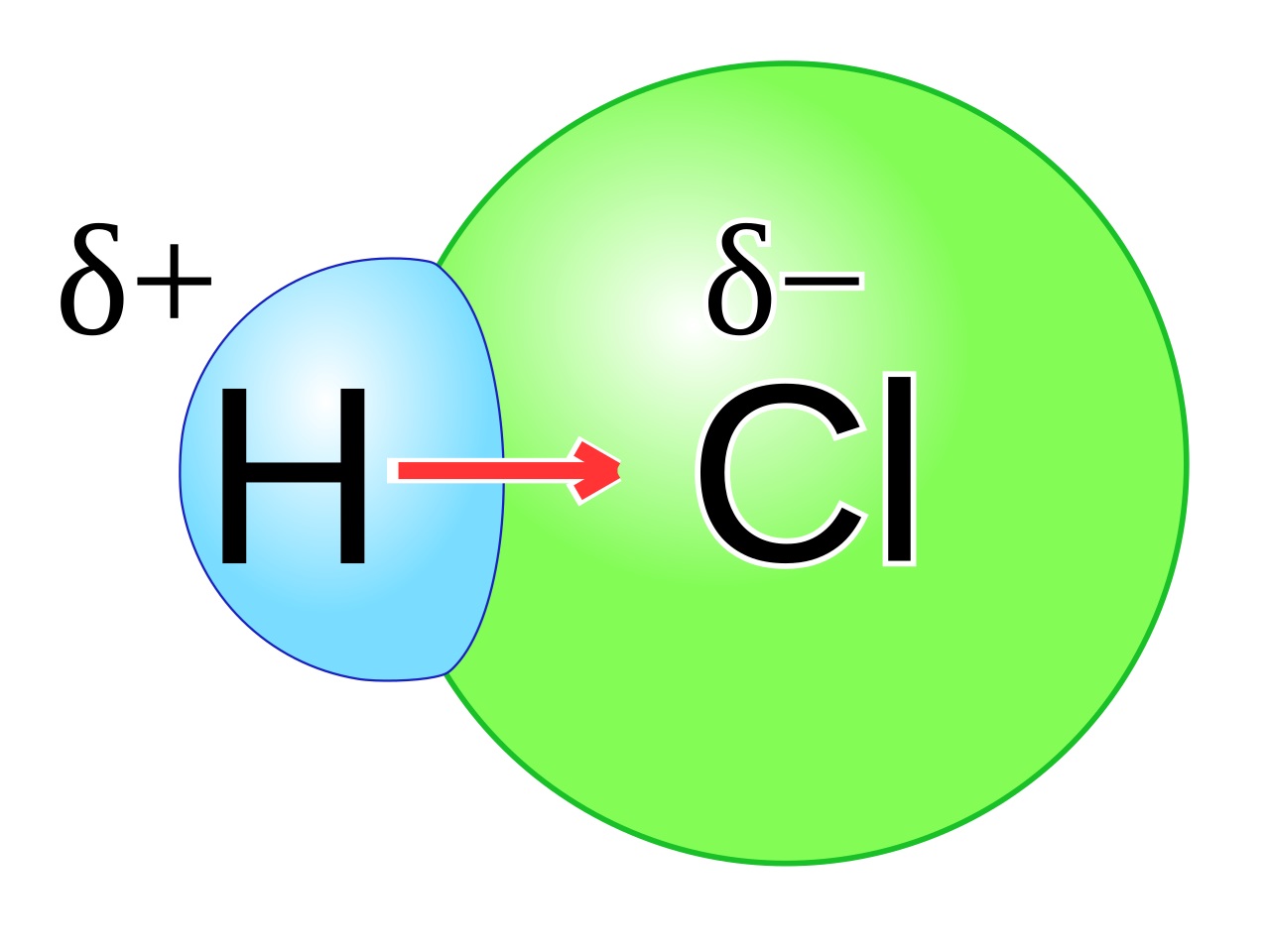
Contoh Senyawa Kovalen Polar
adalah etanol 70% yang bersifat polar, sehingga senyawa flavonoid yang bersifat polar akan tersari dalam etanol 70%. Sesuai dengan penelitian Riwanti tahun 2020,. terpenoid yaitu merupakan senyawa non polar. Fraksi semi polar seperti aglikon flavonoid, alkaloid, polifenol, sedangkan fraksi polar seperti glikosida flavonoid, karbohidrat.

Pasangan Senyawa Berikut Yang Bersifat Polar Dan Nonpolar tanggung jawab kelompok kerja
Ciri - Ciri Senyawa Polar. Ada beberapa ciri-ciri senyawa polar yang diantaranya yaitu: Dapat larut dalam air dan pelarut polar lain. Memiliki kutub + dan kutub - akibat tidak meratanya distribusi elektron. Memiliki pasangan elektron bebas "apabila bentuk molekul diketahui" atau memiliki perbedaan keelektronegatifan.

Perbedan Senyawa Kovalen Polar dan NonPolar Kimia SMA dan SBMPTN Yusuf Studi
Spirulina platensis adalah mikroalga yang dapat dimanfaatkan sebagai suplemen maupun sumber obat alami yang berpotensi sebagai antioksidan.. berbeda, sehingga dapat melarutkan senyawa polar, semi polar dan dapat pula melarutkan senyawa yang bersifat non polar. Setyawan dan Yudha (2013) menyatakan bahwa biomassa sel

Contoh Senyawa Kovalen Polar Dan Nonpolar Terbaru
konsep senyawa polar dan nonpolar, khususnya membedakan senyawa polar dan nonpolar. Vol. 7 No. 1, Februari 2019 Ar-Razi Jurnal Ilmiah ISSN. 2503-4448. adalah metode penelitian yang digunakan untuk menghasilkan produk tertentu, dan menguji keefektifan produk tersebut. Penelitian ini akan mengembangkan produk

Praktikum Senyawa Polar dan NonPolar SMAMuhammadiyah5Jakarta YouTube
senyawa semi polar larut dalam pelarut semi polar .. pelarut semi hingga polar. Flavonoid adalah .. ethyl acetate (semi-polar) and methanol (polar). The results showed that the highest total.
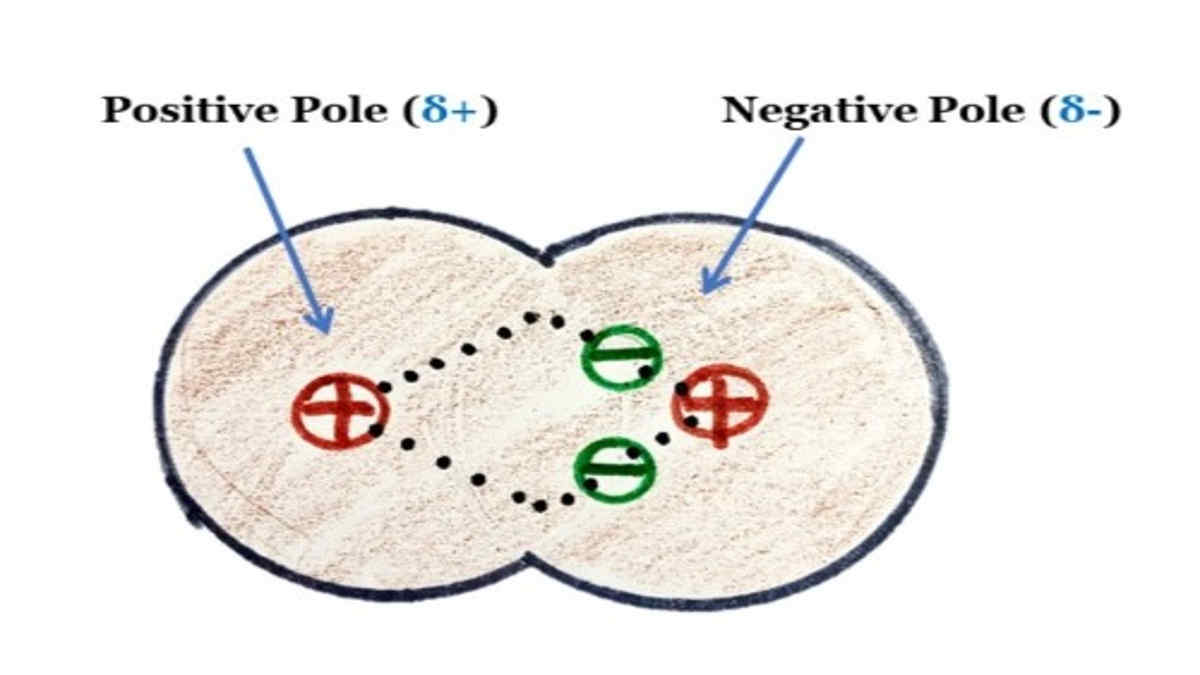
Senyawa Kovalen Polar Pengertian, Sifat, Ciri Beserta Contohnya
GAMBAR SENYAWA POLAR fCIRI - CIRI SENYAWA NON POLAR : tidak larut dalam air dan pelarut polar lain tidak memiliki kutub + dan kutub - , akibat meratanya distribusi elektron - tidak memiliki pasangan elektron bebas ( bila bentuk molekul diketahui ) atau keelektronegatifannya sama. CONTOH : Cl2, PCl5, H2, N2.

🔴IKATAN KOVALEN POLAR & NON POLAR, 🔴SENYAWA KOVALEN POLAR DAN SENYAWA KOVALEN NONPOLAR YouTube
dan organo sulfur (4,20). Senyawa yang mempunyai aktifitas adalah komponen fenol; kavikol, eugenol (non polar dan semipolar); cinamomil klorida (polar) dan senyawa terpena: geraniol, citronella propionate (non polar); cis-pinene (semipolar). Kata Kunci: Piper betle L., fraksi n-heksana, nonpolar, semi polar, polar, analisis GC-MS ABSTRACT

Perbedaan Senyawa Ion Dan Kovalen Polar
Pelarut semi polar adalah jenis pelarut yang memiliki sifat polar dan non-polar. Pelarut ini memiliki daya larut yang baik terhadap senyawa polar maupun non-polar, serta titik didih yang relatif rendah sehingga mudah untuk diuapkan setelah proses ekstraksi selesai dilakukan. Pelarut semi polar umumnya digunakan dalam industri farmasi, kimia.

15 10 Contoh Senyawa Polar Dan Nonpolar
Senyawa fenolik adalah senyawa yang banyak ditemukan pada tumbuhan. Senyawa ini telah diketahui strukturnya, diantaranya adalah kuinon fenolik, flavonoid, fenil propanoid, fenol monosiklik sederhana, polifenol (tannin, lignin. polar dan merupakan pelarut yang serba guna dan sangat baik digunakan sebagai ekstraksi pendahuluan (Harbone 1987.

perbedaan senyawa ion kovalen polar kovalen non polar Sebastian Grant
adalah senyawa pembangun yang diperlukan untuk pertumbuhan dan perkembangan tanaman tersebut, seperti. melarutkan senyawa semi polar, etanol merupakan pelarut yang polar yang dapat

Contoh Senyawa Ion Dan Senyawa Kovalen Polar Merupakan senyawa ion atau kovalen polar. lursdert
👍 Semi polar juga mampu membentuk interaksi ion-dipol dan interaksi hidrogen yang kuat, sehingga molekul semi polar dapat membentuk senyawa polar yang lebih kompleks. 👎 Namun, kekurangan semi polar adalah jumlah molekul yang relative kecil dan variasi jenis molekulnya yang terbatas.

Pasangan senyawa berikut yang bersifat polar dan nonpolar...
KOMPAS.com - Senyawa polar adalah senyawa yang memiliki daerah muatan positif dan negatif yang berbeda (pengkutuban muatan), sebagai hasil ikatan dengan atom seperti nitrogen, oksigen, atau belerang.. Senyawa polar yang terbentuk akibat adanya suatu ikatan antara electron pada unsur-unsurnya. Hal ini terjadi karena unsur yang berikatan tersebut mempunyai nilai keelektronegatifan yang berbeda.