
ecochemical Senyawa Kovalen Polar dan NonPolar
dipengaruhi oleh perbedaan nilai keelektronegatifan. Jika antara atom-atom unsur penyusun senyawa memiliki perbedaan. keelektronegatifan yang kecil atau bahkan nol maka ikatan yang terbentuk adalah ikatan. kovalen nonpolar. Dan sebaliknya, jika perbedaan keelektronegatifan relatif besar maka.

Ikatan Kovalen Polar Dan Nonpolar Beserta Contoh Ikatannya Rumus Kimia Sexiz Pix
Momen dipol akan timbul apabila senyawa kovalen tersebut tersusun dari dua atom dengan keelektronegatifan yang berbeda, seperti HCl dan HBr. 2. Senyawa Nonpolar. Ikatan kovalen nonpolar merupakan ikatan yang pasangan elektron ikatannya tertarik sama kuat kearah atom-atom berikatan, seperti Cl 2, O 2, H 2, N 2.

perbedaan senyawa ion kovalen polar kovalen non polar Sebastian Grant
Ikatan Kovalen Polar. Jenis ikatan kovalen yang jika dilihat berdasarkan muatan di dalam molekul akibat distribusi elektron ikatan, yaitu ikatan kovalen polar dan non polar. Nah, sekarang aku akan membahas dulu tentang ikatan kovalen polar. Ikatan kovalen polar terjadi ketika pasangan elektron ikatan tertarik lebih kuat ke salah satu atom.
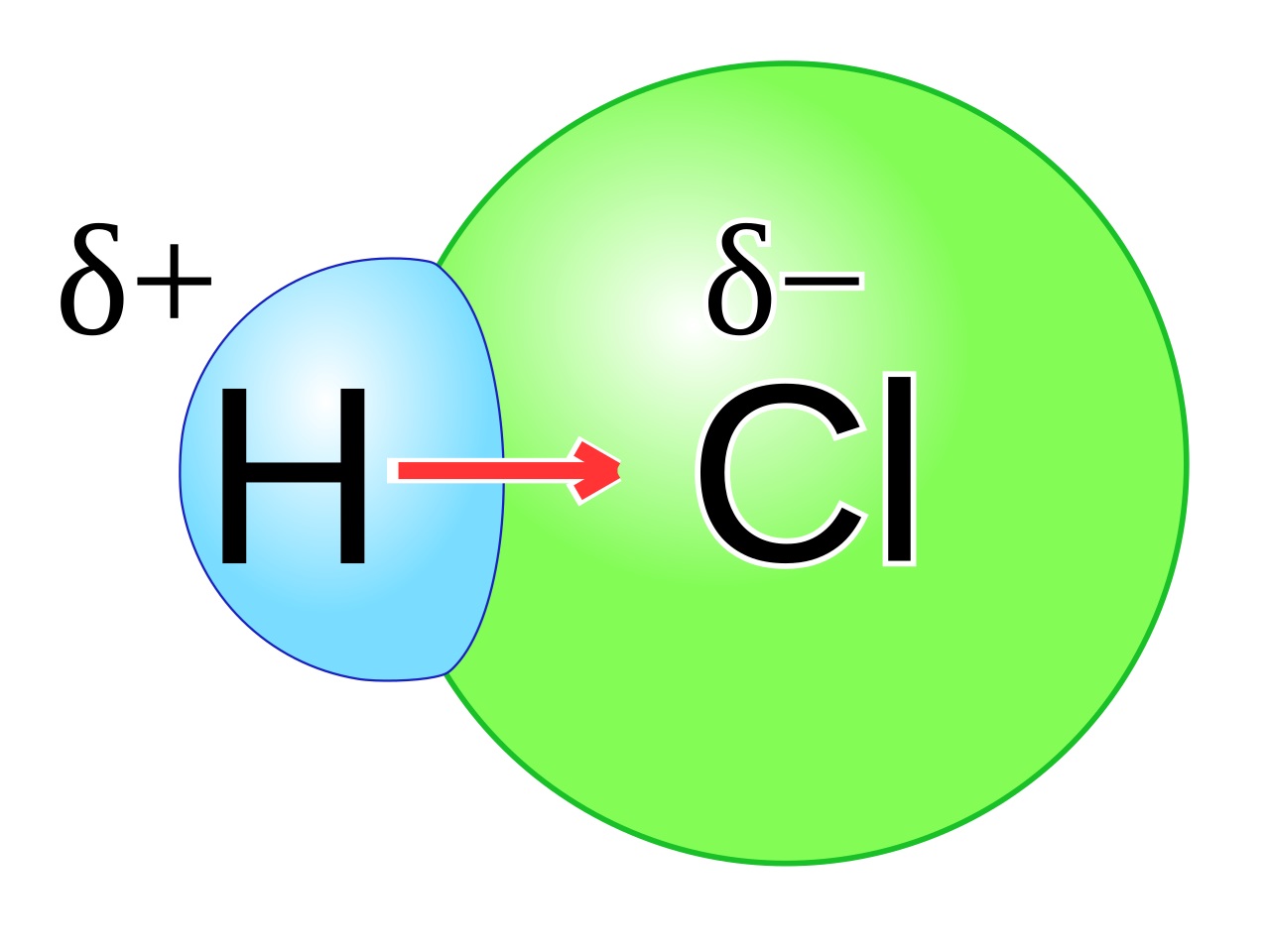
10 Contoh Ikatan Kovalen Polar dan Non Polar dalam Kehidupan Seharihari Materi Kimia
Pelarutan Senyawa Ionik dan Kovalen. Ngomong-ngomong tentang larutan, terbentuknya itu kan karena adanya interaksi antara zat terlarut dan zat pelarut. Nah, yang namanya interaksi, berarti kita akan nyerempet-nyerempet ke jenis ikatan kimia, seperti ikatan ionik, kovalen, polar, dan nonpolar. Contohnya larutan garam (NaCl) dilarutkan oleh air.

Pasangan Senyawa Berikut Yang Bersifat Polar Dan Nonpolar tanggung jawab kelompok kerja
Ikatan kovalen berdasarkan kepolaran di bagi menjadi kovalen non polar, kovalen polar dan Kovalen semoga polar (kovalen koordinasi). Untuk mempermudah dalam.

Contoh Pelarut Polar Dan Nonpolar materisekolah.github.io
Ikatan Kovalen Nonpolar, Polar dan Koordinasi. a. Ikatan kovalen nonpolar. Nah, bila dua buah atom atau unsur yang terikat dalam ikatan kovalen memiliki keelektronegatifan yang sama besar, maka tidak akan mengakibatkan pengutuban atau polarisasi muatan. Hal ini kemudian dinamakan sebagain ikatan kovalen nonpolar. Misalnya pada I 2 dimana.

Perbedan Senyawa Kovalen Polar dan NonPolar Kimia SMA dan SBMPTN Yusuf Studi
Pengertian Senyawa Non Polar. Dilansir dari Encyclopedia Britannica, senyawa non polar adalah senyawa yang tidak memiliki muatan listrik bersih (muatan negatif dan positifnya sama sehingga saling menghilangkan) dan memiliki susunan yang simetris. Artinya, enyawa non polar disebut simetris karena semua sisi atom pusatnya terikat pada elemen dan.

15 10 Contoh Senyawa Polar Dan Nonpolar
Ciri-Ciri Senyawa Kovalen Polar dan Nonpolar. Perlu diingat baik-baik! Pada senyawa kovalen yang memiliki lebih dari dua unsur, kepolarannya ditentukan oleh beberapa hal berikut ini: Jika jumlah momen dipol = 0, senyawa kovalen tersebut merupakan senyawa kovalen nonpolar. Jika momen dipol tidak sama dengan 0, senyawa kovalen tersebut merupakan.

Membedakan Senyawa Kovalen Polar dan Nonpolar YouTube
Senyawa kovalen non polar juga biasanya memiliki bentuk gas atau cair pada suhu kamar. Baca juga: Ikatan Kovalen Koordinasi: Pengertian dan Contohnya. Ikatan kovalen non polar terjadi karena kesamaan keelektronegativan atom-atom yang saling terikat. Di mana jika perbedaan keelektronegativan dua atom di bawah 0,4.

Ikatan kovalen Polar dan Non Polar Alsen Saloka Blog's
Tidak terdapat pasangan elektron bebas, seperti CCl 4, PCl 5, dan SF 6. Senyawa CH 4 atau metana juga termasuk salah satu ikatan kovalen non polar. Senyawa ini memiliki bentuk yang simetris, artinya tidak ada pasangan elektron bebas pada struktur molekul lewisnya. Selain itu, selisih nilai keelektronegatifan atom C dan atom H juga kurang dari 0,5.

Sifat Senyawa Ion, Kovalen Dan PolarNonpolar Ikatan Kovalen PDF
Dari gambar struktur lewis di atas maka senyawa yang berikatan kovalen polar adalah senyawa NH 3, HF dan H 2 O sedangkan senyawa yang berikatan kovalen nonpolar adalah CH 4. Akan tetapi cara menggambarkan struktur lewis satu per satu terasa kurang efisien jika dalam soal terdapat lebih dari 5 jenis senyawa.
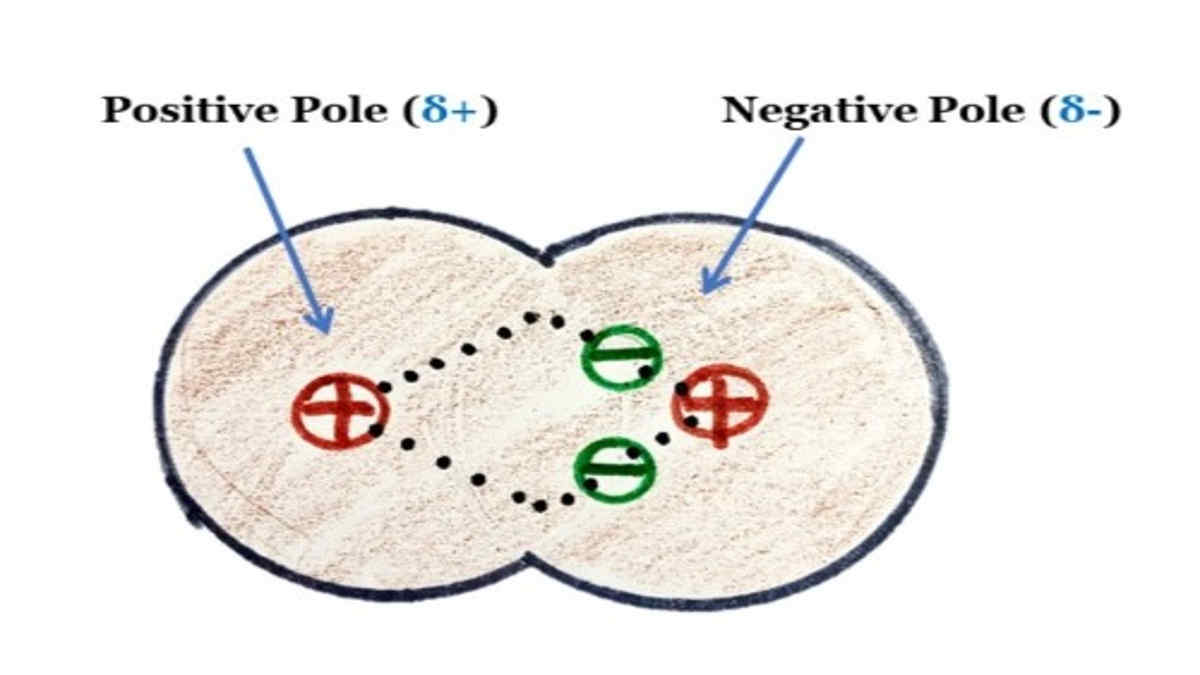
Senyawa Kovalen Polar Pengertian, Sifat, Ciri Beserta Contohnya
senyawa kovalen polar dan nonpolar yang abstrak dan belum dapat memotivasi siswa dalam belajar. Sehingga lebih banyak siswa kurang aktif dalam kegiatan pembelajaran. Penelitian yang dilakukan oleh Latifah, dkk (2014), menyatakan bahwa kegiatan praktikum dalam pembelajaran sangat diperlukan untuk membantu siswa memahami

perbedaan senyawa ion kovalen polar kovalen non polar Sebastian Grant
Contoh ikatan kovalen polar adalah senyawa HF. Atom H memiliki elektronegativitas 2,20. dan atom F memiliki elektronegativitas 3,98. Artinya terdapat perbedaan elektronegativitas sebesar 1,78. Sedangkan, ikatan kovalen nonpolar adalah ikatan kovalen yang terbentuk antara atom-atom yang tidak memiliki perbedaan elektronegativitas. Contoh ikatan.

Contoh Senyawa Kovalen Polar Format Soal
Supaya kamu lebih memahami tentang materi senyawa polar dan nonpolar, perhatikan contoh soal senyawa polar dan nonpolar berikut ini. Tentukan senyawa berikut termasuk senyawa polar atau nonpolar! 1. O2 6. SF4 2. HI 7. SF6 3. SiCl4 8. XeF2 4. HCl 9. XeF4 5. SF2 10. XeF6 Pembahasan Untuk dapat menentukan senyawa tersebut termasuk senyawa
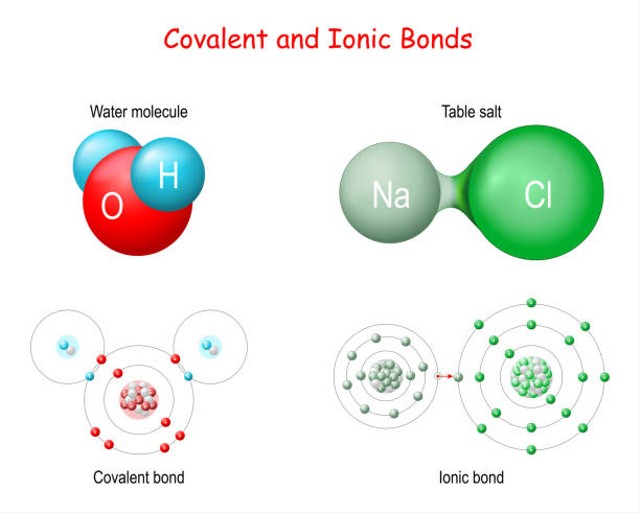
Perbedaan Senyawa Ionik dan Senyawa Kovalen Polar
Senyawa Kovalen Polar Menurut Para Ahli. Sifat Senyawa Kovalen Polar. Ciri Senyawa Kovalen Polar. 1.Terbentuk dari atom-atom yang memiliki perbedaan keelektronegatifan yang cukup besar. 2.Memiliki momen dipol. 3.Mudah larut. 4.Titik leleh dan didihnya yang rendah. 5.Bersifat elektrolit lemah. 6.Bersifat reaktif.
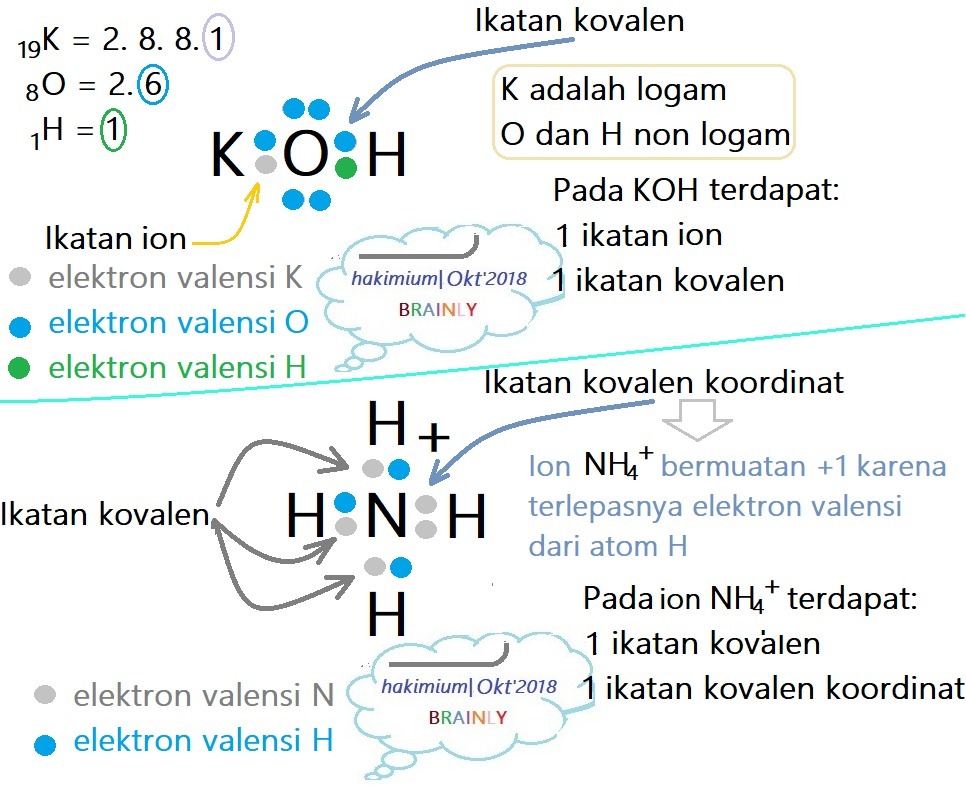
10 Contoh Soal Dan Pembahasan Ikatan Kovalen Polar Dan Nonpolar Materi Kimia Riset
Ciri - Ciri Senyawa Polar. Ada beberapa ciri-ciri senyawa polar yang diantaranya yaitu: Dapat larut dalam air dan pelarut polar lain. Memiliki kutub + dan kutub - akibat tidak meratanya distribusi elektron. Memiliki pasangan elektron bebas "apabila bentuk molekul diketahui" atau memiliki perbedaan keelektronegatifan.