
Tetapan Hidrolisis (nh4)2so4
Hidrolisis Garam - Pengantar. Ketika suatu asam bereaksi dengan suatu basa maka akan dihasilkan senyawa ionik yang disebut garam. Larutan garam dapat bersifat netral, asam, ataupun basa. Hal ini dikarenakan terjadinya hidrolisis garam, yaitu reaksi dari suatu kation atau suatu anion, ataupun keduanya, dengan air menghasilkan ion H + (aq) atau.

Rumus Hidrolisis RUANG BACA
Pembahasan. Nilai tetapan hidrolisis (K h) larutan tersebut adalah 5,6× 10−10. Larutan NH4Cl termasuk garam asam. Tetapan kesetimbangan air (K w) adalah 10−14, maka nilai tetapan hidrolisis (K h) dapat ditentukan dengan rumus sebagai berikut. Kh = = = = KbKw 1,8×10−510−14 0,56× 10−9 5,6×10−10. Besarnya tetapan hidrolisis larutan.

Tetapan Hidrolisis (nh4)2so4
1. Rumus tetapan hidrolisis garam yang berasal dari asam kuat dan basa kuat. Karena perbandingan [H +] dan [OH -] sama, maka larutan bersifat netral sehingga kita tidak memerlukan Kh untuk menghitung pH larutan tersebut, karena sudah dipastikan pH = 7.. 2. Rumus tetapan hidrolisis garam yang berasal dari asam kuat dan basa lemah

Nilai Tetapan Hidrolisis Kh Dari Nh4cl 0 1 M Kb Nh3 = 1 8 Kali 10 Pangkat Min 5 Adalah
Rumus : Di mana : K w = tetapan ionisasi air (10-14) K b = tetapan ionisasi basa [G +] = konsentrasi ion garam yang terhidrolisis. K h = tetapan kesetimbangan hidrolisis . Untuk hidrolisis sempurna (total) pH Hidrolisis total ditentukan oleh harga K a larutan (kekuatan asam) dan harga K b (kekuatan basa), tidak ditentukan oleh konsentrasi garam.

Soal Hidrolisis Garam Dan Penyelesaiannya
Latihan Soal ph Larutan Hidrolisis (Sedang) Pertanyaan ke 1 dari 5. 1. Pertanyaan. Suatu larutan dengan pH p H 5 - log log 2, terbentuk dari reaksi 75 mL larutan NH4OH NH 4 OH 0,4 M dengan larutan H2SO4 H 2 SO 4 0,2 M. Tentukan tetapan hidrolisis dari garam yang terbentuk! 1. 1 ×10−9 1 × 10 − 9. 2. 2 ×10−9 2 × 10 − 9.

Contoh Soal Hidrolisis Asam Lemah Dan Basa Lemah
Hidrolisis: Pengertian, Macam-Macam Reaksi, & Contoh Soal. Dalam industri kimia, pengawet makanan tak jarang digunakan untuk membuat makanan menjadi lebih tahan lama. Beberapa diantaranya merupakan hasil pemanfaatan dari garam natrium asetat yang merupakan salah satu jenis garam organik. Garam ini terbentuk dari basa kuat NaOH dan asam lemah CH.

berapa tetapan hidrolisis dan pH larutan CH3COONa 0,30 M;jika diketahui ka CH3COOH=1,8 ×10
Tetapan keseteimbangan reaksi hidrolisis disebut tetapan hidrolisis (Kw). pH larutan garam dari asam kuat dan basa kuat yang tepat habis bereaksi adalah pH = 7 (netral).. Rumus, dan Penerapannya Juni 13, 2023. Materi Kimia Gaya Antar Molekul, Jenis dan Penerapannya

Pasangan antara reaksi kesetimbangan dengan rumus tetapan...
- [HA] adalah konsentrasi asam lemah. Rumus hidrolisis ini berhubungan dengan tetapan ionisasi asam (Ka) dengan persamaan: Kh = Kw/Ka. Keterangan: - Kw adalah tetapan ionisasi air, yang bernilai 1 x 10^-14 pada 25C. 2. Untuk basa lemah yang mengalami hidrolisis, rumus hidrolisis adalah: Kh = [OH][B+] / [BOH] Keterangan: - Kh adalah tetapan.
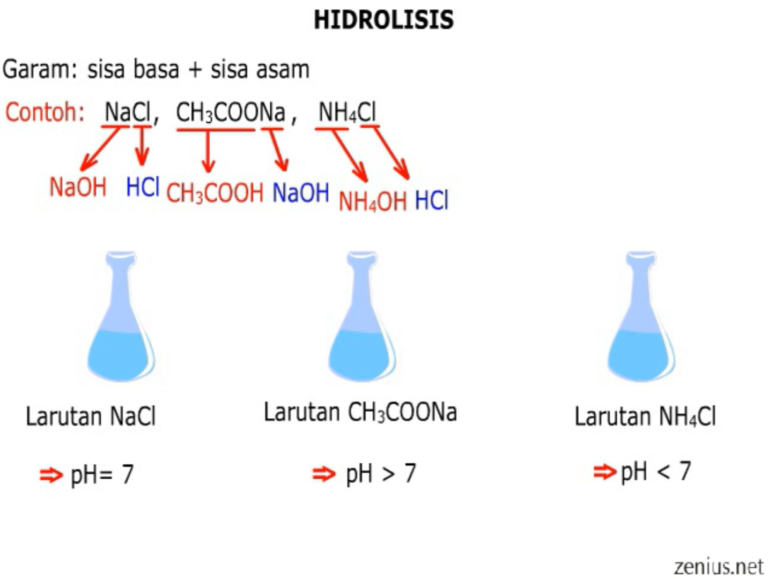
Hidrolisis Garam Materi Kimia Kelas 11
Rumus hidrolisis adalah rumus yang digunakan untuk menghitung tetapan kesetimbangan dari reaksi hidrolisis. Reaksi hidrolisis adalah reaksi yang melibatkan molekul air untuk memecah ikatan kimia dalam suatu senyawa. Rumus hidrolisis bergantung pada jenis senyawa yang mengalami hidrolisis, yaitu asam, basa, atau garam.

Cara Menghitung Ph Asam Lemah Satu Manfaat
Kw = tetapan hidrolisis garam dengan nilai 10-14. Kb = tetapan/konstanta basa lemah [anion] = konsentrasi anion dari garam (M) Jika garam bersifat basa atau terbentuk dari asam lemah dan basa kuat, maka rumus untuk menghitung pH-nya adalah sebagai berikut: Keterangan: [OH-] = konsentrasi ion OH-Kw = tetapan hidrolisis garam dengan nilai 10-14

20+ Contoh Soal Hidrolisis Asam Lemah Dan Basa Kuat Contoh Soal Terbaru
cara mudah menentukan nilai tetapan hidarolisis (Kh) dan pH larutan (NH4)2SO4 0,05 M jika diketahui Kb NH3= 1,8 x 10 -5. dirolisis garam, kimia sma

Tetapan Hidrolisis (nh4)2so4
Pengertian Hidrolisis, Macam, Manfaat, Rumus, dan Contohnya. Oleh Ilmu Kimia Diposting pada 5 Maret 2022. Hidrolisis Adalah. Hidrolisis pada hakekatnya adalah salah satu arti reaksi kimia sederhana yang paling sering terjadi dalam kehidupan kita. Reaksi hidrolisis ini merupakan reaksi yang melibatkan molekul air dalam pemecahan senyawa.

20+ Contoh Soal Hidrolisis Asam Lemah Dan Basa Kuat Contoh Soal Terbaru
TETAPAN HIDROLISIS DAN DERAJAT HIDROLISIS Kelompok v Katharina siena n. ito Ika rezki Ananda Fini novia PENGERTIAN Tetapan hidrolisis (Kh) merupakan tetapan kesetimbangan dari reaksi hidrolisis.. (𝑴)] 𝑲𝒂 Sehingga rumus tetapan hidrolisisnya menjadi : 𝑲𝒘 Kh = atau Pkh = Pkw - Pka 𝑲𝒂 • Banyaknya HA dan ion 𝑂𝐻−.

27+ Contoh Soal Hidrolisis Asam Lemah Basa Lemah Contoh Soal Terbaru
Hidrolisis merupakan satu reaksi kimia yang sering terjadi dalam kehidupan sehari-hari, berikut ini merupakan penjelasan lengkapnya: Skip to the content.. (Mr = 82) sebanyak 410 mg dilarutkan dalam air hingga volume 500 mL. Jika tetapan hidrolisisnya (Kb = 10-2), tentukan pH larutan garam tersebut. Jawab:

Tetapan hidrolisis ( Kh ) dari larutan CH3COONa 0,1 M adalah… ( Ka CH3COOH = 105 dan Kw = 1014
Sehingga, hidrolisis garam adalah reaksi antara salah satu ion-ion garam (kation atau anion) dengan air dan membentuk larutan bersifat asam atau basa. Sifat asam atau basa larutan yang dihasilkan hidrolisis garam bergantung pada jenis asam basa yang membentuk garam tersebut. Baca juga: Hukum Kekekalan Energi: Pengertian, Rumus, dan Penerapannya

K303 Reaksi Hidrolisis Pembuktian/Penurunan Rumus YouTube
Semua jenis K akan mengikuti rumus umum seperti di atas, hanya dilakukan penyesuaian dengan ketentuan yang berlaku untuk setiap jenis K. 1.. Tetapan hidrolisis juga sebenarnya adalah pemendekan istilah dari tetapan kesetimbangan yang diperoleh dari reaksi hidrolisis dari suatu garam. Reaksi hidrolisis adalah reaksi suatu spesi dengan air.