Contoh Soal dan Pembahasan Penurunan Titik Beku (ΔTf) Chemistry is Fun
Penurunan titik beku adalah selisih antara titik beku pelarut dengan titik beku larutan. Penurunan titik beku ini termasuk salah satu sifat koligatif larutan. Dalam perhitungan kimia, penurunan titik beku disimbolkan dengan ΔT f (f berasal dari kata freeze) atau ΔT b . Peristiwa penurunan titik beku ini sering diterapkan pada negara-negara.

Cara Menghitung Tetapan Penurunan Titik Beku Larutan (Kf) (UN Kimia 2018 No. 24) YouTube
Rumus penurunan titik beku kerap digunakan dalam mata pelajaran kimia untuk melihat di suhu berapa sebuah zat akan meleleh. Umumnya, zat yang dihitung dengan rumus tersebut, seperti mentega, air, dan sebagainya. Dengan mengetahui titik beku sebuah zat, maka akan sangat mudah untuk memanfaatkannya dalam kehidupan sehari-hari.

Contoh Soal Penurunan Titik Beku Dan Pembahasan Reverasite Reverasite
Rumus Perhitungan Penurunan Titik Beku. Penurunan titik beku (ΔTb) pada suatu larutan dapat dihitung menggunakan Rumus Colligative Properties, yang terkait dengan penambahan zat terlarut. Rumus ini didasarkan pada hukum Raoult dan dapat dinyatakan sebagai: ΔTb=i⋅Kb⋅mΔTb=i⋅Kb⋅m. Di mana:

Materi Penurunan Titik Beku Beserta Contoh Soal Dan Pembahasan Reverasite
Kf = tetapan penurunan titik beku (ºC kg/mol) Untuk mengaplikasikan rumus di atas, Anda bisa menyimak contoh soal di bawah ini agar meningkatkan pemahaman. Berikut daftarnya.

Penurunan Titik Beku
Besarnya penurunan titik beku larutan diberi lambang ∆T f. Harga ∆T f ditentukan oleh banyaknya partikel zat terlarut dan tidak ditentukan oleh sifat zat terlarutnya. Nilai ∆T f ditentukan berdasarkan rumus Bekmann dan Roult seperti berikut ini. ∆Tf = Tf (pelarut) - Tf (larutan) ∆Tf = m . Kf. Dengan, ∆T f = penurunan titik beku.

10 Contoh Soal Sifat Koligatif Larutan Kenaikan Titik Didih Dan Penurunan Titik Beku Materi
Kuis 11 Penurunan Titik Beku. 50. 50. Rangkuman Penurunan Titik Beku. Kuis Akhir Penurunan Titik Beku. 675. 300. Materi pelajaran Kimia untuk SMA Kelas 12 IPA bab Sifat Koligatif Larutan ⚡️ dengan Penurunan Titik Beku, bikin belajar mu makin seru dengan video belajar beraminasi dari Ruangbelajar.

Diketahui data percobaan penurunan titik beku bebe...
Untuk menentukan perubahan titik beku yang terjadi dapat digunakan rumus dari persamaan Clausius Claypeyron : Keterangan : Kf = tetapan penurunan titik beku molal Masalah yang akan dipecahkan dalam praktikum ini adalah bagaimana menentukan tetapan penurunan titik beku asam asetat dan massa molekul relatif zat X. Dari permasalahan tersebut.

Rumus Penurunan Titik Beku Panduan Lengkap dan Detail
Efek penurunan titik beku pada non-elektrolit dapat dijelaskan dengan menggunakan Rumus Beck (Rumus Clausius-Clapeyron) yang telah dijelaskan sebelumnya: ΔTf = Kf * m * i Di sini, i adalah faktor van't Hoff, yang pada kasus non-elektrolit biasanya memiliki nilai 1, karena zat terlarut non-elektrolit tidak menghasilkan ion.

Menentukan Rumus Molekul Senyawa dari Penurunan Titik Beku YouTube
SBMPTN. 15 Contoh Soal Penurunan Titik Beku: Rumus & Jawaban. Dea Maulida. Contoh Soal Penurunan Titik Beku - Membahas mengenai perhitungan suatu proses kimia terkait zat berbentuk larutan. Dimana reaksi penurunan titik beku tersebut terjadi pada saat suatu larutan saat ditambahkan senyawa lain.

15 Contoh Soal Penurunan Titik Beku Rumus Jawaban Pembahasan Reverasite
Latihan Soal Kenaikan Titik Didih & Penurunan Titik Beku (Sukar) Pertanyaan ke 1 dari 5. Sebanyak 2,85 gram AX2(Mr = 95) dilarutkan ke dalam air sehingga diperoleh 200 mL larutan. Ternyata titik didih larutan tersebut 100, 1404 ∘ C. Ke dalam larutan tersebut ditambahkan 0,95 gram AX2 dan kemudian larutan diencerkan lima kali.

Materi Penurunan Titik Beku Beserta Contoh Soal Dan Pembahasan Reverasite
Penurunan titik beku larutan elektrolit. Rumus penurunan titik beku larutan elektrolit sebagai berikut: ΔT f = K f. m . {1 + (n - 1) α} Keterangan: n = jumlah ion; α = derajat ionisasi; Contoh soal dan pembahasan. Contoh soal 1. Sebanyak 2,4 gram urea (Mr = 60) dilarutkan dalam 50 gram air. Jika Kf air = 1,86 °C/m, tentukanlah titik beku.
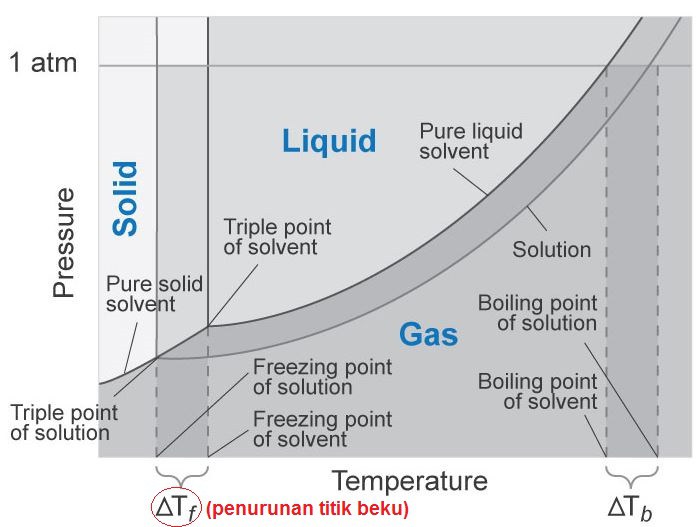
PENURUNAN TITIK BEKU LARUTAN DAN APLIKASINYA
Untuk larutan elektrolit menggunakan rumus: Keterangan: ∆T f = Penurunan titik beku. K f = Tetapan penurunan titik beku molal. n = Jumlah mol zat terlarut. p = Massa pelarut. i = Faktor Van't Hoff. Dalam bidang thermodinamika konstanta titik beku ( K f ) lebih dikenal dengan istilah "Konstanta Kriokopik".
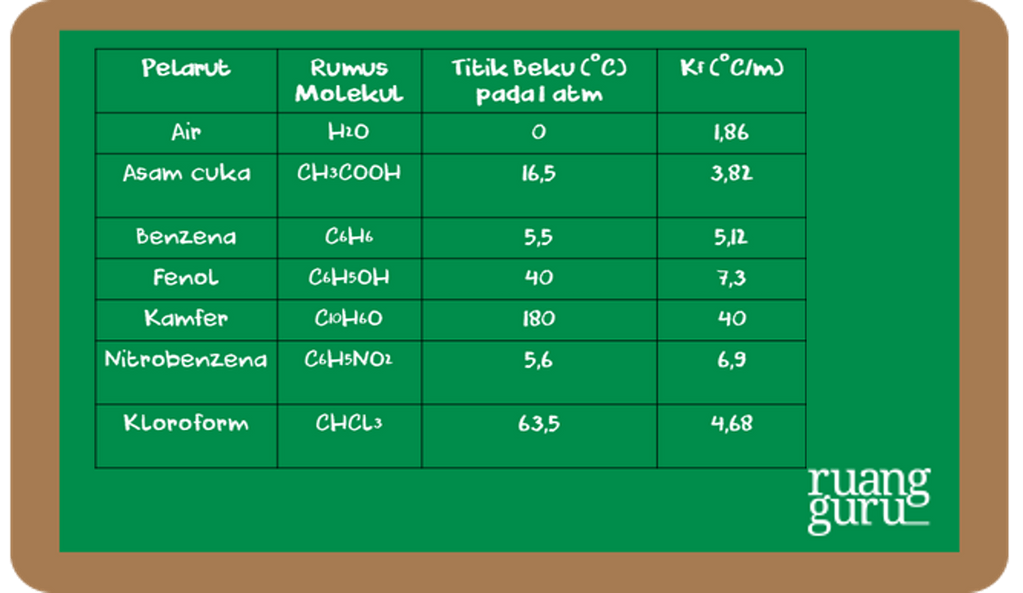
Mengetahui Proses Penurunan Titik Beku Kimia Kelas 12
Contoh larutan elektrolit adalah larutan garam, asam, dan basa. Rumus penurunan titik beku untuk larutan elektrolit adalah: T f = K f . m . i . Penerapan rumus penurunan titik beku dalam kehidupan sehari-hari. foto: freepik.com. Penurunan titik beku ini memiliki banyak penerapan dalam kehidupan sehari-hari, seperti: 1. Pembuatan es krim.

Penurunan Titik Beku Contoh Soal [Pembahasan Simpel] YouTube
Mengenal Rumus dan Contoh Soal Hukum Hess. ∆Tf = Tf (pelarut) - Tf (larutan) ∆Tf = m . Kf. Keterangan: ∆Tf = penurunan titik beku (freezing point depression) m = molalitas. Kf = tetapan penurunan titik beku (ºC kg/mol) Untuk mengaplikasikan rumus di atas, Anda bisa menyimak contoh soal di bawah ini agar meningkatkan pemahaman.

Penurunan Titik Beku
Rumus penurunan titik beku merupakan fenomena fisika di mana titik beku suatu zat cair, seperti air, menurun ketika zat tersebut dicampur dengan zat lain (biasanya dalam bentuk larutan atau campuran). Fenomena ini terjadi karena adanya interaksi antara zat-zat dalam larutan yang mengganggu tata letak molekul atau partikel dalam fase padat.

Penurunan Titik Beku Catatan Pak Rizal
Rumus penurunan titik beku. Besar penurunan titik beku didapat dari selisih antara titik beku pelarut dan titik beku larutan sebagai berikut: Dengan, ΔTf: penurunan titik beku Tf0: titik beku pelarut murni Tf: titik beku larutan. Baca juga: Sifat Koligatif Larutan Elektrolit dan Faktor Vant Hoff .