
Tekanan uap air jenuh pada suhu 30 C adalah 31,8 mmHg dan...
Tekanan yang ditimbulkan oleh uap jenuh air ini disebut tekanan uap jenuh air dan persamaannya disebut dengan rumus penurunan tekanan uap jenuh air. Mengerti tanpa memahami hanya mengotori pikiran yang tak kunjung terisi, ibarat ilmu dan materi yang hanya dipahami dan tidak dimengerti bernilai 50 tapi jika ilmu dan materi dipahami serta.

Animasi Sifat Koligatif Larutan Penurunan Tekanan Uap Free download cek deksripsi YouTube
Oleh karena itu, rumus penurunan tekanan uap jenuh untuk zat elektrolit adalah: ΔP = x B P° {1 + (n - 1)α } Perhatikanlah contoh soal penerapan rumus tekanan uap untuk zat elektrolit. berikut. Contoh Soal. Hitunglah tekanan uap larutan NaOH 0,2 mol dalam 90 gram air jika tekanan uap air pada suhu tertentu adalah 100 mmHg!

Rumus Tekanan Uap Kimia Bit CDN
Contoh Soal Penurunan Tekanan Uap Larutan. 1. Tekanan uap air pada suhu 25 0C adalah 23,76 mmHg. Jika pada suhu yang sama, kedalam 900 mL air ditambahkan urea (Mr = 60 g/mol), tekanan uap larutan menjadi 22,84 mmHg. Penurunan tekanan uap larutan tersebut adalah…. Diketahui:

SIFAT KOLIGATIF LARUTAN PENURUNAN TEKANAN UAP JENUH YouTube
P° = Tekanan uap jenuh dari zat pelarut murni (mmHg) P = Tekanan uap larutan (mmHg) Contoh Soal Penurunan Tekanan Uap dan Penyelesaian Tentukan tekanan uap jenuh air pada larutan yang mengandung 12 % massa urea CO(NH 2) 2, jika diketahui Mr = 60 gram/mol. Penyelesaian: Kenaikan titik didih (∆Tb) Titik didih adalah titik dimana air mendidih.
Contoh Soal Penurunan Tekanan Uap Homecare24
Pengertian Penurunan Tekanan Uap. Ilustrasi penurunan tekanan uap dalam teko. Foto: Pixabay. Disadur dari laman resmi Universitas Malahayati, Francois Marie Raoult menyimpulkan bahwa penurunan tekanan uap adalah tekanan uap jenuh larutan sama dengan fraksi mol pelarut dikalikan dengan tekanan uap jenuh pelarut murni.

Pengertian Dan Contoh Soal Penurunan Tekanan Uap Reverasite
Besarnya penurunan tekanan uap jenuh larutan sebanding (berbanding lurus) dengan fraksi mol zat terlarut (yaitu jumlah zat terlarut) dan suhu. Rumus penurunan tekanan uap jenuh larutan (Δp) adalah sebagai berikut: P ₀ = tekanan uap jenuh pelarut murni (dalam mmHg) Xt = fraksi mol zat terlarut. Dari rumus di atas dapat ditarik kesimpulan, yakni.

Soal dan Pembahasan Penurunan Tekanan Uap Jenuh Bisakimia
Standar IUPAC sekarang ini adalah temperatur 0 °C (273,15 K, 32 °F) dan tekanan absolut 100 kPa (14,504 psi ), [1] sedangkan standar NIST adalah 20 °C (293,15 K, 68 °F) dan tekanan absolut 101,325 kPa (14,696 psi). Dalam bidang industri dan komersial, kondisi standar temperatur dan tekanan bisanya perlu disebutkan untuk merujuk pada kondisi.

Rumus Dan Contoh Soal Penurunan Tekanan Uap Jenuh Kenaikan Titik Didih Rezfoods Resep
Sebaliknya, larutan yang memiliki tekanan uap paling rendah adalah larutan dengan penurunan tekanan uap paling besar. Nilai fraksi mol dalam zat terlarut pun berarti yang paling besar dan larutan 4 lah yang memiliki zat terlarut paling banyak. Sobat Zenius! Itu tadi materi tentang tekanan uap & penurunan tekanan uap.
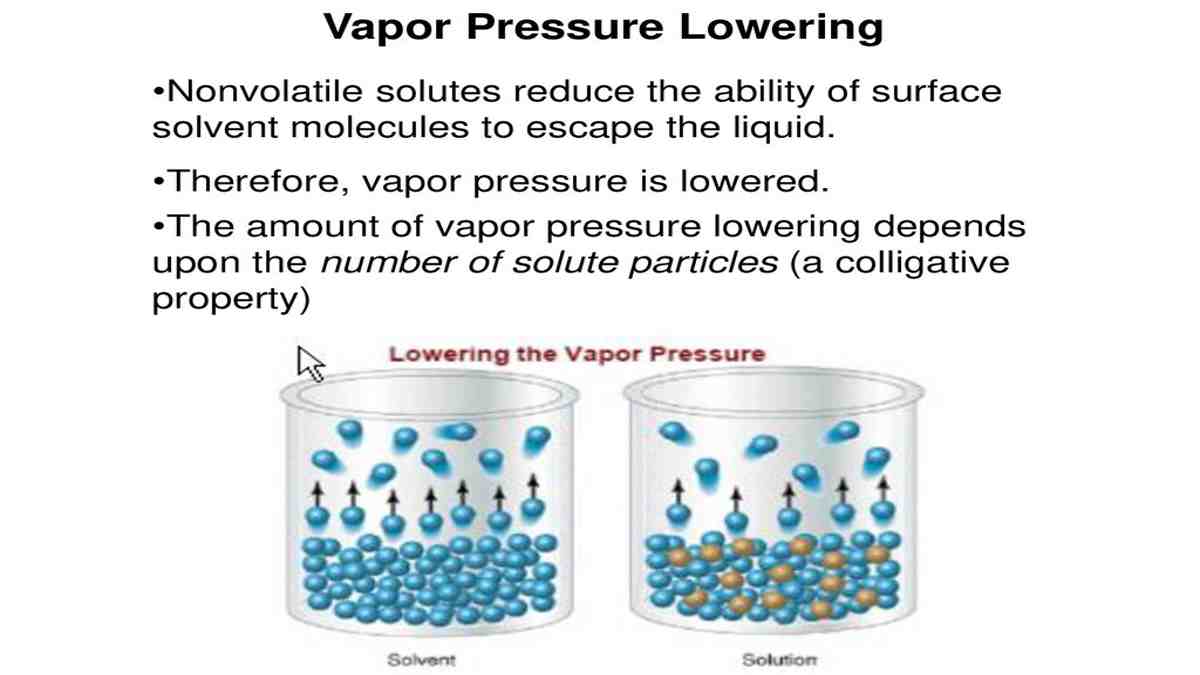
Penurunan Tekanan Uap, Ini Pengertian dan Rumusnya!
Ilustrasi Pengertian Tekanan Uap Jenuh beserta Rumus dan Contoh Soalnya, foto. ADVERTISEMENT. Pada materi kimia, tekanan uap jenuh adalah tekanan yang terbentuk akibat uap jenuh. Di mana terjadinya kesetimbangan dinamis antara zat air dengan uap jenuhnya. Pada keadaan jenuh tetap terjadi proses penguapan dengan disertai suatu proses pengembunan.

Soal Kimia Sifat Koligatif Penurunan Tekanan Uap Jenuh Read Master
Berikut penjelasan kelompok sifat koligatif: 1. Koligatif Larutan - Penurunan tekanan uap jenuh (Δ Tp ) Penurunan tekanan uap jenuh adalah selisih tekanan uap pelarut murni dan tekanan uap larutan . tabel penurunan tekanan uap jenuh larutan non elektrolit dan elektrolit ↓. Uraian. Larutah non elektrolit.

Penurunan Tekanan Uap Sifat Koligatif Larutan YouTube
Rumus penurunan tekanan uap zat elektrolit. Jika zat terlarut membentuk larutan bersifat asam, basa atau garam ternyata rumus penurunan tekanan uap memiliki nilai tidak sama atau lebih besar dari harga yang dihitung menurut perhitungan ideal. Rumus penurunan tekanan uap jenuh zat elektrolit sebagai berikut: ΔP = x B P o {1 + (n - 1) α.

Proses Terjadinya Penurunan Tekanan Uap Kimia Kelas 12 Belajar Gratis di Rumah Kapan Pun
Latihan Soal Penurunan Tekanan Uap (Sedang) Pertanyaan ke 1 dari 5. 1. Pertanyaan. 18,625 gram garam KCl KCl dilarutkan dalam 750 mL air. Tentukan penurunan tekanan uap (ΔP) ( Δ P), bila tekanan uap jenuh air adalah 31,82 mmHg. ( Ar A r K = 39 K = 39; Cl Cl =35,5) 1. 0, 191 mmHg 0, 191 mmHg.

Penurunan Tekanan Uap Larutan Pembahasan Soal YouTube
Tekanan yang ditimbulkan oleh uap jenuh air ini disebut tekanan uap jenuh air dan persamaannya disebut dengan rumus penurunan tekanan uap jenuh air. Dapat digambarkan melalui ilustrasi berikut: Besarnya tekanan uap jenuh untuk setiap zat tidak sama, bergantung pada jenis zat dan suhu. Zat yang lebih sukar menguap, misalnya glukosa, garam.

tentukan penurunan tekanan uap jenuh larutan yang
Contoh Soal Penurunan Tekanan Uap: 1. Tentukan penurunan tekanan uap jenuh ar untuk larutan 9% berat glukosa dalam air, jika diketahui bahwa tekanan uap air 20°C adalah 17,54 mmHg. Misalkan bobot larutan = 100 gram, maka glukosa akan memiliki bobot sebesar 9% dari 100 gram. Berdasarkan Ar, glukosa memiliki Mr = 100 g/mol, sedangkan air 18 g.

Materi Penurunan Tekanan Uap Sekolah Siswa
Rumus Dasar. ΔP = P o.Xt Xt = nt nt+np P = P o − ΔP Δ P = P o. X t X t = n t n t + n p P = P o − Δ P. Keterangan: ΔP Δ P : penurunan tekanan uap larutan P : tekanan uap jenuh larutan Po : tekanan uap jenuh pelarut murni nt : mol zat terlarut np : mol pelarut Xt : fraksi mol zat pelarut. #KOLIGATIF #SMA. FACEBOOK TWITTER.

Tekanan uap jenuh air pada 30 C adalah 31,8 mmHg dan frak...
Masukkan konstanta-konstanta Anda. Persamaan Clausius-Clapeyron memiliki dua konstanta: R dan ΔH uap.R selalu sama dengan 8,314 J/(K × Mol). Akan tetapi, ΔH uap (entalpi penguapan) bergantung pada zat yang tekanan uapnya Anda cari. Seperti yang dituliskan di atas, Anda biasanya dapat mencari nilai-nilai ΔH uap untuk berbagai macam zat di bagian belakang buku paket kimia atau fisika, atau.