
Rumus Molaritas, Definisi, Persamaan Molaritas, Contoh Soal
Contoh penggunaan rumus ini adalah dalam menghitung jumlah molekul air dalam 1 liter air. Kita dapat menghitung berapa mol air yang terkandung dalam 1 liter air, yaitu sekitar 55,5 mol. Dengan menggunakan rumus di atas, kita dapat mengalikan jumlah mol dengan bilangan Avogadro untuk mendapatkan jumlah molekul air, yaitu sekitar 3,34 x 10^25.

Menghitung Jumlah mol jika diketahui Massa Molar Zat dan Massa Molekul Relatif YouTube
As mass/volume = molarity × molar mass, then mass / (volume × molar mass) = molarity. Substitute the known values to calculate the molarity: molarity = 5 / (1.2 × 36.46) = 0.114 mol/l = 0.114 M. You can also use this molarity calculator to find the mass concentration or molar mass. Simply type in the remaining values and watch it do all the.

KONSEP MOL DAN HUKUM GAS Kimiazainal
Rumus menghitung mol suatu senyawa yaitu : n = gram/Mr. Keterangan: n = mol suatu zat (mol) Mr = massa molekul relatif suatu zat (gram/mol) gr = massa suatu zat (gr) Molalitas Larutan (m) Molalitas yaitu besaran yang menyatakan jumlah mol zat terlarut pada tiap satuan berat pelarut. Satuan molalitas ialah molal (m) yang sama dengan mol/kilogram.
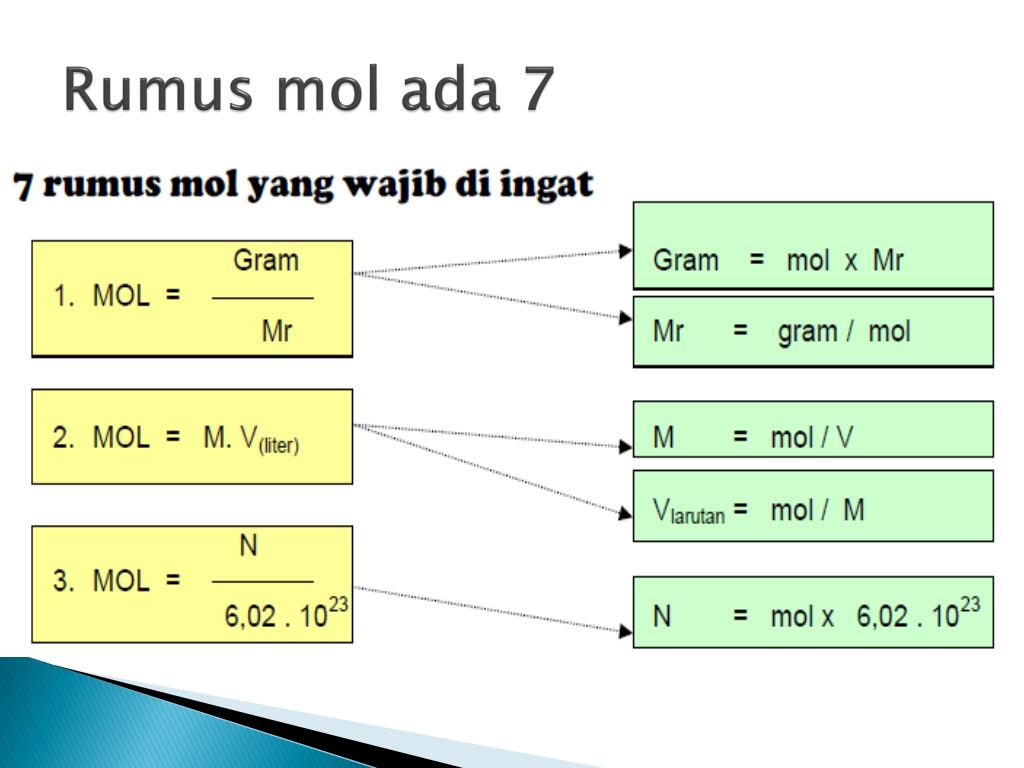
PPT STOIKIOMETRI KIMIA PowerPoint Presentation, free download ID5068620
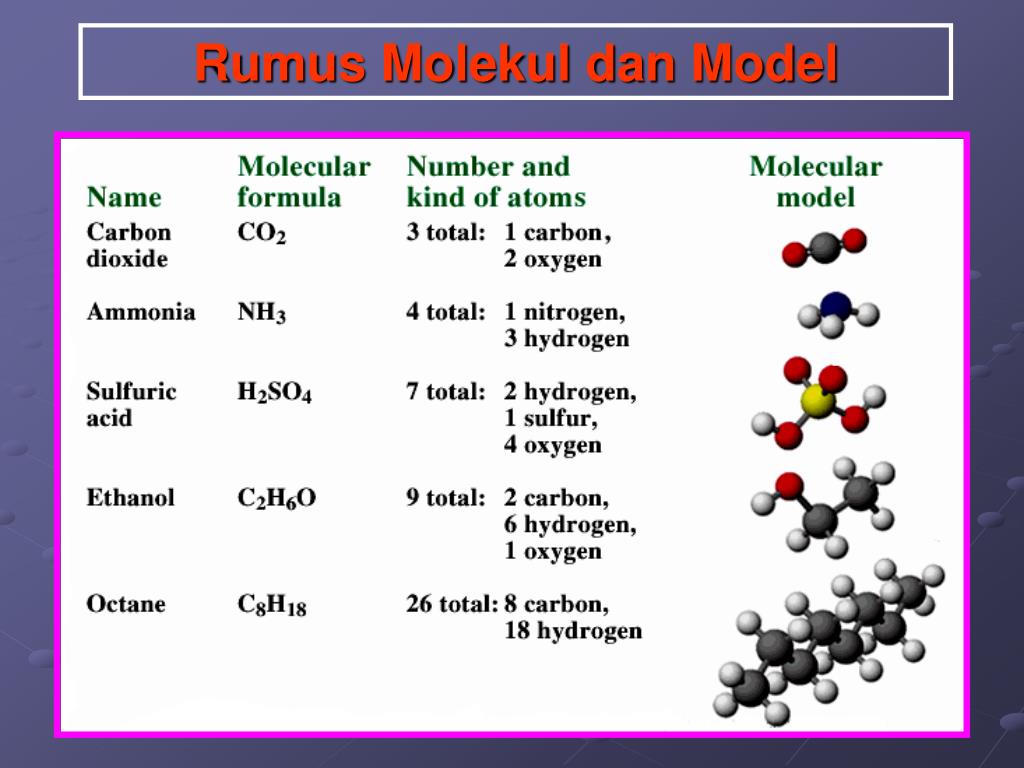
Rumus kimia ini terbagi menjadi 2, yaitu rumus empiris dan juga rumus molekul. Rumus Empiris. Rumus kimia yang pertama adalah rumus empiris. Rumus ini menunjukkan perbandingan dari mol unsur penyusun suatu senyawa. Rumus empiris tidak menunjukkan jumlah sesungguhnya dari unsur penyusun dalam senyawa, namun hanya perbandingan sederhananya.

PPT KONSEP MOL PowerPoint Presentation, free download ID6336687
Rasio mol adalah perbandingan antara jumlah dalam senyawa yang sebagai faktor konversi. Juga dikenal sebagai: Rasio mol juga disebut rasio mol-ke-mol. Satuan perbandingan mol adalah mol:mol atau bilangan tak berdimensi karena satuannya saling meniadakan. Untuk setiap 1 mol O2 yang. Untuk setiap 2 mol H Jika 4 mol hidrogen digunakan, maka 4 mol air.
PPT Konsep Mol dan Stoikiometri PowerPoint Presentation, free download ID5410845
Dalam bidang kimia ada beberapa satuan yang sering digunakan untuk menyatakan konsentrasi larutan ( banyaknya zat terlarut dalam sejumlah pelarut ). Beberapa satuan konsentrasi itu antara lain : mol, molalitas, molaritas, normalitas, ppm, persen massa, persen volum. Berikut akan saya jelaskan pengertian dan rumus dari satuan-satuan di atas : 1.

Fraksi mol dan molalitas (m) Soal dan Pembahasan KIMIA KELAS 12 YouTube
Contoh Soal Konsep Mol Beserta Jawabannya. 1. Sebanyak 4,9 gram H2SO4 H 2 SO 4 dilarutkan dalam air sehingga diperoleh 500 mL larutan. Tentukan jumlah ion yang yang terlarut dalam larutan dan tentukan konsentrasi ion H+ H +. Jawaban contoh soal konsep mol dan penyelesaiannya. nH2SO4 = m Mr = 4, 9 98 = 0, 05 mol n H 2 SO 4 = m M r = 4, 9 98 = 0.

Pengertian Mol Konsep dan Penggunaannya dalam Kimia
Rumus Mol. Jika kamu diminta untuk menentukan mol dari suatu zat yang diketahui massanya, gunakan persamaan berikut. Dengan: n = mol; m = massa zat; dan. Mr = massa molekul relatif. Langkah-Langkah Menentukan Fraksi Mol. Untuk memudahkanmu dalam menentukan fraksi mol, yuk ikuti langkah berikut.
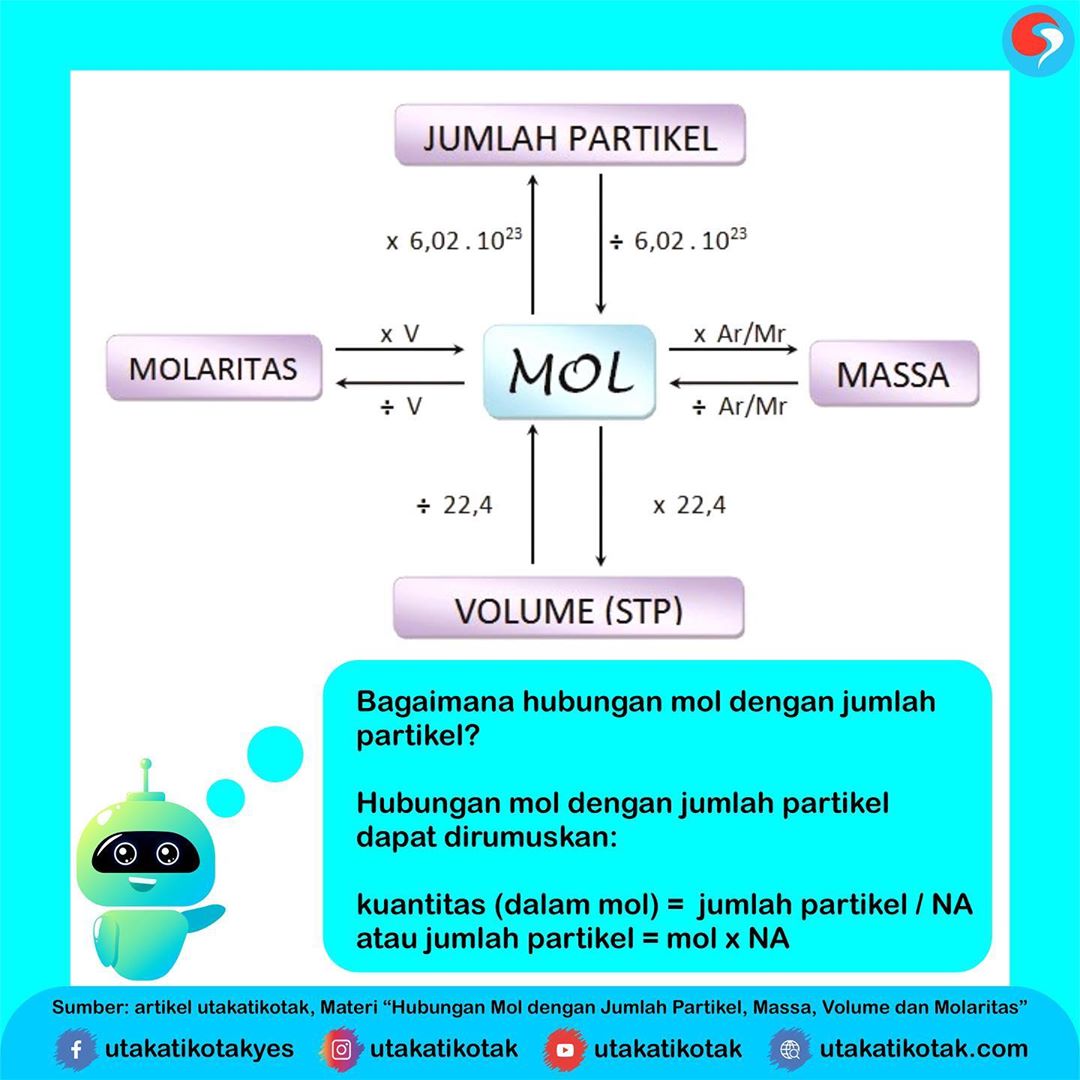
Hubungan Mol dengan Jumlah Partikel, Massa, Volume dan Molaritas
Dikutip dari Buku Pintar Pelajaran Ringkasan Materi dan Kumpulan Rumus Lengkap, Drs. Joko Untoro & Tim Guru Indonesia, (2010: 137) pengertian mol adalah satuan jumlah zat yang dipergunakan dalam perhitungan kimia. Sedangkan satu mol adalah satuan banyaknya partikel atau merupakan penyederhanaan jumlah partikel suatu ion, molekul, atau unsur.
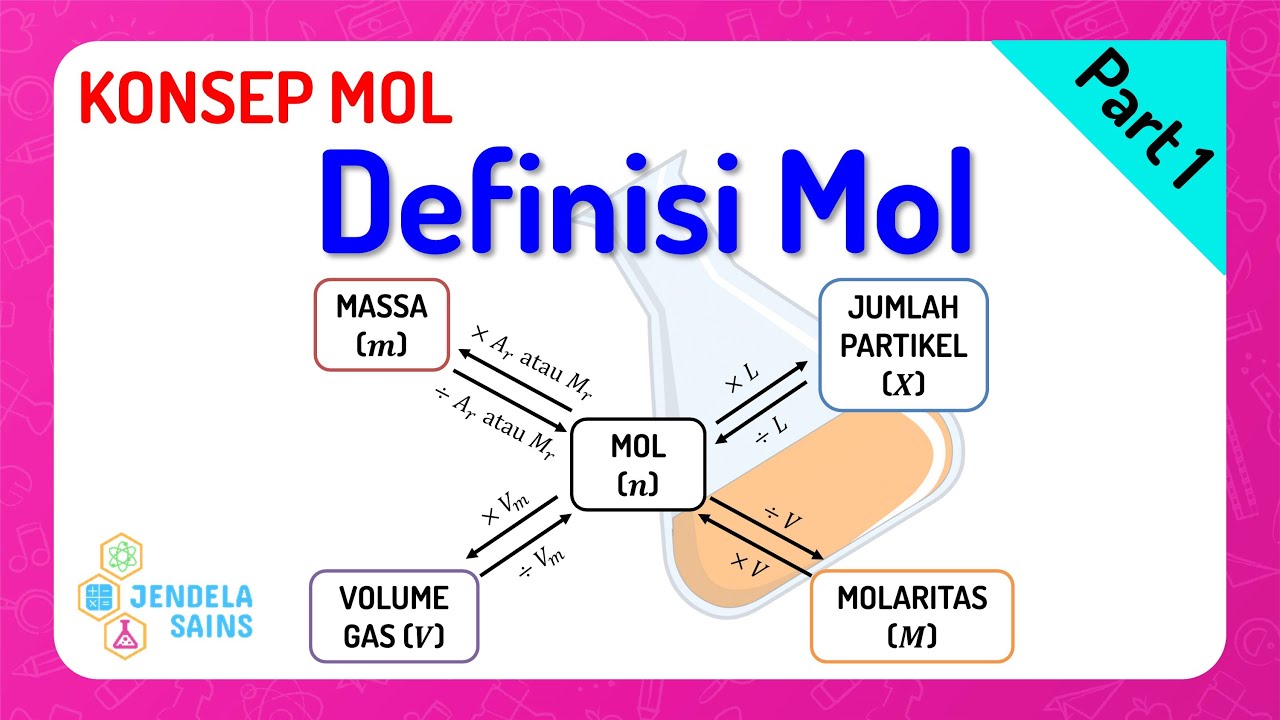
Konsep Mol Kimia Kelas 10 • Part 1 Hubungan Mol & Massa, Jumlah Partikel, Volume Gas, Molaritas
Rumus fraksi mol zat pelarut. Zat pelarut adalah suatu zat yang dapat melarutkan bahan lain dan membentuk campuran atau larutan. Biasanya, zat pelarut merupakan zat cair baik yang bersifat polar maupun non polar. Rumus fraksi mol zat pelarut adalah: Dengan, xp: fraksi mol zat pelarut. np: jumlah mol zat pelarut.

Belajar Kimia Rumusrumus dasar Konsep Mol YouTube
Rumus Mol. Tonton video Pengertian Mol serta Hubungan antara Mol dengan Massa Suatu Zat. Gimana biar lebih paham dengan rumus-rumus di atas kita langsung praktekkan aja nih guysss ke contoh soal. Contoh soal 1. Berapa sih volume dari 23 g gas NO₂ yang diukur pada tekanan 1 atm dan suhu 27°C?
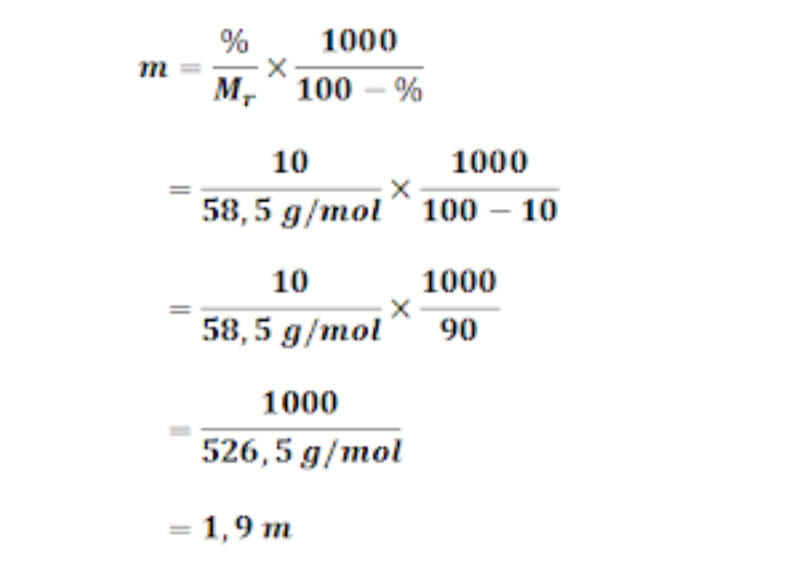
Cara Menghitung dan Contoh Soal Fraksi Mol dan Jawabannya Rumus dan Pembahasan Fraksi Mol
Konsep mol Kimia ternyata enggak sesulit yang dibayangkan, lho. Simak penjabaran konsep, pengertian, dan latihan soalnya di sini, yuk. SBMPTN.. Senyawa kimia identik dengan rumus-rumus kimia yang dinyatakan dengan unsur-unsur tertentu, contohnya air (H 2 O), oksigen (O 2), dan glukosa (C 6 H 12 O 6). Setiap unsur penyusun tersebut memiliki.

Soal Mol Penjelasan Lengkap dan Komprehensif tentang Mol dalam Kimia
Both ppm (parts per million) and molarity are measures of concentration. Did you know that ppm is used in different ways depending on the context? When dealing with dilute solutions, 1 ppm can be approximated as 1 mg 1\ \text{mg} 1 mg of substance per liter of water, or 1 mg / L 1\ \text{mg}/\text{L} 1 mg / L.. On the other hand, molarity is molar concentration, meaning that it tells you how.
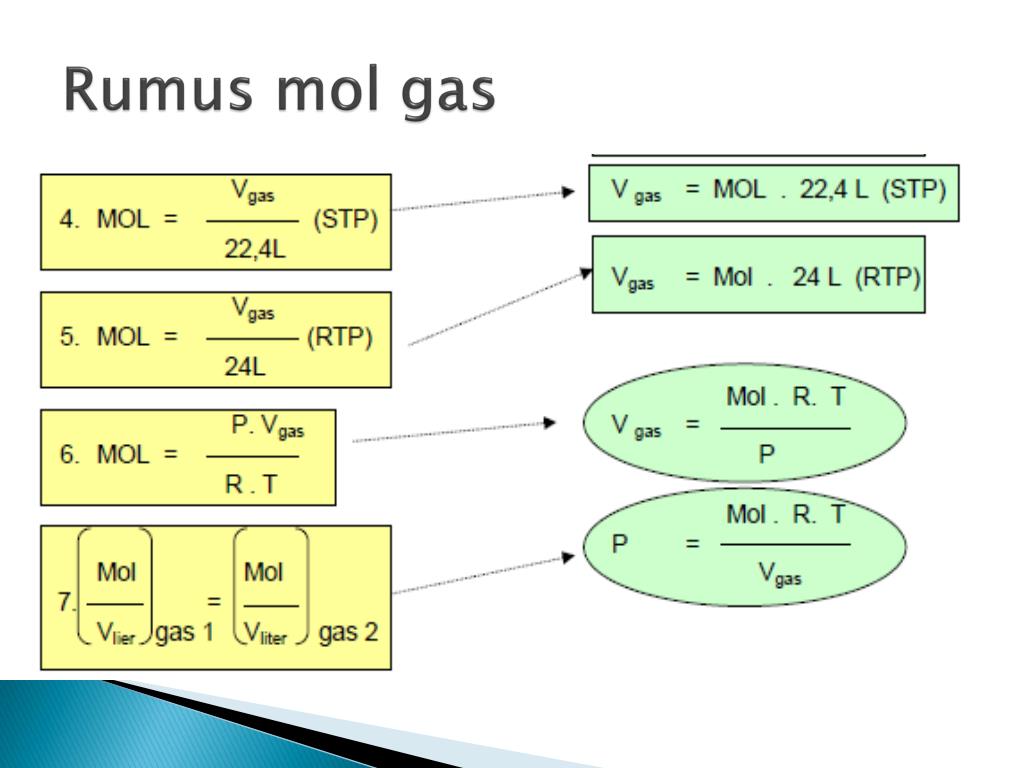
PPT STOIKIOMETRI KIMIA PowerPoint Presentation, free download ID4269409
Pengertian, Konsep, Rumus Mol. Ilustrasi Pengertian, Konsep, Rumus Mol, Foto: Unsplash/coffeekai. Dikutip dari buku Pendekatan Pembelajaran Sains Berbasis Konstruktivis Ed. Revisi, Srini M. Iskandar (2022: 168), terdapat pengertian, konsep, rumus mol yang perlu diketahui. Jadi, reaksi kimia berlangsung antara partikel-partikel pereaksi dalam.

Konsep Mol Pada Kimia Rezfoods Resep Masakan Indonesia
Setelah mempelajari mol & konsep stoikiometri, maka kita telah menguasai dasar-dasar dari salah satu cabang kimia yakni kimia analitik, yang berkutat mengenai jumlah zat dan perubahannya dalam reaksi. Untuk mulai belajar materi & contoh soal Mol & Stoikiometri dan penyelesaiannya kamu bisa langsung klik daftar materi dibawah ini.
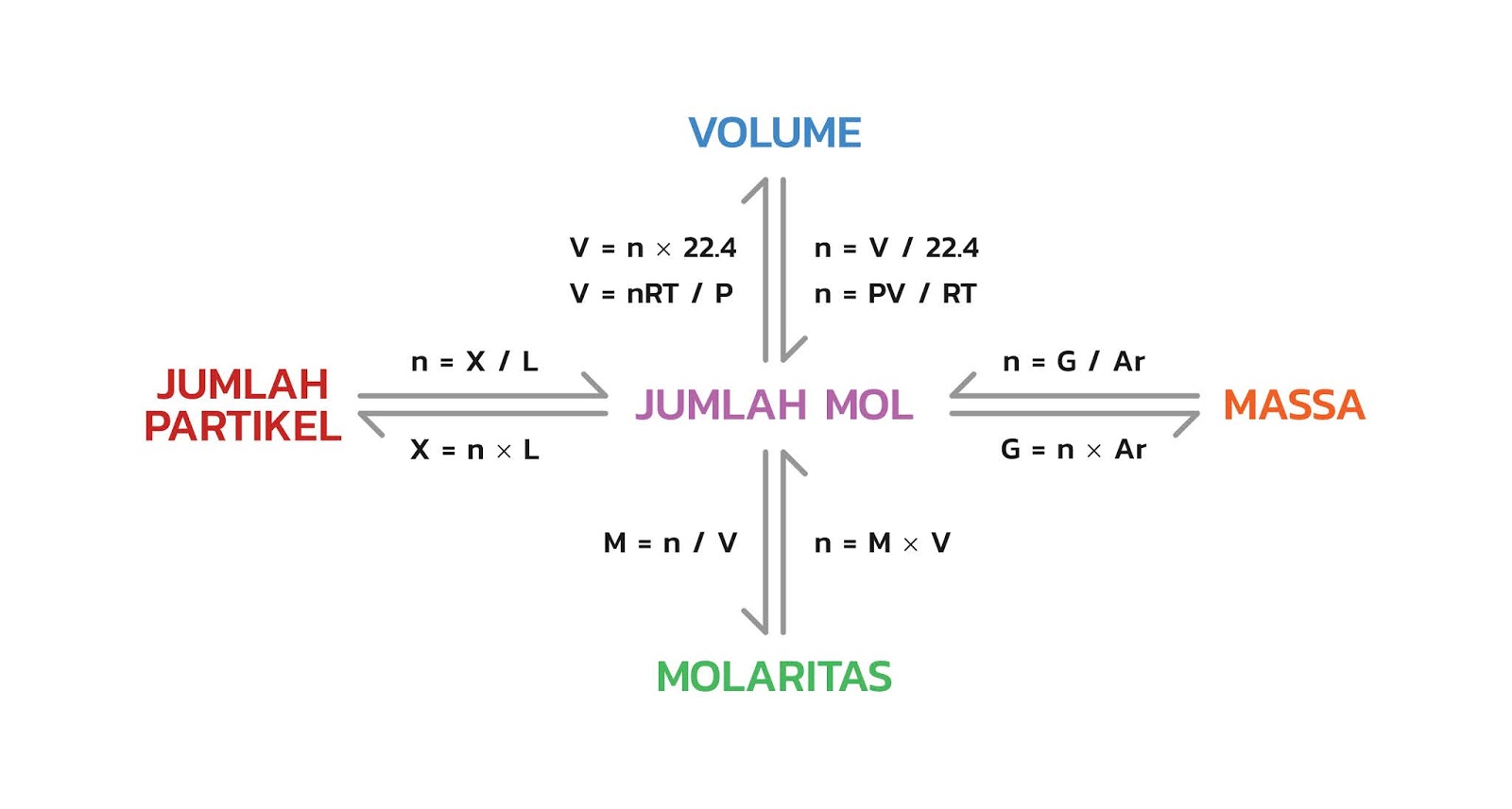
Hubungan Mol Dengan Jumlah Partikel Massa Volume Dan Molaritas Riset
In chemistry, a mole is a unit of measurement that is used to express the amount of a substance. The mole is defined as the amount of a substance that contains the same number of particles (atoms, molecules, or ions) as there are in 12 grams of carbon-12.