
Mengenal Pengertian Konsentrasi Larutan dan Satuansatuannya Gramedia Literasi
Nah, itulah beberapa satuan dan rumus konsentrasi larutan yang biasa digunakan untuk menghitung jumlah atau nilai dari konsentrasi suatu zat terlarut dalam sebuah larutan. Eh guys , ternyata ada alat ukur untuk membantu mengetahui jumlah kadar zat terlarut dalam sebuah larutan, lho.
Contoh Soal Konsentrasi Larutan Dan Pembahasannya
Digunakan untuk mendapatkan konsentrasi larutan secara kuantitatif. Molaritas dinyatakan sebagai jumlah mol Solut dalam larutan dibagi dengan volume larutan. Molaritas menyatakan banyaknya mol Solut yang terdapat dalam 1 liter larutan. Rumus: M = massa zatMR x 1000volume. Massa zat = M x Mr x volume1000. Volume = massa zat x 1000M x Mr.

Cara Menghitung Konsentrasi Larutan Dalam Persen
Cara Menghitung Molalitas Larutan. Molalitas digunakan untuk menyatakan konsentrasi larutan ketika Anda melakukan eksperimen yang melibatkan perubahan suhu atau bekerja dengan sifat koligatif.Perhatikan bahwa dengan larutan berair pada suhu kamar, kerapatan air kira-kira 1 kg/L, sehingga M dan m hampir sama.

Perhitungan Konsentrasi Larutan Baku dan Larutan Uji yang Dibuat pada Prosedur GC YouTube
Adapun rumus konsentrasi larutan, yaitu C = m/V. Dalam rumus tersebut, C adalah konsentrasi, m adalah massa dari zat terlarut, dan V adalah total dari volume larutan. Satuan Konsentrasi Larutan. Di bawah ini akan dijelaskan lebih lanjut tentang konsentrasi larutan beserta dengan cara menghitung konsentrasi larutan. 1. Molaritas (M)

Kumpulan Soal Konsentrasi Larutan
Rumus standarnya adalah C = m/V, yaitu C adalah konsentrasi, m adalah massa zat terlarut, dan V adalah total volume larutan. Kalau larutan Anda berkonsentrasi kecil, carilah jawabannya dalam bagian per juta (bpj) supaya lebih mudah dipahami. Saat di laboratorium, Anda bisa diminta mencari molaritas atau konsentrasi molar larutan terkait.

Contoh Soal Menghitung Konsentrasi Larutan
Keterangan : p = Massa pelarut. MOLALITAS LARUTAN CAMPURAN. Untuk menghitung molalitas dari larutan campuran dapat menggunakan rumus kimia sebagai berikut: Keterangan : m = molalitas larutan. g1 = massa zat terlarut 1 (gram) g2 = massa zat terlarut 2 (gram) Mr1 = Massa relative zat terlarut 1.

Cara Menghitung Konsentrasi Larutan Dalam Persen
Konsentrasi NaOH = (0,1 M x 25 ml x 0,4) / 50 ml = 0,02 M. Dengan mengetahui konsentrasi NaOH, kita dapat menghitung kadar asam klorida dalam larutan tersebut: Kadar asam klorida = (2,5 mmol x 0,1 M) / 100 ml = 0,0025 M atau 2,5 mM. Kesimpulan. Dalam artikel ini, kita telah mempelajari tentang rumus kadar titrasi, sebuah cara mudah untuk.

Cara Perhitungan Konsentrasi Larutan Konsentasi dalam a Persen Berat (W/W) gram zat
Masukkan nilai Anda ke dalam rumus C 1 V 1 = C 2 V 2. Dalam rumus ini, C 1 adalah konsentrasi awal larutan, V 1 adalah volume larutan awal, C 2 adalah konsentrasi akhir larutan, dan V 2 adalah volume larutan akhir. Memasukkan nilai-nilai yang sudah diketahui ke dalam persamaan ini akan membantu Anda mencari nilai yang belum diketahui dengan sedikit kesulitan.

(Larutan) Contoh Soal b konsentrasi larutan 1 YouTube
Dalam kimia, menghitung konsentrasi larutan dalam persen atau lebih singkatnya penentuan kadar campuran sangatlah penting. Karena konsentrasi larutan sangat mempengaruhi dalam reaksi kimia yang terjadi. Menghitung konsentrasi larutan dalam persen (kadar) dapat dapat dilakukan dengan 4 cara: 1. Persen Massa (% Massa : Massa) Keterangan; % = kadar zat (%) grt = massa zat terlarut

Cara Menghitung Konsentrasi Larutan Dalam Persen
Jika dua jenis larutan dengan konsentrasi berbeda dicampurkan, maka akan terbentuk larutan baru dengan konsentrasi tertentu. Konsentrasi larutan setelah dicampur dirumuskan sebagai berikut. Bagaimana Quipperian, cukup banyak ya rumus yang harus kamu hafalkan. Akan tetapi, Quipperian tidak perlu khawatir. Rumus-rumus di atas bisa dengan mudah.

Cara Menghitung Konsentrasi Larutan Dalam Persen
V 1 = volume larutan pekat (L). M 1 = konsentrasi larutan pekat (M). V 2 = volume larutan encer (L). M 2 = konsentrasi larutan encer (M). x = banyak pelarut yang ditambahkan (L) Dengan catatan, V2=V1+x. Kalau sudah ketemu perhitungan yang tepat, elo hanya perlu menuangkan jumlah pelarut yang dibutuhkan ke dalam zat yang akan dilarutkan atau diencerkan.

Cara Menghitung Konsentrasi Larutan Dalam Persen
Video ini berisi penjelasan dan contoh-contoh soal konsentrasi larutan yang meliputi molaritas, molalitas dan fraksi molOpen private class/kelompok belajar k.
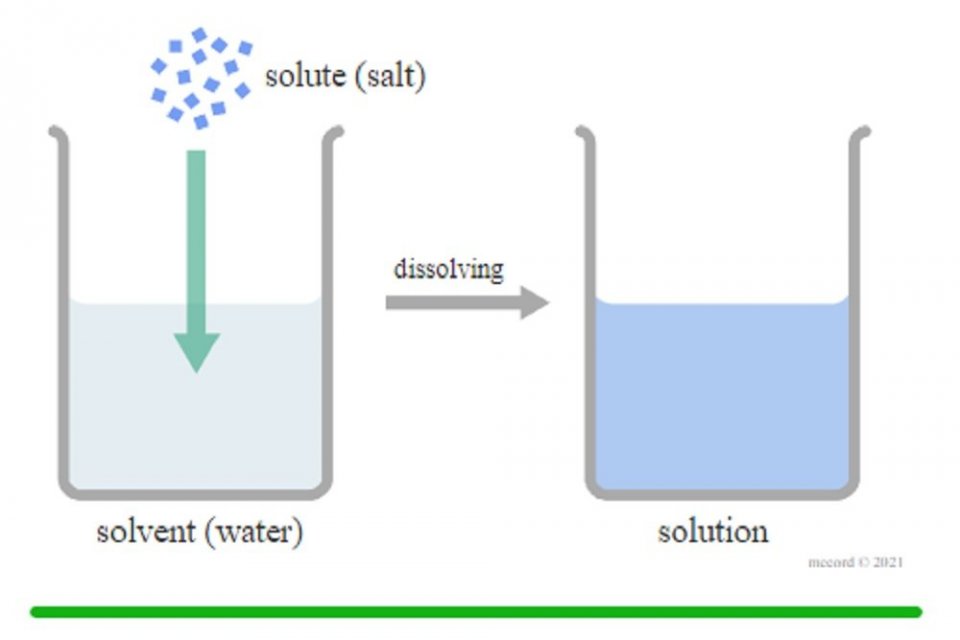
Memahami Rumus Konsentrasi Larutan dan Jenis Satuan Nasional Katadata.co.id
Rumus Konsentrasi Larutan-Materi pembelajaran ini ialah materi mata pelajaran kimia untuk siswa/siswi kelas X, mereka juga pastinya merasa awam untuk setiap materi pembelajaran yang baru. Nah pada kali ini saya akan berbagi ilmu mengenai konsentrasi larutan. Dalam ilmu kimia, larutan merupakan campuran homogen dari dua zat-zat terlarut dan zat terlarut yang berfungsi untuk melarutkannya.
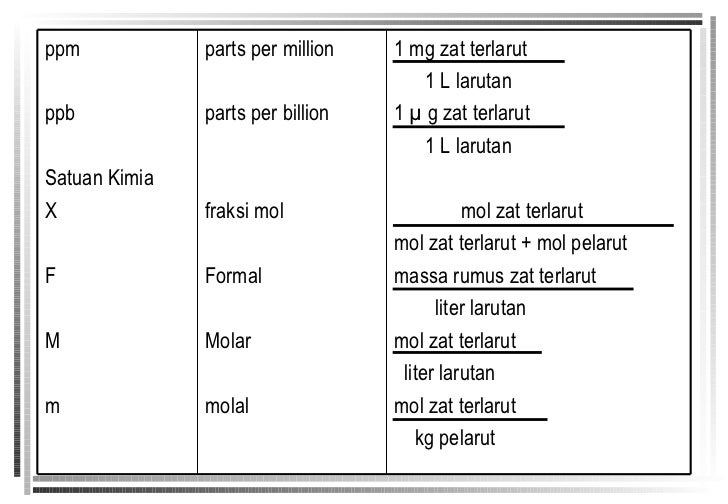
Rumus Konsentrasi Larutan Kimia
Konsentrasi larutan adalah jumlah zat yang terlarut dalam setiap satuan larutan atau pelarut. Secara sederhana, konsentrasi larutan dapat memberikan. 1000 mL larutan Rumus Molaritas (M) M= mol L →M= massa zat Mr × 1000 Volume Dari rumus diatas, didapatkan rumus-rumus sebagai berikut Massa zat= M ×Mr ×Volume 1000

Cara Menghitung Konsentrasi Larutan Dalam Persen
Demikian penjelasan mengenai konsentrasi larutan, rumus, cara menghitung, hingga cara membuat sebuah konsentrasi dari larutan. Solar Industri menyediakan produk dan jasa di bidang bahan bakar minyak. Solar Industri menyediakan berbagai layanan bahan bakar minyak, salah satunya adalah pembelian Bio Solar B30 untuk industri.

PERTEMUAN8 MEMBUAT LARUTAN DENGAN KONSENTRASI TERTENTU YouTube
Soal dan Jawaban Konsentrasi Larutan: Molaritas, Molalitas, Fraksi Mol, Persen Berat, Normalitas. 1. Konversi molal ke % massa. Contoh soal: Hitunglah % massa dari larutan NaI 0,2 molal (massa molar NaI = 150 g/mol) Penyelesaian: Arti 0,2 molal NaI adalah 0,2 mol NaI dalam 1 Kg pelarut air. massa NaI sebanyak 0,2 mol = 0,2 mol x 150 g/mol = 30.