
27+ Contoh Soal Hidrolisis Asam Lemah Basa Lemah Contoh Soal Terbaru
Rumus PH asam kuat yaitu: PH = -log (n x a) Contoh soal: Tentukan PH dari larutan H2SO4 0,01 M! Jawaban. Contoh soal menghitung PH. Dok: istimewa. Reaksi ionisasinya merupakan reaksi reversibel. Berikut rumus PH basa lemah: POH = - log (a x α ) dan PH = 14 - POH. Contoh soal: Tentukan PH larutan LOH 0,1 M dengan derajat ionisasi (α) 0,01.

20+ Contoh Soal Hidrolisis Asam Lemah Dan Basa Kuat Contoh Soal Terbaru
Video ini adalah lanjutan dari materi larutan asam dan basa. Materi kimia kelas 11. Di video ini dibahas mengenai cara menentukan pH dari campuran asam, camp.

Mengenal Rumus Ph Beserta Contoh Soal Dan Cara Menghitungnya Kumparan Unamed
Rumus Mencari PH Asam. Untuk menghitung atau rumus mencari pH asam suatu larutan, Anda dapat menggunakan rumus berikut: pH = -log[H+]. Adapun rumus untuk asam lemah biasanya ditulis sebagai berikut: HA + H2O ⇌ H3O+ + A-Dimana HA mewakili asam lemah, H2O mewakili air, H3O+ mewakili ion hidronium, dan A- mewakili basa konjugat dari asam.

Cara Menghitung pH Larutan Asam, Basa, Garam Beserta Contoh Soal dan Pembahasan Asymmetrical Life
3. Jika larutan garam terbentuk dari asam lemah dan basa kuat, maka larutan mengalami hidrolisis parsial (sebagian). Larutan tersebut bersifat basa dengan nilai pH lebih dari 7 (pH>7). Rumus yang digunakan untuk menentukan konsentrasi ion OH- adalah sebagai berikut. 4. Jika larutan garam terbentuk dari asam lemah dan basa lemah, maka larutan.

Konsep Mudah Belajar Menentukan pH Asam Lemah Kimia SMA YouTube
pH = 14 - (-log OH- ) pH 14 + log. pH = 14 + log 0,43. pH = 13,63. Jadi, pH larutan dalam cairan campuran tersebut adalah 13,63. Cara menghitung pH larutan bisa dilakukan dengan mengaplikasikan berbagai rumus. Tergantung pada larutan apa yang diukur pHnya dan apa yang ditanyakan. Apakah itu larutan asam kuat, asam lemah, basa kuat, basa lemah.

Mengenal Rumus Ph Beserta Contoh Soal Dan Cara Menghitungnya Kumparan Unamed
Hubungan antara pH dan pOH adalah : pH + pOH = pKw. dimana Kw adalah konstanta disosiasi air (menghasilkan H + dan OH −) yang bernilai 10 − 14, sehingga persamaan di atas menjadi. pH + pOH = 14. Suatu larutan akan bersifat asam bila jumlah H + lebih besar dari jumlah OH −, sehingga pada kondisi netral, pH = pOH = 7.

Cara Menghitung Ph Asam Lemah Satu Manfaat
Perbedaaan jenis tentu akan mempengaruhi rumus yang akan dipakai. Untuk menghitung ph larutan penyangga asam, kamu bisa menggunakan rumus yang terdiri dari ketetapan ionisasi asam lemah (Ka), jumlah mol asam lemah (a), dan jumlah mol basa konjugasi (g). Untuk menghitung ph larutan penyangga basa, kamu bisa gunakan rumus yang terdiri dari.

Rumus ph asam lemah beserta penjelasannya Universityku
Rumus dan Definisi untuk Konstanta pH dan Kesetimbangan. pH dan pOH berhubungan, seperti halnya Ka, pKa, Kb, dan pKb.. Nilai Ka yang kecil berarti sedikit asam yang terdisosiasi, jadi Anda memiliki asam lemah. Nilai Ka untuk kebanyakan asam lemah berkisar antara 10 -2 sampai 10 -14. pKa memberikan informasi yang sama, hanya dengan cara yang.

Cara Menghitung PH Larutan Asam Kuat Dan Asam Lemah Panduan Kimia + Riset
pH dan pOH asam kuat dan basa kuat bisa dihitung dengan menggunakan rumus pH dan pOH. Asam terbagi atas 2, yaitu asam kuat dan lemah. Dalam perhitungannya re.
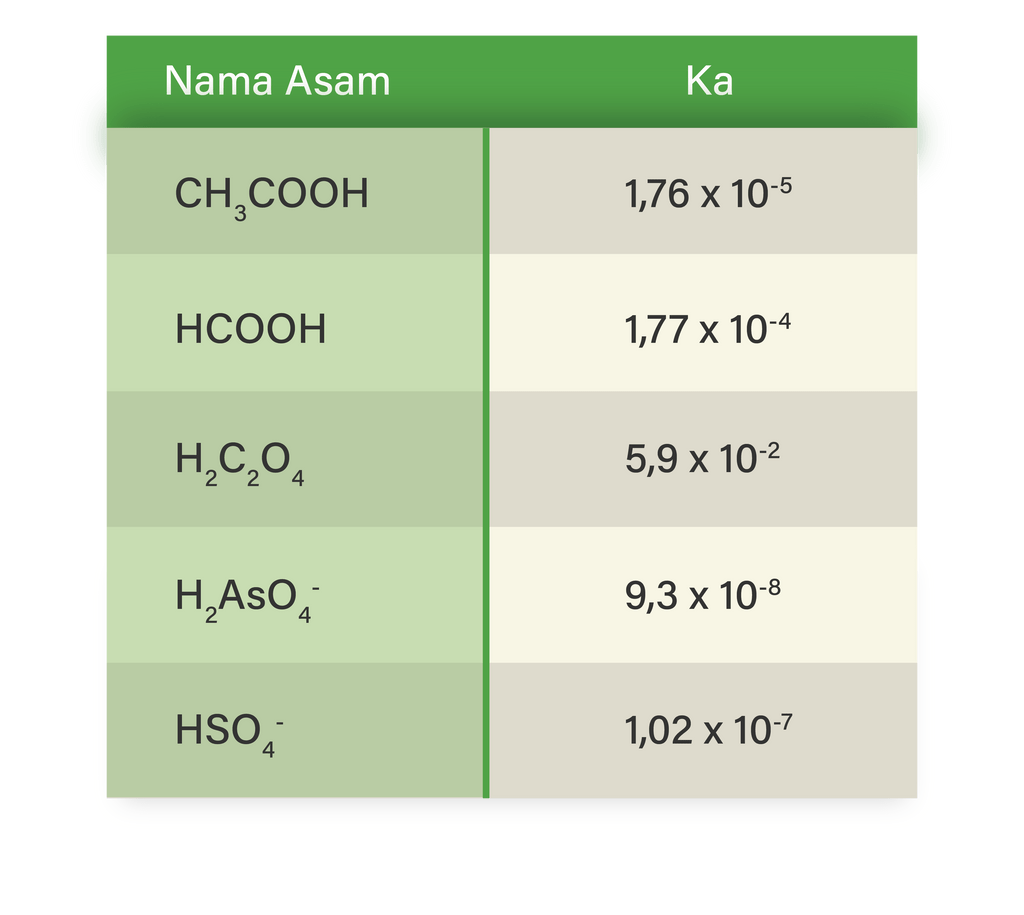
Diketahui nilai K a dari beberapa asam lemah ada...
Materi ini bertujuan untuk menghitung pH Asam Lemah dan Basa Lemah. Dengan trik Asyik dan pemahaman yang kuat maka materi ini jadi lebih mudah untuk di menge.

27+ Contoh Soal Hidrolisis Asam Lemah Basa Lemah Contoh Soal Terbaru
Pengertian Titrasi Asam Basa. Titrasi adalah prosedur menetapkan kadar suatu larutan dengan mereaksikan sejumlah larutan tersebut yang volumenya terukur dengan suatu larutan lain yang telah diketahui kadarnya (larutan standar) secara bertahap. Berdasarkan jenis reaksi yang terjadi, titrasi dibedakan menjadi titrasi asam basa, titrasi.

Perhitungan pH Garam dari Asam lemah dan Basa Lemah
Tingkat keasaman/pH larutan asam basa tergantung pada molaritas ion H+ dalam larutan. Jika molaritas ion H+ semakin besar, maka semakin asam larutan itu. 1. Rumus pH Nilai pH larutan asam basa diperoleh sebagai hasil negatif logaritma 10 dari molaritas ion H+. Secara matematis dapat dituliskan: pH = -log [H+] Keterangan: pH = derajat keasaman [H+]

PERHITUNGAN pH ASAM LEMAH DAN BASA LEMAH YouTube
Untuk menghitung pH dari asam lemah dapat digunakan rumus berikut : dimana [H +] dihitung dalam Molaritas. Contoh Soal Menghitung pH Dan pOH dari Asam Lemah dan Basa Lemah + Pembahasan . 1. Tentukan pH dari 555 ml Asam Etanoat 0,2 M dengan Ka = 1,8 x 10-5! 2. Jika diketahui suatu asam lemah berpH 5,5 dengan Ka = 2 x 10-5,.

Mengenal Rumus Ph Beserta Contoh Soal Dan Cara Menghitungnya Kumparan Unamed
PH = - Log [H+] Contoh Soal : 1. Hitunglah PH dari larutan asam lemah HClO 0,1 M ! ( Dik Ka = 3,5 x 10>-8 ) Asam Hipoklorit merupakan asam lemah yang hanya dapat terionisasi sebagian membentuk ion-ion , berikut ini reaksi ionisasinya : HClO >> H+ + ClO-. 0,1 M x x. Pertama kita cari konsentrasi ion H+ nya :

Cara Menghitung pH Garam dari Asam Kuat dan Basa Lemah Materi hidrolisis garam Kimia SMA Kelas
2. Hitung pH Asam Lemah. Setelah mendapatkan konsentrasi ion H+, kita dapat menentukan pH asam lemah dengan menggunakan rumus: pH = -log [H+] Dengan memasukkan nilai [H+] yang sudah diperoleh, maka: pH = -log (0,001341) = 2,87; Jadi pH larutan CH3COOH 0,1 M adalah 2,87. Semakin kecil nilai pH, semakin asam larutan tersebut. Contoh Soal.

35+ Contoh Soal Asam Basa Lemah Rochelle Proctor
Oleh karena itu, larutan garam dari asam lemah dan basa kuat akan meningkatkan konsentrasi OH − dalam air sehingga larutannya bersifat basa (pH > 7).. Garam dari asam lemah dan basa lemah. Garam seperti CH 3 COONH 4 yang dapat terbentuk dari reaksi asam lemah (CH 3 COOH) dan basa lemah (NH 3) akan mengalami hidrolisis kation dan anionnya. pH larutan garam demikian bergantung pada kekuatan.