
Cara menghitung massa benda dan massa jenis benda dengan menggunakan Hukum Archimedes YouTube
Jadi untuk molekul CO 2 memiliki massa relatif sebesar 44 gram/mol. Rumus Perhitungan Konsep Mol.. rumus kimia ini dapat berupa jenis atom atau rumus senyawanya.. Semoga melalui artikel ini dapat memberikan wawasan serta refrensi kepada segenap pembaca yang mencari literasi terkait kimia. Sebarkan ini: Posting terkait: Pengertian.

Rumus Kimia Urea Dan Mr Bit CDN
Karena dalam soal sudah memakai s.m.a, Jadi kalian tinggal masukin aja deh massa atom C-12 dengan satuan s.m.a. Nah, akhirnya dapet deh jawabannya sebesar 35 s.m.a, tapi biasanya dalam soal kalian akan disuguhkan dalam satuan metrik seperti kilogram atau gram, sehingga kalian harus menghitungnya dengan teliti dan cermat!

Relative Atomic Mass, Here's an explanation, formula, and how to calculate it World Today News
Sebelum mencari rumus molekul senyawa tersebut, tentukan dahulu massa molekul relatifnya (Mr)!. Jadi, rumus molekul senyawa tersebut adalah C 5 H 10 O 5. Melengkapi Persamaan Reaksi Kimia. Reaksi kimia merupakan reaksi yang berlangsung secara spontan. Jika suatu senyawa yang mengandung ion negatif direaksikan dengan senyawa lain yang.

Menghitung Mr Glukosa Massa Molekul Relatif C6H12O6 Kimia SMA YouTube
Massa 1,5 mol C = 1,5 mol × 12 g mol-1 = 18 g. 3. Ar Fe = 56 sma, Jadi, massa molar Fe = 56 g mol-1. m = 9,3 × 1023 g. 4. Massa molar CO2 = 44 g mol-1. Jumlah molekul CO2 = 0,54× 1023 molekul. Demikianlah artikel tentang pengertian dan rumus massa molar (Mm), beserta contoh soal dan pembahasannya lengkap.
5 Tahapan Reaksi Kimia kabarmedia.github.io
Kadar massa dalam suatu zat dapat dinyatakan dalam fraksi massa: Dalam penghitungan rumus massa benda atau juga rumus volume benda dalam perhitungan kimia, kadar massa dalam suatu zat dapat dinyatakan dalam fraksi massa $\frac{Ar\times z}{Mr}$

Contoh Soal Nomor Atom Dan Nomor Massa Homecare24
Pengertian rumus molekul adalah rumus yang menyatakan jumlah atom dari unsur-unsur dalam senyawa. Rumus Empiris. Untuk mendapatkan rumus empiris (RE) atau empirical formula, dapat digunakan perhitungan dalam mol unsur menghasilkan perbandingan jumlah atom dalam molekul. Langkah-langkah menentukan rumus empiris suatu senyawa, sebagai berikut:
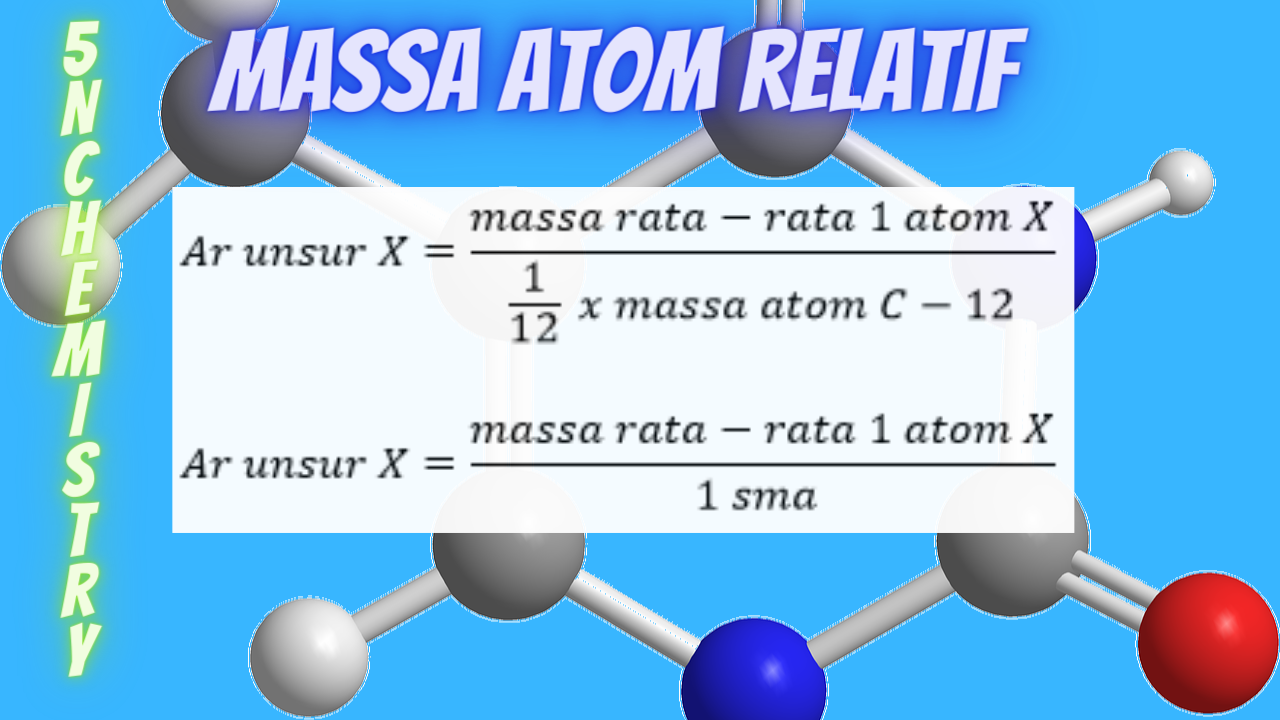
Cara Menentukan Massa Atom Relatif (Ar) Unsur 5NChemistry
Lalu, setelah mengetahui massa atom rata-rata dari unsur klorin, selanjutnya kita hitung massa atom relatifnya menggunakan rumus Ar seperti berikut. Jadi, massa atom relatif atau Ar dari klorin tersebut adalah sebesar 0,355. Eits ingat, menulisnya tanpa satuan ya, karena seperti tadi sudah kita bahas, massa atom relatif tidak mempunyai satuan.
11+ Soal Hukum Dasar Kimia Kelas 10 Pdf Contoh Soal dan Jawaban
Saat diminta untuk mencari "persen massa", Anda harus mencari massa zat kimia tertentu (yang ditanyakan dalam soal) dalam bentuk persentase dibandingkan massa total seluruh penyusunnya.. Carilah bobot atom setiap unsur dalam rumus kimia di tabel periodik. Massa unsur biasanya dapat ditemukan di bawah simbol kimianya. Tuliskan massa setiap.

Reaksi Asam Basa Rumus Kimia Contoh Soal Dan Jawaban Riset
Contoh Soal Konsep Mol Beserta Jawabannya. 1. Sebanyak 4,9 gram H2SO4 H 2 SO 4 dilarutkan dalam air sehingga diperoleh 500 mL larutan. Tentukan jumlah ion yang yang terlarut dalam larutan dan tentukan konsentrasi ion H+ H +. Jawaban contoh soal konsep mol dan penyelesaiannya. nH2SO4 = m Mr = 4, 9 98 = 0, 05 mol n H 2 SO 4 = m M r = 4, 9 98 = 0.
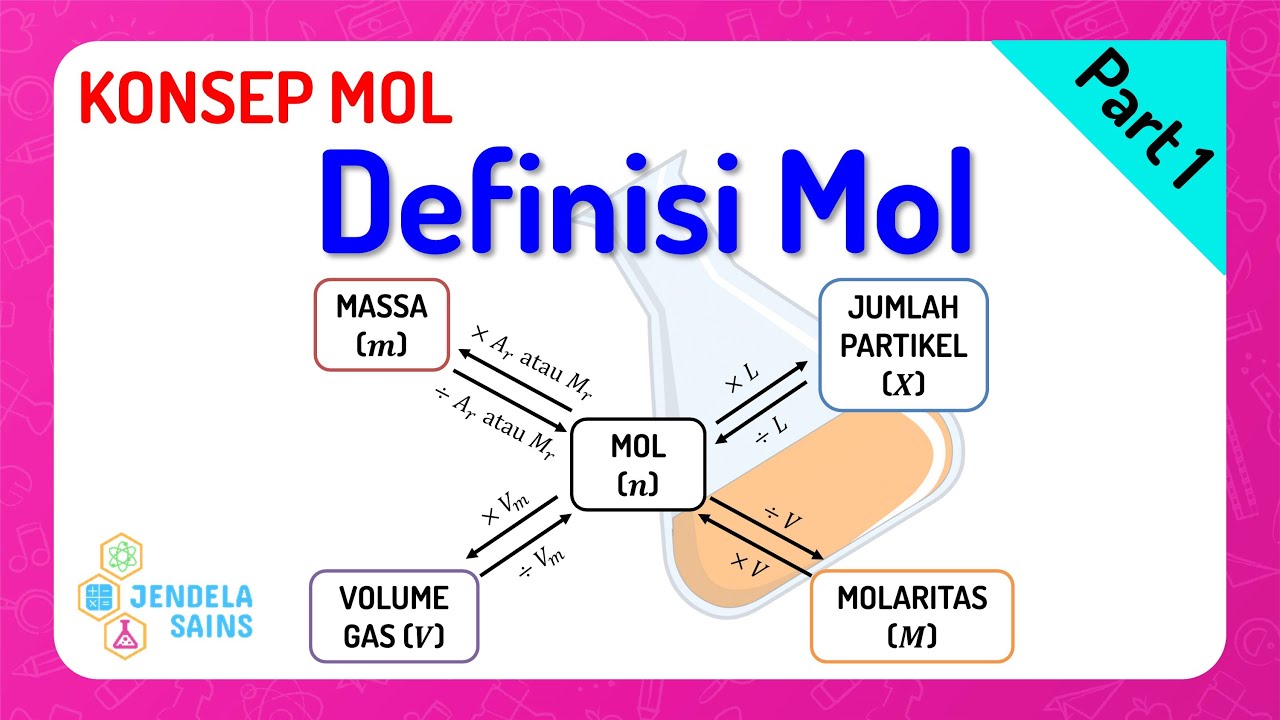
Konsep Mol Kimia Kelas 10 • Part 1 Hubungan Mol & Massa, Jumlah Partikel, Volume Gas, Molaritas
Contoh Soal 1. Suatu material X memiliki bentuk kubus dengan sisi-sisinya 4 m. Material tersebut kemudian ditimbang dengan neraca sebesar 2 kg. Hitunglah massa jenis atau densitas massa benda X! Jawab: massa = 2 kg. volume kubus = s x s x s = 4 x 4 x 4 = 64 m3. ρ = m / v = 2 / 64 = 0,031 kg/m3. Jadi, ρ dari material tersebut adalah 0,031 kg/m3.

Cara Menentukan Massa Jenis Zat
Baca Juga: Pengertian dan Rumus Larutan Penyangga - Materi Kimia Kelas 11. Persamaan Kimia Reaksi Pengendapan. Seperti apa sih persamaan kimia dari reaksi pengendapan? Reaksinya seperti ini:. Pertama, elo bisa mencari massa dari masing-masing larutan: n Pb(NO 3) 2 = 10-3 x 0,5 = 5×10-4 M;

Hitunglah Kemolalan Larutan Cuka Yang Mengandung 24 Massa Ch3cooh Belajar di Rumah
Dari definisi massa molekul relatif ini, sebenarnya sudah bisa diketahui rumusnya, yaitu: Mr molekul AxBy = (x. Ar A) + (y. Ar B) + dst. Selain itu, massa molekul relatif juga dapat ditentukan dengan rumus: Mr molekul atau zat X =. massa rata-rata satu molekul atau zat X. 1/12 x massa atom isotop C-12.

Cara Mencari Massa Jenis Zat Cair dan Contoh Soalnya
Persentase Massa Unsur. Senyawa kimia identik dengan rumus-rumus kimia yang dinyatakan dengan unsur-unsur tertentu, contohnya air (H 2 O), oksigen (O 2), dan glukosa (C 6 H 12 O 6). Setiap unsur penyusun tersebut memiliki massa berbeda-beda. Untuk menghitung persentase massa unsur, gunakan persamaan berikut. Untuk lebih jelasnya, perhatikan.

Cara Mencari Mr Kimia Homecare24
H = 1,00794 N = 14.0067. Selanjutnya, kalikan massa atom setiap atom dengan jumlah atom dalam senyawa. Ada satu atom nitrogen (tidak ada subskrip yang diberikan untuk satu atom). Ada tiga atom hidrogen, seperti yang ditunjukkan oleh subscript. massa molekul = (1 x 14,0067) + (3 x 1,00794) massa molekul = 14,0067 + 3,02382 massa molekul = 17,0305.

Menghitung Jumlah mol jika diketahui Massa Molar Zat dan Massa Molekul Relatif YouTube
Penggunaan Normalitas dalam Analisis Kimia.. atau zat pelarut. Jika massa atau berat ekuivalen (gram) belum diketahui, kamu dapat mencarinya dengan menggunakan rumus: Massa ekuivalen (gram) =Mrn.. maka gunakan rumus berikut untuk mencari normalitasnya: N = molaritas x ekuivalen. N = 0,1 x 2.
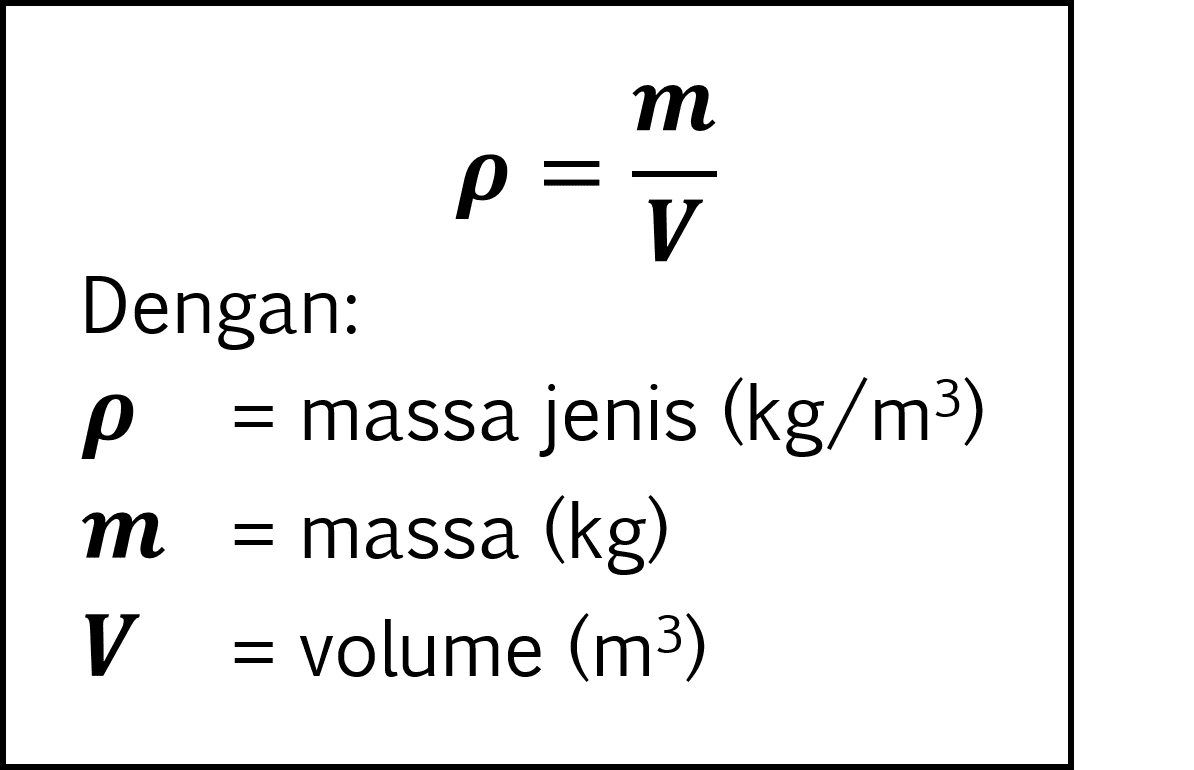
Fisika Rumus Fluida Statis (Hidrostatika) RUMUS MATEMATIKA FISIKA
2. Hitunglah jumlah mol dari 54 g Al dalam sebuah perabotan rumah tangga (Ar Al = 27) Jawaban: Jumlah mol = massa / massa molar = massa / Mr atau Ar. mol Al = 54 g Al / 27 g/mol = 2,0 mol. 3. Tentukan volume dari 4,4 g gas CO2 yang diukur pada tekanan 2 atm dan suhu 27 °C!