
Tuliskan Persamaan Ion dan RumusRumus Ksp nya, jika zatzat berikut dilarutkan ke dalam air
The solubility product constant is the equilibrium constant for the dissolution of a solid substance into an aqueous solution. It is denoted by the symbol Ksp. The solubility product is a kind of equilibrium constant and its value depends on temperature. Ksp usually increases with an increase in temperature due to increased solubility.

Cara Menentukan Rumus Ksp Suatu Senyawa Shorts Kimia Kelarutan Ksp Contohsoalkimia
The equilibrium constant for a dissolution reaction, called the solubility product ( Ksp ), is a measure of the solubility of a compound. Whereas solubility is usually expressed in terms of mass of solute per 100 mL of solvent, Ksp is defined in terms of the molar concentrations of the component ions. In contrast, the ion product ( Q) describes.

Materi Kelarutan Dan Hasil Kali Kelarutan Homecare24
Di artikel kali ini, Quipperian akan diajak untuk mempelajari kelarutan suatu senyawa, mulai dari senyawa larut sampai terjadinya endapan. Daftar Isi Sembunyikan. Kelarutan Garam. Pengertian Kelarutan (s) Tetapan Hasil Kali Kelarutan (Ksp) Hubungan antara Kelarutan dan Tetapan Hasil Kelarutan. Contoh soal 1. Pengaruh Ion Senama pada Kelarutan.

Soal Tentukan rumus Ksp dari CuCl!
Table of Contents. The equilibrium constant for a solid substance dissolving in an aqueous solution is the Ksp. The level at which a solute can be dissolved in the solution is represented by Ksp. The higher the Ksp value of a substance, the more it is soluble. Consider the general dissolution reaction in the solution.
Tuliskanlah rumus kelarutan(Ksp) dari senyawa beri...
It is meaningless to compare the solubilities of two salts having different formulas on the basis of their Ks values. Example 17.2.2 17.2. 2. The solubility of CaF 2 (molar mass 78.1) at 18°C is reported to be 1.6 mg per 100 mL of water. Calculate the value of Ks under these conditions.

Menentukan rumus Ksp Senyawa liangl leskimia shorts ksp utbk sbmptn utbkkimia kimia
First, write out the Ksp expression, then substitute in concentrations and solve for Ksp: CaF 2 ( s) ↽ − − ⇀ Ca 2 + ( aq) + 2 F − ( aq) A saturated solution is a solution at equilibrium with the solid. Thus: K sp = [ Ca 2 +] [ F −] 2 = ( 2.1 × 10 − 4) ( 4.2 × 10 − 4) 2 = 3.7 × 10 − 11. As with other equilibrium constants.

Kelarutan dan ksp soal kimia SMA YouTube
Hai sobat trivia,Di video kali ini berisi penjelasan Bab Hasil Kali Kelarutan mengenai konsep kelarutan dan rumus Ksp. Penjelasan materi di video ini juga di.

Hasil Kali Kelarutan Ksp
Contoh Soal Kelarutan dan Hasil Kali Kelarutan (KSP) dan Pembahasan Contoh Soal 1: Hitunglah kelarutan Cu(OH) 2 dalam satuan g/L, jika diketahui K sp Cu(OH) 2 = 2,2 × 10 −20. Pembahasan: Contoh Soal 2: Hitunglah kelarutan molar PbI 2 dalam larutan KI 0,1 M. (K sp PbI 2 = 7,1 × 10 −9) Pembahasan: Dalam larutan, KI akan terdisosiasi menjadi.

Menentukan nilai kelarutan dari Ksp Kelarutan 2 YouTube
Here's an example: The K s p value of A g 2 S O 4 ,silver sulfate, is 1.4× 10 - 5. Determine the molar solubility. First, we need to write out the dissociation equation: K s p = [ A g +] 2 [ S O 4 2] Next, we plug in the K s p value to create an algebraic expression. 1.4× 10 - 5 = ( 2 x) 2 ( x) 1.4× 10 - 5 = 4 x 3.

How To Calculate The Ksp
Practice Questions (please show all work) 1. Given the Ksp for Fe F2 is 2.36 x 10^(-6), find the solubility of the Fe and F2 ions in mols/L or molarity (M).

Kelarutan (s) dan Hasil Kali Kelarutan (Ksp) Soal dan Pembahasan KIMIA KELAS 11 YouTube
Tuliskan rumus tetapan hasil kali kelarutan untuk senyawa Mg(OH) 2! Pembahasan: Mg(OH) 2 dalam larutan akan terurai menjadi ion-ionnya, Mg(OH) 2 ⇄ Mg 2 + + 2OH - Maka dari rumus Ksp diperoleh Ksp = [Mg 2+][OH -] 2. Contoh soal 3 : Pada suhu tertentu, kelarutan AgIO 3 adalah 2 × 10 -6 mol/L, tentukan harga tetapan hasil kali.

Soal Kimia tentang Kelarutan dan Hasil kelarutan serta Pembahasannya
Rumus Ksp merupakan konsep yang sangat penting dalam ilmu kimia, terutama dalam memahami kelarutan suatu senyawa ionik dalam pelarut. Dalam menghitung Ksp, kita perlu mengetahui konsentrasi ion-ion yang terlarut dalam larutan jenuh dan koefisien stoikiometri dari masing-masing ion dalam persamaan reaksi.

Rumus Tetapan Hasil Kali Kelarutan Ksp YouTube
K_(sp) is called solubility product constant, or simply solubility product. In general, the solubility product of a compound represents the product of molar concentrations of ions raised to the power of their respective stoichiometric coefficients in the equilibrium reaction. Here's an example to better demonstrate the concept. Let's consider the saturated solution of silver chloride (AgCl.

Rumus hasil kali kelarutan (KSP) Ag2CrO4 dinyatakan sebag...
Rumus Ksp dihitung dengan mengalikan konsentrasi ion-ion yang terlarut dalam suatu senyawa. Misalnya, jika kita memiliki senyawa AgCl yang terlarut dalam air, rumus Ksp-nya adalah [Ag+][Cl-]. Contoh Penghitungan Rumus Ksp. Mari kita ambil contoh senyawa BaSO4. Jika kita menambahkan BaSO4 ke dalam air, senyawa ini akan terurai menjadi ion-ion.
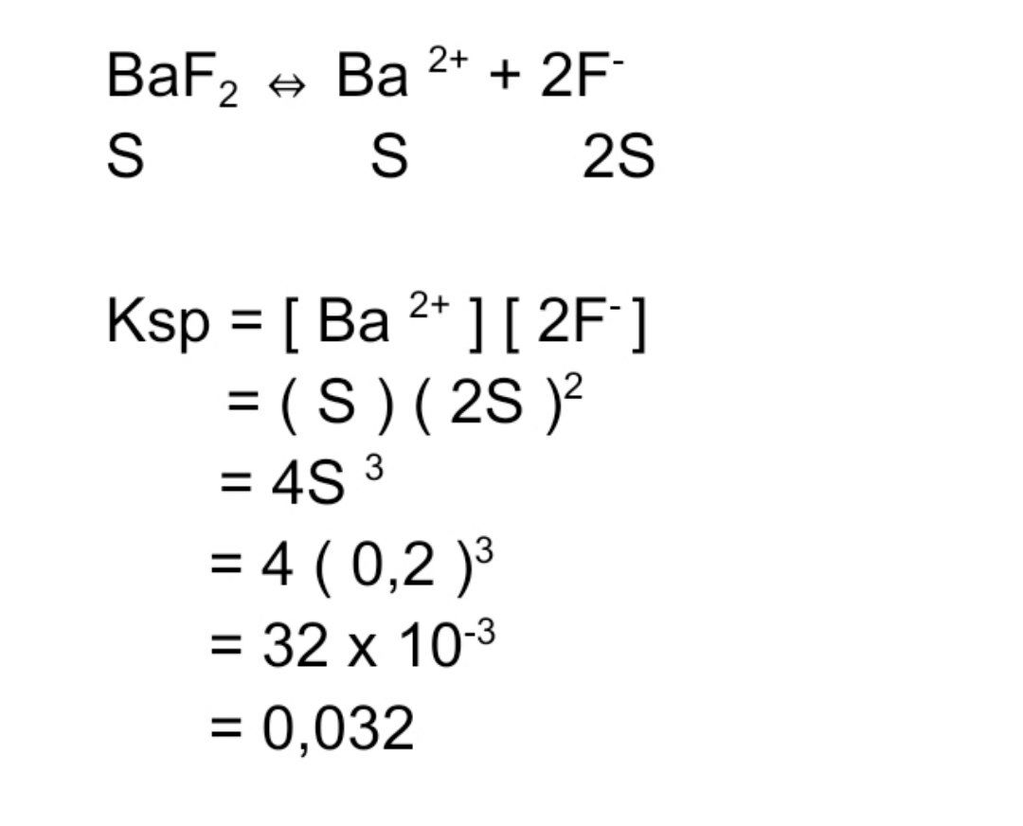
Tentukan besarnya Ksp senyawa berikut. 350 gram Ba...
The dissociation equation for PbF 2 and the corresponding K s p expression. PbF 2 ( s) ⇄ Pb 2 + ( a q) + 2 F − ( a q) K s p = [ Pb 2 +] [ F −] 2. The steps above will be followed to calculate the K s p for PbF 2. Step 2: Solve. molar solubility 0.533 g L × 1 mol 245.20 g = 2.17 × 10 − 3 M. The dissociation equation shows that for.

Cara Mentukan Rumus Ksp Kimia Bit CDN
Tetapan Hasil Kali Kelarutan (Ksp) - RumusKimia.net kali ini akan berbagi materi kimia tentang Rumus Tetapan Hasil Kali Kelarutan dan Contoh Soal Penyelesaian. Dalam suatu larutan jenuh dari suatu elektrolit yang sukar larut, terdapat kesetimbangan antara zat padat yang tidak larut dan ion-ion zat itu yang larut. MxAy (s) ⇄ x My+(aq) + y Ax.