
√ Materi Hukum Faraday Bunyi, Rumus, Contoh Soal
Jumlah mol elektron yang terlibat dalam reaksi elektrolisis dihitung dengan rumus: Q = n e × F. Setengah reaksi pembentukan H 2 pada elektrolisis larutan KBr: 2H 2 O(l) + 2e − → H 2 (g) + 2OH − (aq) Berdasarkan perbandingan koefisien reaksi, . Jadi, volum . volum . volum . Hukum Faraday: Sumber Referensi. Brown, Theodore L. et al. 2015.

Foto Hukum Faraday I dan II tentang Elektrolisis
Rumus hukum Faraday 2 atau Faraday's law of electromagnetic induction adalah rumus matematika yang menjelaskan hubungan antara perubahan medan magnet dengan arus listrik yang dihasilkan. Rumus ini merupakan pengembangan dari hukum Faraday yang pertama, yang mengatakan bahwa arus listrik akan dihasilkan oleh sebuah konduktor yang berada dalam.

Apa Bunyi Hukum Faraday 1 dan 2? Kimia Kelas 12
Jika rumus hukum Faraday 1 dan 2 ini digabungkan, maka akan diperoleh rumus baru, yaitu: G = k . i . t . ME. Keterangan: k = tetapan/faktor pembanding. Faraday menemukan bahwa harga faktor pembanding ini adalah 1/96.500, sehingga rumus di atas dapat dituliskan sebagai berikut. di mana : G = massa yang dihasilkan pada elektrolisis (gram) i.

La llei de Faraday (II/II) YouTube
Pengertian dan Bunyi hukum Faraday 1 dan 2☑️ Rumus (persamaan), Contoh Soal dan pembahasan hukum Faraday 1 dan 2 lengkap☑️ Seorang ilmuwan yang berasal dari Inggris bernama Michael Faraday menemukan sebuah hukum yang digunakan dalam ilmu kimia dinamakan Hukum Faraday. Hubungan antara penggunaan muatan listrik dan hasil massa zat dalam electrode dijelaskan melalui hukum ini.

Mengenal Bunyi Hukum Faraday Kimia Kelas 12
Rumus Hukum Faraday 2 dapat dinyatakan sebagai berikut: M = E * F * n. Dimana: M = massa zat yang terbentuk selama elektrolisis (gram) E = ekuivalen massa zat (gram/Coulomb) F = konstanta Faraday ≈ 96,485 Coulomb/mol (muatan per mol elektron) n = jumlah mol zat yang berpartisipasi dalam reaksi redoks.

PERHITUNGAN SEL ELEKTROLISIS (HUKUM FARADAY 2) YouTube
Rumus hukum Faraday II adalah W1 / W2 = e1 / e3, W1 adalah massa zat 1 (gram), W2 adalah massa zat 2 (gram), ei adalah ekuivalen zat 1 dan e2 adalah ekuivalen zat 2. Penjelasan ini menegaskan jika memang adanya penerapan hukum ini dipakai untuk memperhitungkan aspek kuantitatif zat-zat yang terlibat dalam reaksi di dalam sel elektrolisis.

Hukum Faraday 2 Elektrolisis Seri Kimia SMA Kelas 3 YouTube
Perbandingan ini menjadi persamaan dengan penambahan faktor 1/96.500, sehingga diperoleh rumus hukum faraday: w = 1/96.500 x I x t x ME. dengan, Contoh soal Hukum Faraday . Arus listrik 0,2 ampere dilewatkan selama 50 menit ke dalam sel elektrolisis yang mengandung larutan CuCl 2. Hitunglah endapan Cu yang terbentuk pada katode.

Pengertian Hukum Faraday Dilengkapi Bunyi Rumus Dan Contoh Soal Riset
Rumus Hukum Faraday 1 Dan 2. Dalam sebuah Hukum Faraday, secara matematis perhitungan arus listrik dapat dirumuskan menjadi: Rumus Hukum Faraday untuk menghitung suatu gaya gerak listrik maka, rumus yang digunakan secara sistematis ialah sebagai berikut: ɛ = -N (ΔΦ / ∆t) Keterangan: ɛ ialah gaya gerak listrik (ggl) induksi (volt)

Rumus Praktis Hukum Faraday Pojok Kimia
Michael Faraday, ia adalah seorang ilmuan asal Inggris yang lahir pada 22 September 1791 di Newington Butts, Inggris. Kemudian ia dijuluki sebagai "bapak listrik", berkat usahanya listrik bisa jadi teknologi yang memiliki banyak kegunaan. Michael Faraday menjadi seorang ahli kimia dan fisika berkat mempelajari aspek kuantitatif dan.

Pembahasan Soal Elektrolisis Hukum Faraday 1 dan 2 YouTube
Rumus Hukum Faraday 2 adalah rumus yang digunakan untuk menghitung kuantitas zat yang bereaksi atau diproduksi dalam suatu proses elektrokimia. Dengan mengetahui luas permukaan elektrode, waktu reaksi, arus listrik, dan koefisien elektrokimia suatu zat, rumus Hukum Faraday 2 dapat digunakan untuk menghitung jumlah zat yang terlibat dalam reaksi.

Hukum Faraday II Tanpa Menghafal Rumus YouTube
Adapun rumus hukum Faraday 1 dan 2 adalah sebagai berikut. Rumus Hukum Faraday 1. Ingat, bunyi hukum Faraday 1: "Massa zat yang dilepaskan selama elektrolisis berbanding lurus dengan jumlah listrik yang digunakan" Berdasarkan bunyinya, rumus hukum Faraday 1 dapat dituliskan sebagai berikut. G ≈ Q atau G ≈ it. Keterangan:

Rumus Hukum Faraday Bentuk turunan II YouTube
Sebelum kita membahas contoh soal hukum faraday 2, mari kita ingat kembali bunyi Hukum Faraday II "massa zat yang dihasilkan berbanding lurus dengan massa ekuivalennya untuk jumlah listrik yang sama." Selanjutnya mari kita simak contoh soal hukum faraday 2 dan pembahasannya berikut ini. Soal No. 1 Pada elektrolisis larutan NiSO4 selama 45 menit menghasilkan endapan
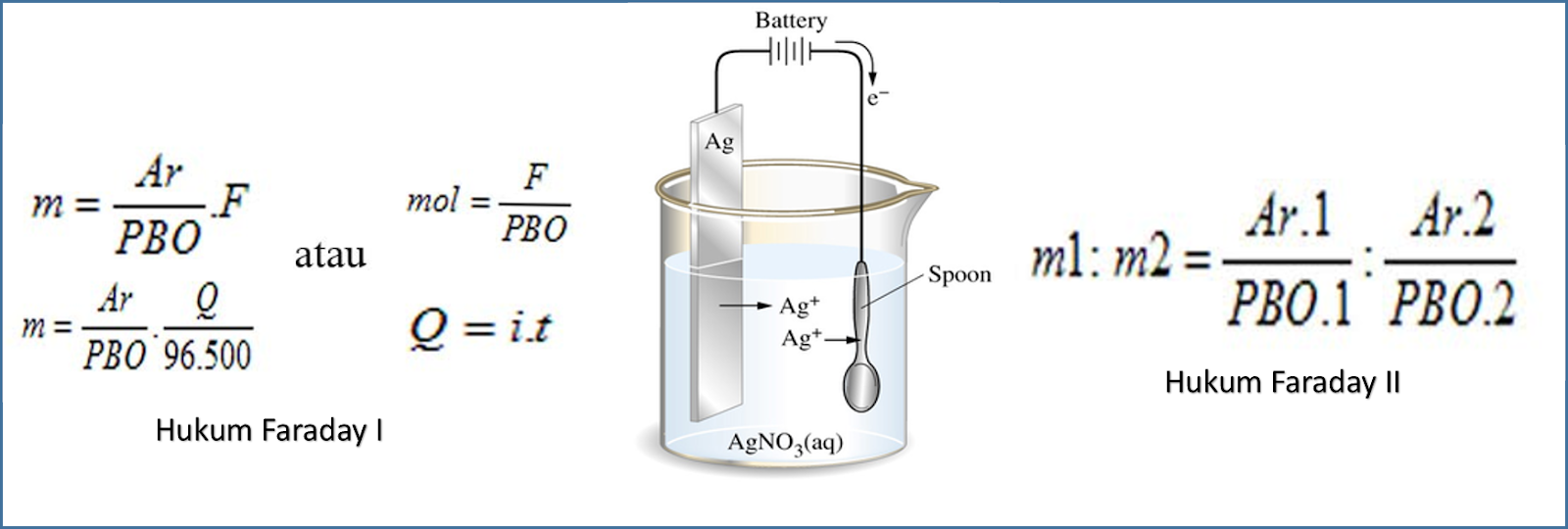
Hukum Faraday Pojok Kimia
Hukum Faraday: Bunyi, Rumus, & Contoh Soal. Oktober 2, 2023 Oleh Eka, S.Si. Hukum Faraday adalah ilmu yang mempelajari mengenai dasar elektromagnetisme yang merupakan proses perubahan kimia menghasilkan arus listrik maupun sebaliknya. Hukum ini dikemukakan oleh Michael Faraday, seorang ilmuwan asal Inggris yang bekerja dalam bidang elektrolisis.

Apa Bunyi Hukum Faraday 1 dan 2? Kimia Kelas 12
Bunyi Hukum Faraday 1 dan 2, Beserta Rumus Faraday. Bunyi Hukum Faraday - Pengertian Hukum Faraday adalah salah satu hukum yang menyatakan bahwa hubungan antara jumlah listrik yang dipakai dengan Massa Zat yang dihasilkan pada proses Elektrolisis baik di Katoda maupun Anoda, dan Teori Faraday ini sering disebut juga dengan Teori Kuantitatif.

PPT HUKUM INDUKSI FARADAY PowerPoint Presentation, free download ID5738336
Rumus hukum Faraday 2. W1 / W2 = e1 / e2. Keterangan: W1 adalah massa zat 1 (gram) W2 adalah massa zat 2 (gram) e1 adalah massa ekuivalen zat 1. e2 adalah massa ekuivalen zat 2. Dari penjelasan di atas, pada dasarnya hukum Faraday digunakan untuk memperhitungkan aspek kuantitatif zat-zat yang terlibat dalam reaksi dalam sel elektrolisis.

Soal Hukum Faraday LEMBAR EDU
Belajar Modul, Rumus, & Soal Elektrolisis dan kuis interaktif.. Terdapa 2 Hukum Faraday Kimia yakni hukum faraday 1 dan hukum faraday 2, lebih lanjut seperti berikut: 1. Hukum Faraday I "Massa zat yang terjadi atau melarut selama proses electrolysis berbanding lurus dengan jumlah muatan listrik yang melalui sel elektrolisis kimia.