
Cara Menghitung pH Larutan Asam, Basa, Garam Beserta Contoh Soal dan Pembahasan
Cara kedua ini harus menghasilkan sisa dari asam lemah atau basa lemah. Dari persamaan tersebut, CH 3 COOH (asam lemah) dan NH 3 (basa lemah) masih tersisa, sedangkan NaOH dan HCl habis bereaksi.. Jadi, garam yang terbentuk dari CH 3 COONa mengandung basa konjugasi. Sedangkan garam dari NH 4 Cl mengandung asam konjugasi.. Jenis-Jenis Larutan Buffer dan Cara Kerjanya

contoh soal asam basa kelas 11 Rumus buffer asam lemah basa lemah (lengkap contoh soal penyelesaian
Rumus Buffer Basa. Rumus ini mempertimbangkan larutan buffer basa dengan asam kuat, dan basa lemah (B) serta garamnya (BA). Nilai pOH dapat Anda hitung dengan cara yang sama seperti sebelumnya, sehingga rumus yang Anda dapatkan adalah: Contoh Soal dan Pembahasan 1. Contoh Soal 1.
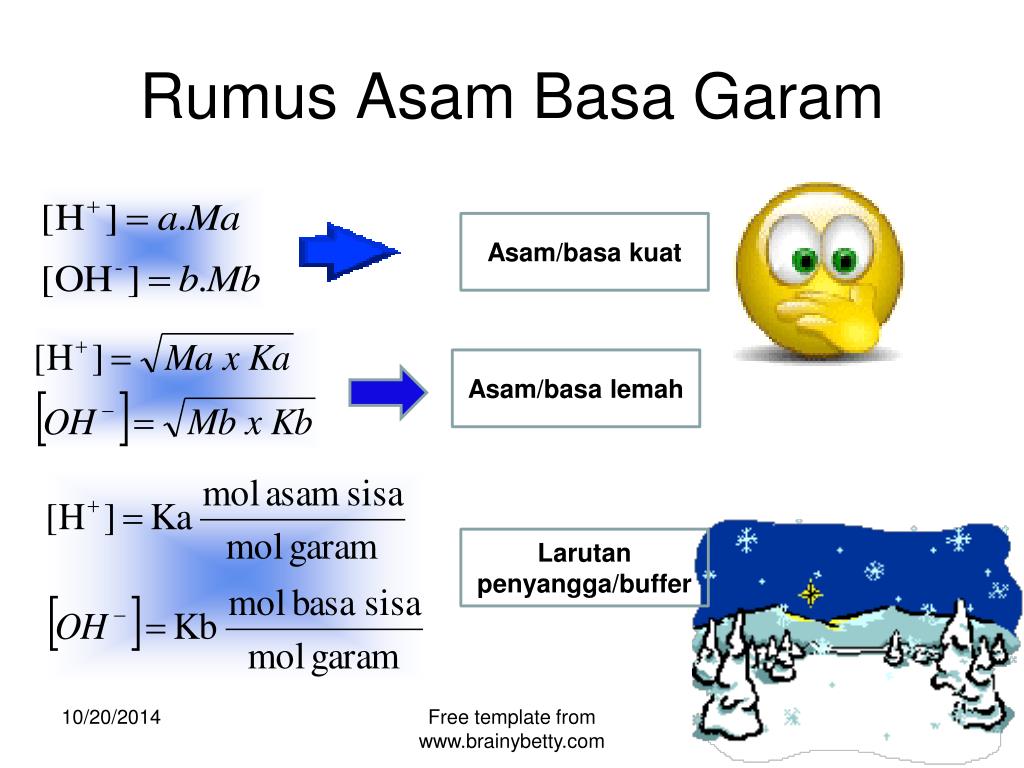
PPT ASAM BASA PowerPoint Presentation, free download ID5640840
Pada penambahan basa (OH−), kesetimbangan akan bergeser ke arah kanan, yakni reaksi pembentukan CH3COO− dan H+, sebagaimana untuk mempertahankan konsentrasi ion H+ yang menjadi berkurang karena OH− yang ditambahkan bereaksi dengan H+ membentuk H2O. b. Larutan penyangga basa. Larutan buffer basa mempertahankan pH pada suasana basa (pH > 7).
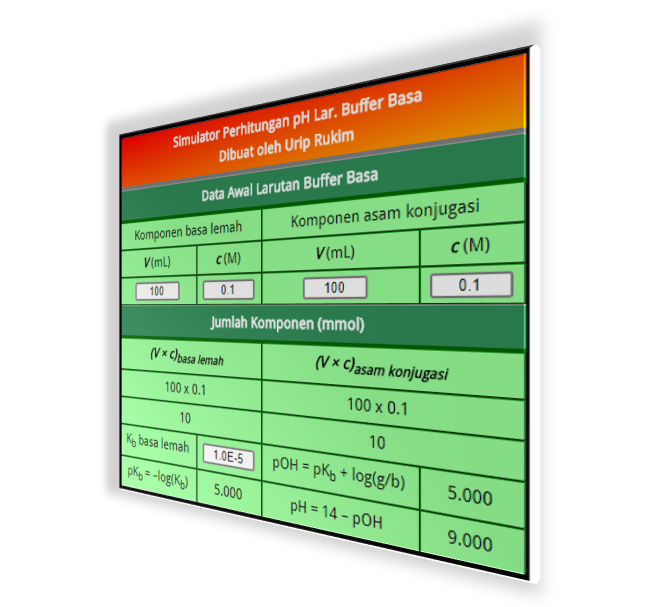
Simulator Perhitungan pH Larutan Buffer dan pH setelah Penambahan Asam/Basa Markas Belajar
Video ini pembahasan pengantar asam basa yang dikhususkan pada larutan penyangga. Pada pembahasan kali ini akan menelusuri beberapa kasus dengan konsep keset.

27+ Contoh Soal Hidrolisis Asam Lemah Basa Lemah Contoh Soal Terbaru
Larutan penyangga adalah larutan yang mampu mempertahankan derajat keasaman (pH) pada saat asam atau basa dimasukkan dalam suatu larutan. Larutan penyangga disebut juga "buffer" atau "penahan". Berikut ini yang termasuk dalam larutan buffer. 1. Campuran asam lemah dengan garam yang berasal dari asam lemah tersebut. Contoh : CH 3 COOH.

Unduh Contoh Soal Larutan Asam Basa Dan Pembahasannya Terbaru Dikdasmen My XXX Hot Girl
Dalam jmateri larutan penyangga kita akan belajar tentang dua macam larutan buffer yaitu buffer asam dan buffer basa juga rumus larutan penyangga yang dapat kamu pelajari dibawah ini. 1. Buffer asam. Pada larutan penyangga asam, buffer asam adalah larutan buffer yang mengandung campuran asam lemah dan basa konjugasinya. Cara membuat buffer asam:

Reaksi Asam Basa Rumus Kimia Contoh Soal Dan Jawaban Riset
Larutan penyangga basa adalah buffer yang terdiri dari basa lemah dan konjugasinya. Larutan ini terbentuk dari basa lemah dan garamnya, dan basa lemah dan asam kuat di mana jumlah mol basa lemah lebih banyak.. Agar lebih memahami rumus yang telah dimasukkan di atas, yuk kita mengerjakan contoh soal di bawah ini. Hitunglah PH larutan yang.

Penurunan Rumus pH Larutan Penyangga Basa Materi Larutan Penyangga Kimia SMA Pojan.id
Campuran tersebut mengandung basa konjugasi CH 3 COO -. 2. Larutan penyangga basa. Larutan penyangga basa merupakan larutan penyangga yang terdiri dari basa lemah dan asam konjugasinya. Larutan ini berfungsi untuk mempertahankan pH pada kondisi basa (pH > 7). Adapun contoh larutan penyangga basa adalah campuran antara NH 4 OH dan NH 4 Cl.

Chemical Analyst pH Larutan ( Menentukan Rumus Yang Akan Dipakai Untuk Mencari pH Suatu Larutan
Pengertian Larutan Buffer. Larutan penyangga (buffer) adalah larutan yang dapat menjaga (mempertahankan) pH-nya dari penambahan asam, basa, maupun pengenceran oleh air . pH larutan buffer tidak berubah (konstan) setelah penambahan sejumlah asam, basa, maupun air. Larutan buffer mampu menetralkan penambahan asam maupun basa dari luar.
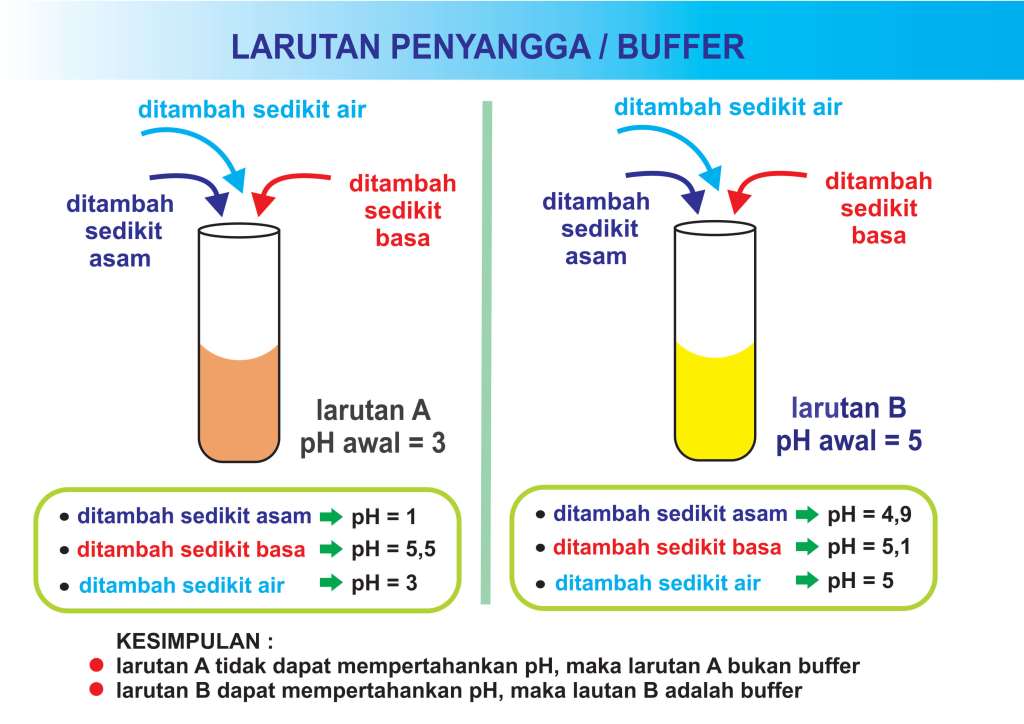
√ Larutan Penyangga / Buffer Pengertian, Rumus, dan Contoh Soal
Rumus buffer basa sangat penting dalam kimia karena dapat membantu dalam pembuatan larutan buffer basa yang berguna untuk menetralkan asam atau basa yang masuk ke dalamnya atau mencegah perubahan pH yang drastis ketika asam atau basa ditambahkan. Dalam menghitung rumus buffer basa, perlu dilakukan beberapa langkah seperti menentukan asam lemah.

Chemical Analyst pH Larutan ( Menentukan Rumus Yang Akan Dipakai Untuk Mencari pH Suatu Larutan
Bismillah.Berisi Penjelasan Mengenai Rumus dan Perhitungan Larutan Penyangga/Buffer Basa :- Basa lemah dengan garamnya (asam konjugasi)- Basa lemah dengan as.

Baru 28+ Rumus Ph
Tujuan dari larutan buffer adalah untuk membantu menjaga pH stabil ketika sejumlah kecil asam atau basa dimasukkan ke dalam larutan. Larutan penyangga fosfat adalah penyangga yang praktis untuk dimiliki, terutama untuk aplikasi biologis. Karena asam fosfat memiliki beberapa konstanta disosiasi, Anda dapat menyiapkan buffer fosfat di dekat salah satu dari tiga pH, yaitu pada 2,15, 6,86, dan 12,32.

Soal Larutan Asam Basa
Dalam mempelajari ilmu kimia, kamu akan sampai pada jenis larutan lainnya, yaitu larutan penyangga (buffer solution), yaitu larutan yang mempertahankan pHnya meski ditambahkan sedikit asam atau basa, maupun ketika diencerkan.Larutan ini berperan besar dalam menjaga pH darah maupun sel di dalam tubuh tetap stabil.

Inilah Contoh Soal Menghitung Ph Larutan Buffer Terbaru Daftar Contoh Soal 2022
Untuk larutan asam, pH-nya ini berada di angka 7 yang dibuat dari asam lemah seperti CH₃C00H, HCN, H₂C0₃, dan ditambahkan basa konjugasi. Jadi, meskipun namanya larutan asam, tapi tetap nih ada sifat basanya juga. Larutan Penyangga Basa. Nah, kalau untuk larutan basa, harus ada campuran antara basa lemah seperti NH₃ dan asam konjugasinya.
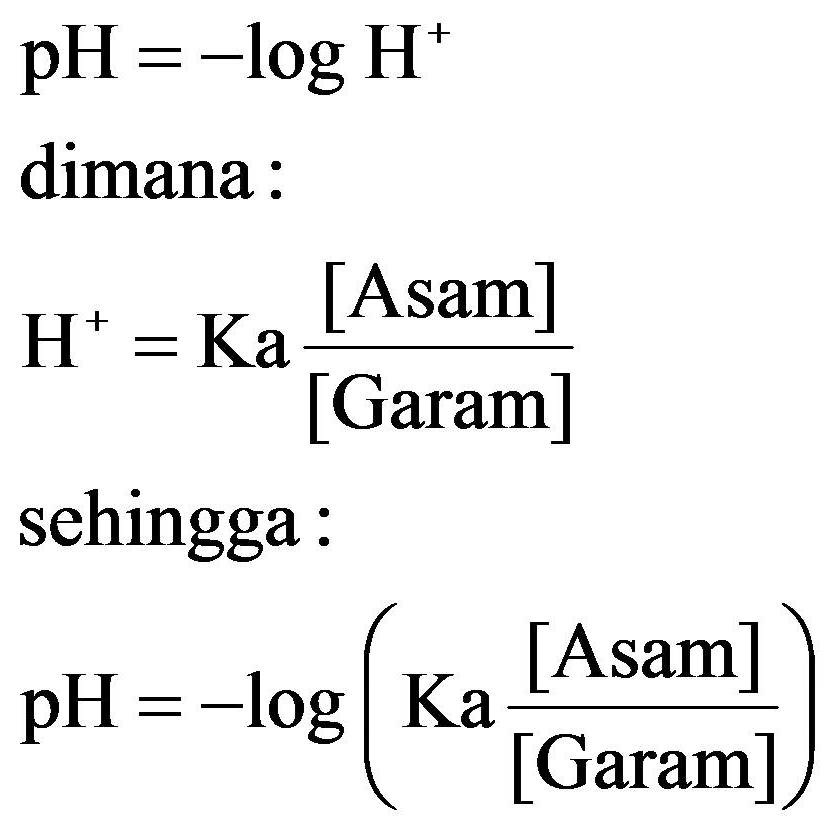
Menghitung Ph Campuran
Rumus Buffer Asam Lemah Basa Lemah - Kali ini kami akan berbagi materi kimia yang berkenaan dengan rumus Buffer asam lemah dan basa lemah. Tahukah sahabat bahwa istilah Buffer memiliki makna yang sama dengan Larutan Penyangga dalam kimia atau kadang juga disebut dengan Larutan Dapar.

(DOC) Buffer Asam dan Basa Victor Mendrofa Academia.edu
Rumus Buffer Asam ( PH < 7) LARUTAN PENYANGGA ATAU LARUTAN BUFFER | BIMBEL-Q.COM. LARUTAN PENYANGGA ATAU LARUTAN BUFFER | BIMBEL-Q.COM . Buffer Basa adalah campuran Basa Lemah dan garamnya. Contoh: NH 3 - NH 4 Cl → buffer basa NH 4 OH - NH 4 2 SO 4 → buffer basa. NH 3 - NH 4 CN → bukan buffer basa . Rumus Buffer Basa ( PH > 7)