
Mempelajari Konsep Reaksi Redoks (ReduksiOksidasi) Kimia Kelas 10
Konsep Reaksi Redoks - Contoh, Cara Menentukan Biloks dan Tatanama - Materi dasar redoks dipelajari pada kelas 10 SMA semester 2 dimana akan dilanjutkan juga nantinya pada kelas 12 lebih mendalam tentang penyetaraan reaksi redoks. Reaksi redoks adalah reaksi yang melibatkan reaksi reduksi dan reaksi oksidasi.

Penyetaraan Reaksi Redoks dengan Cara Biloks
Penyetaraan reaksi redoks merupakan suatu langkah penting dalam memahami perubahan kimia. Dalam tahap ini, keseimbangan antara elektron yang diterima dan diberikan pada setiap reaksi harus dilakukan dengan baik. Dengan demikian, memahami cara penyetaraan reaksi redoks akan memudahkan pemahaman tentang konsep dasar Kimia dalam konteks simbolis. Maka dari itu, mari kita bedah lebih lanjut.
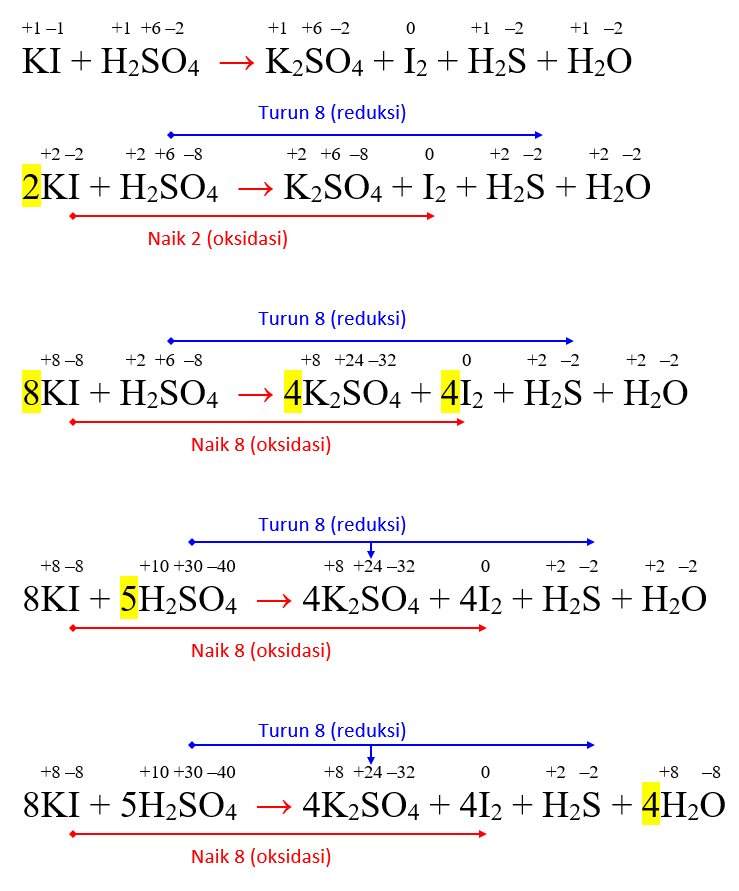
Penyetaraan Reaksi Redoks KI + H2SO4 → K2SO4 + I2 + H2S + H2O Markas Belajar
Fundamental. Reaksi Redoks: Pengertian, Bilangan Oksidasi, Penyetaraan Redoks, Aplikasi [Lengkap+Contoh Soal] Reaksi redoks atau reduksi - oksidasi, merupakan reaksi yang menunjukkan adanya perubahan bilangan oksidasi pada reaktan dan produk. Prinsip reaksi redoks banyak diaplikasikan dalam kehidupan sehari-hari, seperti pada baterai dan aki.

45 Latihan Soal Penyetaraan Reaksi Redoks Pilihan Ganda Dan Jawaban Jempol kimia
Setarakan unsur yang mengalami reaksi redoks, yaitu unsur yang mengalami perubahan bilangan oksidasi. Tambahkan molekul H2O pada ruas yang kekurangan atom O dan ruas yang kelebihan atom O.. Nantinya, penyetaraan reaksi redoks dapat diselesaikan dengan menggunakan metode perubahan biloks (PBO), baik pada reaksi molekul dan reaksi ion di mana.

PENYETARAAN REDOKS DENGAN CARA BILOKS UNTUK REAKSI ION (Part 1) YouTube
5. Mengalikan koefisien masing-masing setengah-reaksi dengan bilangan bulat tertentu agar jumlah e − yang dilepas dalam setengah-reaksi oksidasi sama dengan jumlah e − yang diterima dalam setengah-reaksi reduksi. 6. Menggabungkan kedua setengah-reaksi yang sudah setara tersebut menjadi satu persamaan reaksi, lalu menghilangkan jumlah spesi-spesi yang sama pada kedua sisi

Penyetaraan reaksi redoks metode bilangan oksidasi MnO4− + SO32− → MnO2 + SO42− dalam suasana
Reduksi adalah peristiwa reaksi yang menurunkan bilangan oksidasia yang mengakibatkan terjadinya kenaikan elektron. Menurut penjelasan tersebut, reduksi bisa diartikan sebagai reaksi ketika suatu zat kehilangan oksigen. Reaksi redoks kelas 12 adalah reaksi ketika suatu atom mengalami penurunan bilangan oksidasi.

Penyetaraan reaksi redoks MnO4 dan SO3 2 dalam suasana asam dengan metode bilangan oksidasi
Berdasarkan penangkapan atau pelepasan oksigen. Oksidasi: reaksi yang melibatkan penangkapan atom oksigen. Contoh: C+ O2 → CO2. Atom C (karbon) mengalami oksidasi karena dalam reaksi atom karbon mengikat atom oksigen menjadi CO2. Reduksi: reaksi yang melibatkan pelepasan atom oksigen. Contoh: H2O2 → H2O + O2.
Reaksi Redoks dan Reaksi Reduksi
Latihan Soal Penyetaraan Reaksi Redoks (Sedang) Pertanyaan ke 1 dari 5. 1. Pertanyaan. Reaksi setengah oksidasi dari reaksi berikut dalam kondisi asam adalah. . Br2 → BrO − 3 + Br −. 1. 2BrO − 3 + 6H2O + 10e → Br2 + 12OH −. 2.

Penyetaraan reaksi redoks metode setengah reaksi suasana asam YouTube
Reaksi redoks adalah reaksikimia yang menyebabkan adanya perubahan bilangan oksidasi pada suatu unsur, maupun molekul.. Pada reaksi diatas, Cl2 mengalami reduksi menjadi KCl dimana penurunan bilangan oksidasi Cl (0) menjadi Cl(-1).. Baca juga: Rumus Keliling Layang-Layang beserta Contoh dan Pembahasannya. Penyetaraan Reaksi Redoks.

Konsep Reaksi Redoks
Berdasarkan hal tersebut, maka persamaan reaksi redoks yang sudah setara pada suasana basa adalah: 2MnO + 5PbO 2 + 4H 2 O → 2MnO 4 - + 5Pb 2+ + 8OH - Cara Setengah Reaksi. Berikut langkah-langkah penyetaraan reaksi redoks dengan cara setengah reaksi: Setarakan jumlah atom yang terlibat dalam reaksi, kecuali atom O dan H.

Materi Reaksi Redoks Homecare24
Adapun fungsi reaksi redoks dalam kehidupan sehari-hari, antara lain: - Untuk memahami fenomena korosi logam dan cara pencegahannya. - Penggunaan lumpur aktif untuk mengolah limbah. - Mengetahui reaksi fotosintesis. - Oksidasi makanan dalam sel. - Mur dan baut diberi lapisan zinc, di mana dalam lapisan itu terdapat proses oksidasi logam zinc.
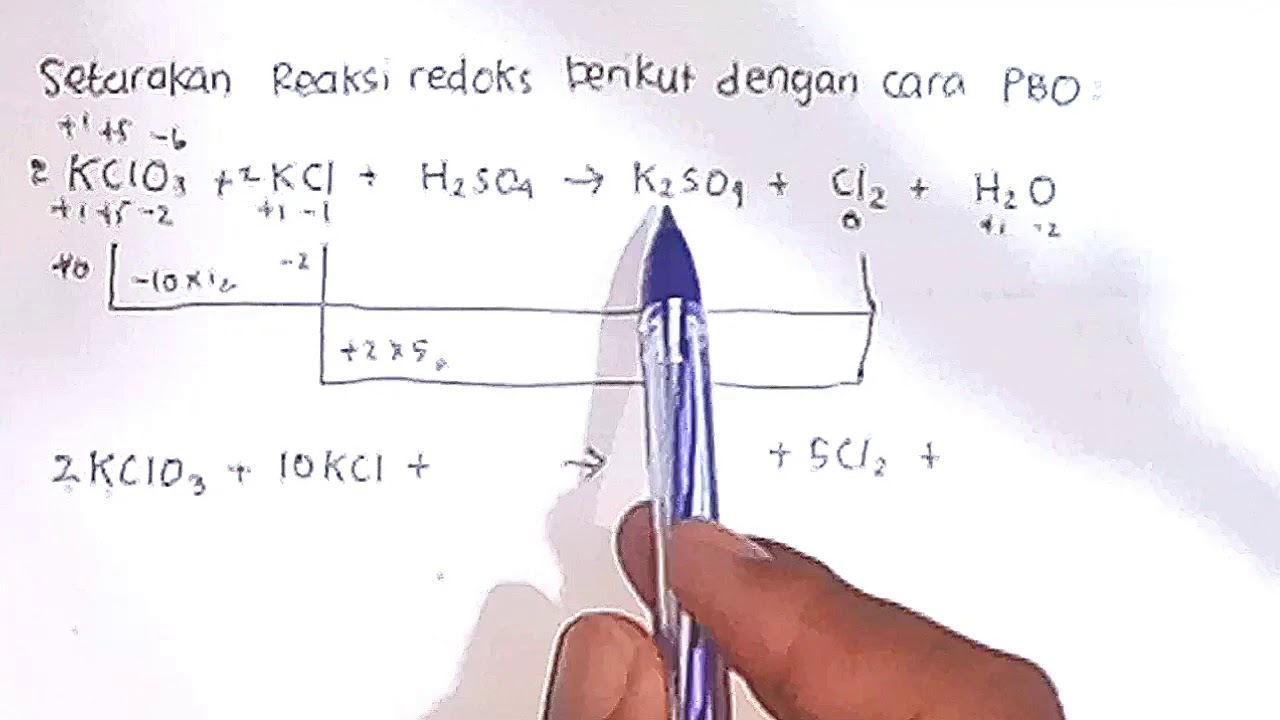
Penyetaraan Reaksi Redoks Cara PBO YouTube
Tahap terpenting dalam reaksi redoks adalah penyetaraan jumlah atom dan muatan yang ada di reaktan dan produknya. Nah, penyetaraan ini bisa dilakukan dengan beberapa cara, yaitu: Metode Bilangan Oksidasi. Elo cermati mana aja unsur yang mengalami perubahan biloks, hitung biloks setiap elemen, lalu hitung kenaikan atau penurunan biloks per unsurnya.

Penyetaraan Reaksi Redoks
Langkah 2: Setarakan unsur selain O dan H. Dalam kasus ini, hanya Cr yang perlu disetarakan. Cr 2 O 72-(aq) → 2Cr 3+(aq) HNO 2 (aq) → NO 3-(aq) Langkah 3: Tambah H 2 O untuk menyetarakan oksigen. Reaksi chromium membutuhkan 7H 2 O untuk bisa setara. Reaksi yang lain, hanya membutuhkan 1H 2 O untuk setara.

Penyetaraan Reaksi Redoks Cara Setengah Reaksi YouTube
24. Reaksi redoks yang sudah mengalami penyetaraan ialah.. a. I 2 (s). Yang mengalami reaksi disproporsionasi adalah bromine dari biloks 0 menjadi -1 dan +1. 40. Diketahui beberapa persamaan reaksi berikut:. Download Soal penyetaraan reaksi redoks: Google Drive. Sudah selesai membaca dan berlatih soal ini ?

Diantara reaksi redoks berikut ini yang sudah setara adal...
Oke, kita lanjut ya bahasannya! Pada reaksi redoks, terdapat unsur-unsur yang bertindak sebagai reduktor dan oksidator. Zat yang mengalami oksidasi itu disebut reduktor, sedangkan zat yang mengalami reduksi disebut oksidator. Coba perhatikan contoh berikut ini, ya! Reaksi: Mg(s) + 2HCl -----> MgCl2(aq) + H2(g) Karena Mg merupakan unsur bebas, jadi biloks Mg = 0.

Penyetaraan Reaksi Redoks Metode Biloks YouTube
Reaksi yang memenuhi adalah reaksi B karena jumlah atom di kedua sisi sama dan muatan di kedua sisi sama, yaitu +2. Jadi, reaksi redoks yang sudah mengalami penyetaraan adalah B. Perdalam pemahamanmu bersama Master Teacher di sesi Live Teaching, GRATIS!