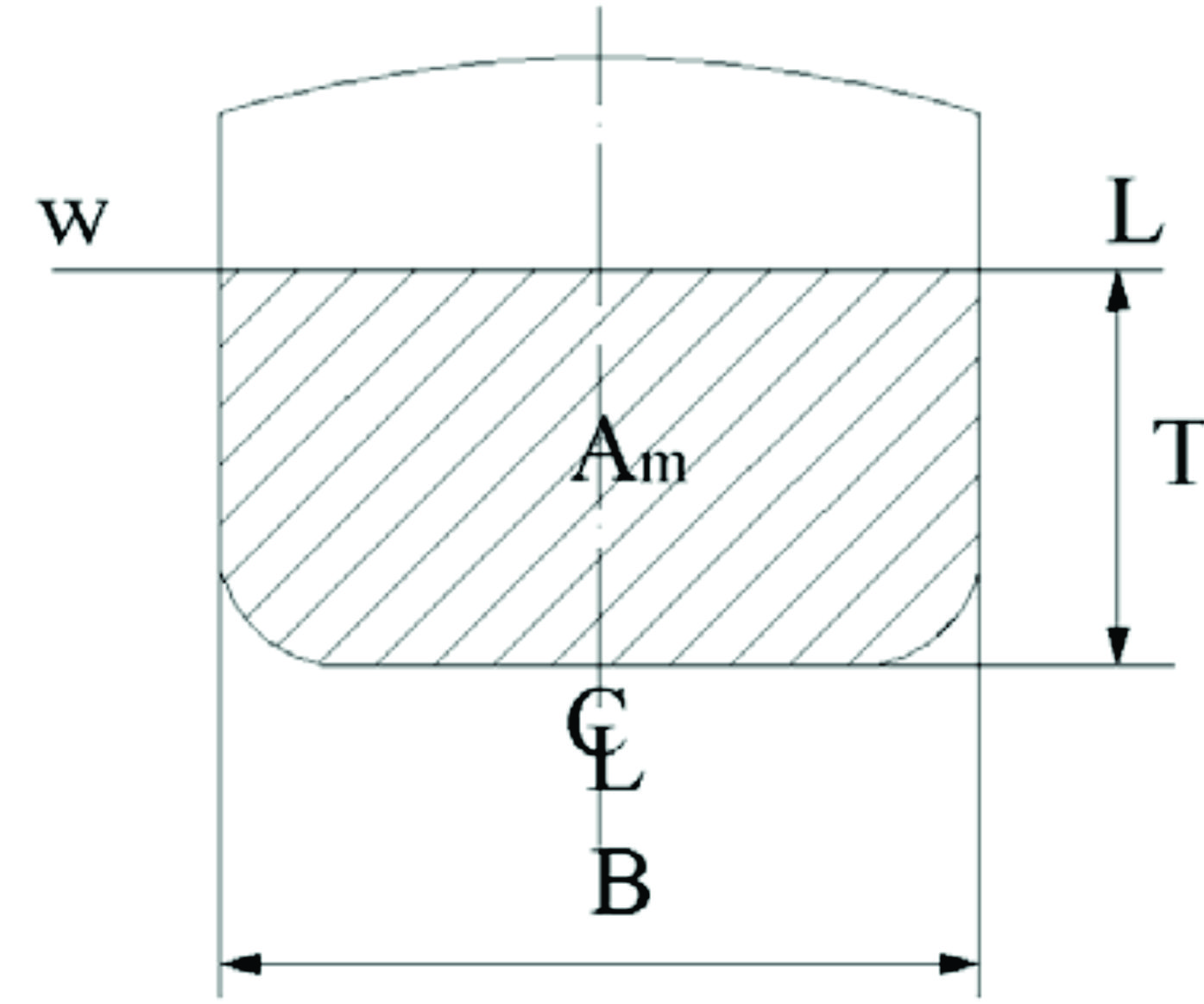
Materi Kuliah Koefisien Bentuk Dan Perbandingan Ukuran Utama Pada Kapal
Stoikiometri (Perhitungan Kimia) 4. Larutan Elektrolit dan Nonelektrolit. 5. Reaksi Redoks (Reduksi-Oksidasi) Koefisien reaksi merupakan perbandingan jumlah partikel dari zat yang terlibat dalam reaksi. Oleh karena 1 mol setiap zat mengandung jumlah partikel yang sama, maka perbandingan jumlah partikel sama dengan perbandingan jumlah mol. Jadi.

Cara Menghitung Koefisien Variasi Data Berkelompok Satu Manfaat
Perbandingan koefisien reaksi ini dinamakan rasio stoikiometri yang disingkat RS. Dalam ilmu kimia mol adalah satuan pengukuran jumlah yang standar. Ketika kita mereaksikan zat-zat tertentu, zat tersebut bereaksi dengan perbandingan mol yang bulat dan sederhana tetapi kita tidak dapat menghitung jumlah zat-zat tersebut secara langsung dengan.

Perbandingan Ukuran kapal dan karakteristik kapal Kapal Pelaut Surveyor
Zat pereaksi tersebut akan berubah menjadi produk jika memenuhi perbandingan koefisien tertentu. perbandingan koefisien biasanya mengacu pada jumlah mol yang terlibat selama reaksi berlangsung. Penentuan mol produk didasarkan pada perbandingan koefisien mol zat pereaksi. Nah, jika mol pereaksinya berasal dari dua zat yang bereaksi, maka perlu.

Dalam Persamaan Reaksi Yang Setara Berlaku Perbandingan Mol Sama Dengan Perbandingan Koefisien PDF
Perbandingan koefisien-koefisien reaksi menunjukkan perbandingan mol zat-zat yang bereaksi dalam reaksi kimia tersebut. Pada setiap reaktan dan produk perlu dituliskan wujud zatnya, seperti ( s) yaitu padat (solid) , (l) yaitu cair (liquid) , (g) yaitu gas , atau (aq) yaitu larutan dengan pelarut air (aqueous) di dalam tanda kurung di sisi.
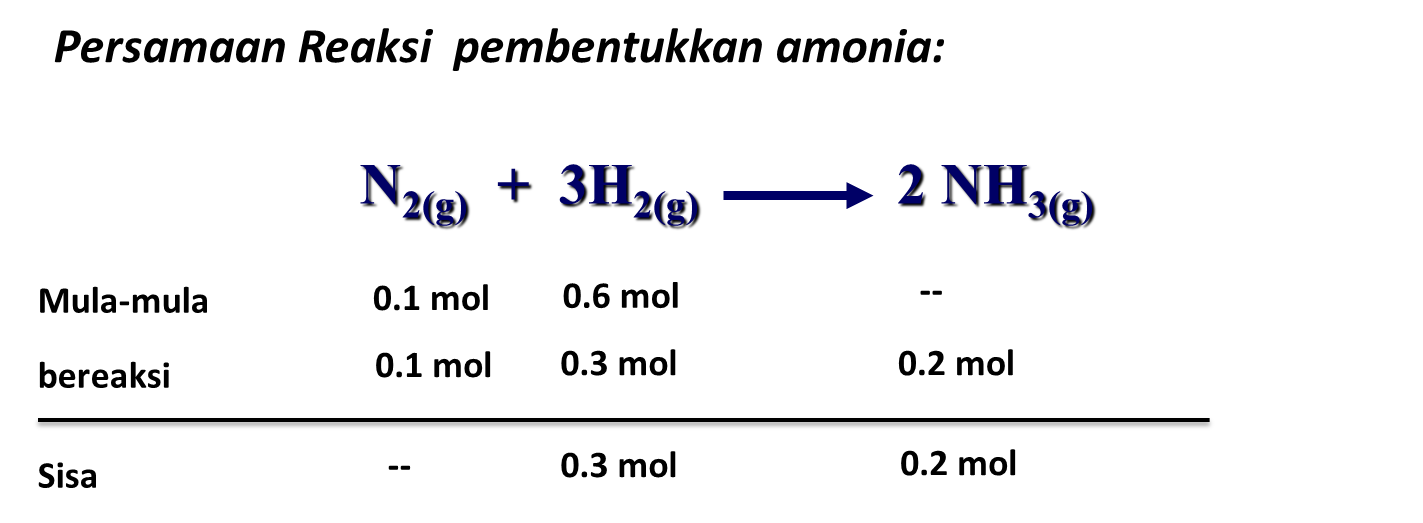
Koefisien Reaksi Dan Indeks Perhatikan Dan Lengk My XXX Hot Girl
menuliskan perbandingan koefisien dari persamaan reaksi kimiayang setara

Perbandingan antara koefisien suku ketiga dan suku kedua
Persamaan yang menunjukkan perubahan zat sebelum dan sesudah reaksi kimia yang dinyatakan dengan rumus kimia, koefisien reaksi dan wujud zat. Persamaan Suatu Reaksi Kimia. Sebuah persamaan suatu reaksi adalah persamaan yang menunjukkan perubahan zat-zat yang terjadi selama reaksi kimia berlangsung. Zat-zat yang terletak di sebelah kiri tanda.

Koefisien reaksi atau nilai a, b, c, dan d dari persamaan...
Unsur-unsur perbandingan mungkin terdapat interaksi dari dua atau lebih perbandingan. Nilai koefisien untuk perbandingan interaksi tersebut ditentukan dengan cara multiplikasi (perkalian) dari koefisien-koefisien yang bersesuaian dari kedua perbandingan (Tabel 11). Tabel 11. Percobaan pemupukan dengan 4 perlakuan, 2 taraf untuk N dan 2 taraf.

Koefisien Variasi Koefisien variasi adalah perbandingan antara simpangan
Perbandingan koefisien-koefisien reaksi menunjukkan perbandingan mol zat-zat yang bereaksi dalam reaksi kimia tersebut. Pada setiap reaktan dan produk perlu dituliskan wujud zatnya, seperti s yaitu padat (solid), l yaitu cair (liquid), g yaitu gas, atau aq yaitu larutan dengan pelarut air (aqueous) di dalam tanda kurung di sebelah kanan rumus.

Gambar 5 Perbandingan koefisien perpindahan panas konveksi pada... Download Scientific Diagram
Persamaan (18) membuktikan kepada kita bahwa besar koefisien muai volume suatu bahan sama dengan 3/2 kali koefisien muai luasnya. Contoh Soal 3: Sebuah bola yang memiliki volume 50 m 3 jika dipanaskan hingga mencapai temperatur 50 o C. Jika pada kondisi awal, kondisi tersebut memiliki temperatur 0 o C, tentukanlah volume akhir bola tersebut.

Koefisien Reaksi Dan Indeks Perhatikan Dan Lengk Riset My XXX Hot Girl
Hasil mol koefisien HCl < Fe, sehingga HCl sebagai pereaksi pembatas. Selanjutnya jumlah mol dari limiting reagent inilah yang menentukan jumlah mol reaksi/hasil reaksi. Misal dari contoh soal tersebut ditanyakan massa FeCl2 yang terbentuk, sehingga. nFeCl2 = 1 2 × mol HCl = 1 2 × 0, 1 mol = 0, 05 mol mFeCl2 = 0, 05 × 127 gram = 6, 35 gram.

Soal Perbandingan antara koefisien suku keenam dan suku keempat dari penguraian (2a+3b)^(8) ada
Perbandingan koefisien-koefisien reaksi dapat diinterpretasi sebagai perbandingan mol zat-zat dalam reaksi. Pada setiap reaktan dan produk, dituliskan wujud zatnya (s (padat), l (cair), g (gas), atau aq (larutan dengan pelarut air)) dalam tanda kurung di sebelah kanan rumus molekuler masing-masing.

Soal Sbm Kimia Perbandingan Koifisien Reaksi Read Master
Bila diperhatikan bahwa hasil perbandingan volume dari percobaan Gay-Lussac sama dengan perbandingan koefisien gas-gas yang bereaksi dalam persamaan reaksi setara. Sehingga ia menyimpulkan penerapan hukum perbandingan volume dalam kehidupan sehari-hari bahwa pada suhu dan tekanan yang sama, volume gas-gas yang bereaksi dan hasil reaksi.

Perbandingan koefisien H2S dan Na2S dalam reaksi setaraN...
Apakah Anda ingin belajar kimia dasar dengan mudah dan menyenangkan? Tonton video ini untuk mempelajari cara mencari koefisien persamaan reaksi kimia dengan metode sederhana dan efektif. Video ini.

Gambar 5 Perbandingan koefisien perpindahan panas konveksi pada... Download Scientific Diagram
Koefisien reaksi = 1 di depan NH 2, 3 di depan H 2, dan 2 di depan NH 3. Indeks reaksi = 2 di sebelah kanan bawah N, 2 di sebelah kanan bawah H,. Saat diminta perbandingan antara volume gas satu dan lainnya pada suhu dan tekanan tertentu, gunakan persamaan berikut. Keterangan: n 1 = jumlah mol gas ke-1;

Gambar 5 Perbandingan koefisien perpindahan panas konveksi pada... Download Scientific Diagram
Pembahasan Koefisien reaksi merupakan perbandingan jumlah partikel dari zat yang terlibat dalam reaksi. Oleh karena 1 mol setiap zat mengandung jumlah partikel yang sama, maka perbandingan jumlah partikel sama dengan perbandingan jumlah mol. Jadi, koefisien reaksi merupakan perbandingan jumlah mol zat yang terlibat dalam reaksi.

PPT KONSEPKONSEP DASAR TERMODINAMIKA PowerPoint Presentation, free download ID4751506
Koefisien muai panjang adalah perbandingan pertambahan panjang benda dari panjangnya semula setiap kenaikan suhu sebesar satu satuan suhu, dirumuskan α = ΔL / L 0. ΔT. Gimana adik-adik, udah paham kan materi koefisien muai panjang di atas? Jangan lupa lagi yah. Sekian dulu materi kali ini, bagikan agar teman yang lain bisa membacanya..