
Teori Asam Basa Menurut Para Ahli Beserta Contohnya Semua Halaman Hot Sex Picture
Berdasarkan teori Lewis, H 2 O adalah basa Lewis karena mendonorkan pasangan elektron kepada ion H + yang berasal dari molekul HCN membentuk ion H 3 O + sedangkan H + dari HCN adalah asam Lewis karena menerima pasangan elektron dari atom O pada H 2 O. 2. Teori Arrhenius dan teori Brønsted-Lowry tidak dapat menjelaskan reaksi ini.
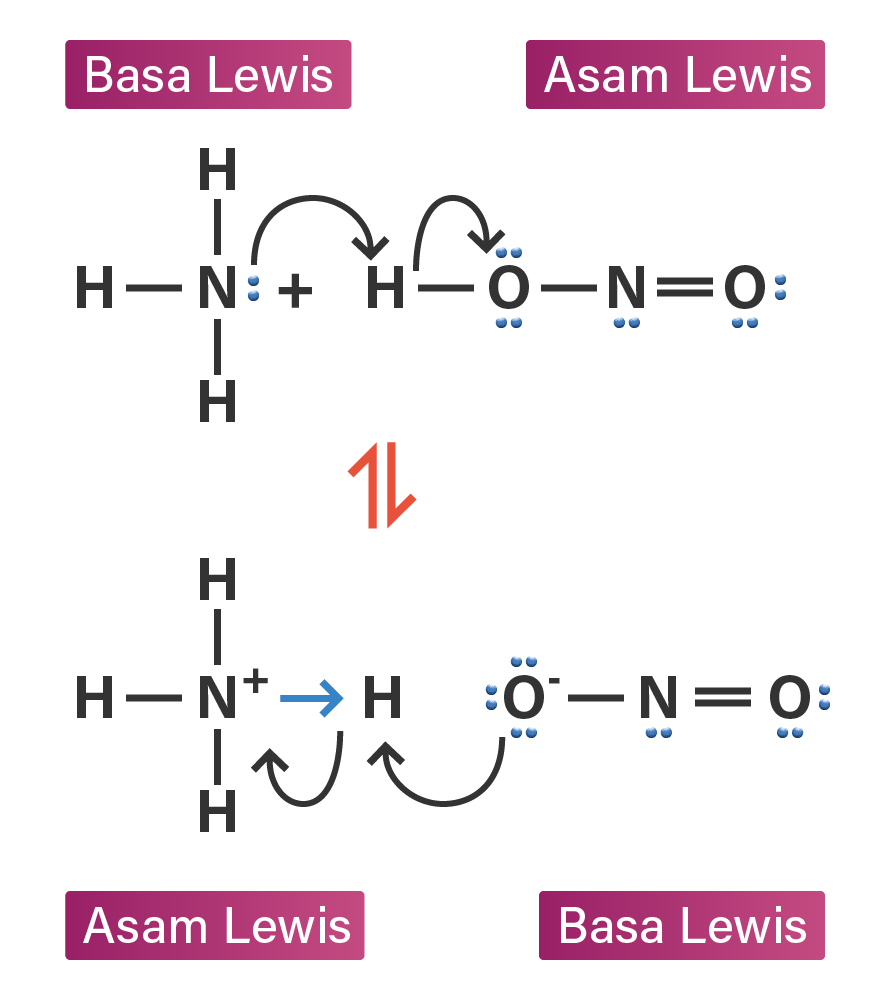
tuliskan pasangan asam basa lewis dari reaksi beri...
Trimetilborana (Me 3 B) adalah suatu asam Lewis karena mampu menerima pasangan elektron sunyi. Dalam suatu aduk Lewis, asam dan basa Lewis berbagi pasangan elektron yang dilengkapi oleh basa Lewis, membentuk ikatan koordinasi. [1] Dalam konteks reaksi kimia tertentu antara NH 3 dan Me 3 B, pasangan elektron sunyi dari NH 3 akan membentuk ikatan.

LENGKAP ‼️ Teori Asam Basa Lewis Latihan Soal dan Pembahasan YouTube
Lewis: Menurut definisi ini, asam adalah penerima pasangan elektron dari basa. Definisi yang dikemukakan oleh Gilbert N. Lewis ini dapat mencakup asam yang tak mengandung hidrogen atau proton yang dapat dipindahkan, seperti besi(III) klorida. Definisi Lewis dapat pula dijelaskan dengan teori orbital molekul.

27+ Contoh Soal Asam Basa Lewis Ike Hodge
Contoh dari beberapa asam Lewis adalah SO3, BF3, maupun AlF3. Sedangkan basa menurut Newton Lewis merupakan zat yang mampu memberikan pasangan pada electron. Dalam pandangan teori asam basa Lewis, basa memiliki pasangan yang elektronnya bebas, contohnya adalah seperti NH3, Cl-, maupuan ROH.

XI.6.q. Teori Asam Basa Lewis (Teori) YouTube
Pengertian asam menurut ilmu kimia berarti sebuah senyawa kimia atau zat yang bisa dilaturkan dalam air dan akan menghasilkan larutan dengan pH yang lebih kecil dari 7 serta yang bisa memberikan proton [ion H+] pada zat lain atau senyawa lain yang dinamakan dengan basa.. Pengertian Teori Asam Basa Lewis.

Struktur Lewis Asam Sulfat H2SO4 dan Cara Menggambarnya
Teori Asam Basa Menurut Lewis. Materi Asam-Basa: Pengertian, Ciri-Ciri, Contoh, & Rangkuman. Pengertian Asam, Basa, dan Garam: Ciri, Contoh, dan Rangkuman. Teori Asam Basa Menurut Para Ahli Serta Indikator Alami dan Buatan. Populer Jokowi Tunjuk Ma'ruf Amin jadi Plt Presiden hingga 6 Maret 2024.

Asam Basa Teori, Contoh, dan Sifat Asam Basa InformasainsEdu
Berdasarkan persamaan reaksi asam basa yang disampaikannya, Lewis mengatakan bahwa asam adalah suatu molekul atau ion yang bisa menerima pasangan elektron. Sementara basa adalah molekul atau ion yang bisa memberikan pasangan elektronnya. Menurut Lewis senyawa asam adalah senyawa yang bisa menerima pasangan elektron atau akseptor pasangan elektron.

Konsep Mudah Belajar Teori Asam Basa LewisKimia SMA YouTube
Salah satu pengertian asam yang dapat digunakan sebagai dasar pemahaman adalah menurut konsep asam menurut Lewis. Gagasan ini diperkenalkan oleh ilmuwan Gilbert N. Lewis pada tahun 1923. Konsep asam menurut Lewis memberikan sudut pandang yang berbeda tentang sifat-sifat asam dan dapat membantu dalam memahami interaksi kimia yang kompleks.
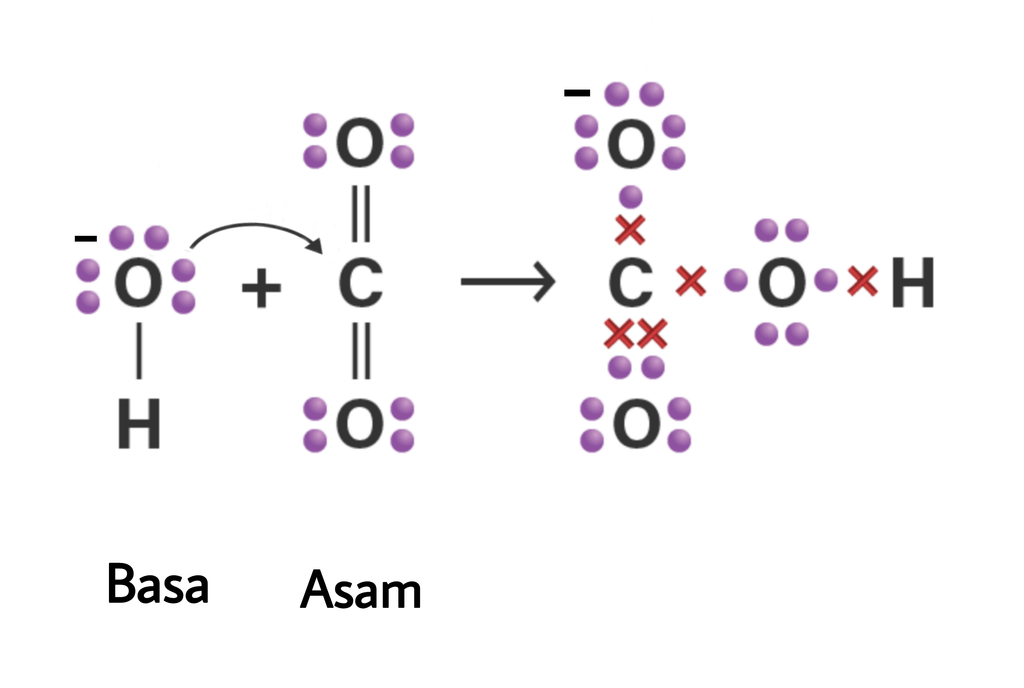
Berdasarkan teori asam basa Lewis, manakah spesi y...
Oleh karena itu, pada tahun 1932, Gilbert N. Lewis, seorang kimiawan asal Amerika Serikat mengemukakan teori asam basa yang lebih luas dibandingkan dua teori sebelumnya yang kemudian dikenal dengan teori asam basa Lewis. Menurut Lewis, asam basa adalah reaksi yang berkaitan dengan proses serah terima (transfer) elektron.

Pengertian Larutan Asam Basa, Contoh serta Indikator Asam Basa PerpusPedia
Pengertian Asam Basa Menurut Lewis - Konsep asam basa merupakan salah satu konsep dalam kimia yang sangat penting. Konsep ini membantu kita memahami bagaimana suatu zat dapat bereaksi dalam larutan, dan memberikan pemahaman yang mendalam tentang sifat-sifat asam dan basa. Salah satu tokoh yang memberikan kontribusi besar dalam pengembangan.
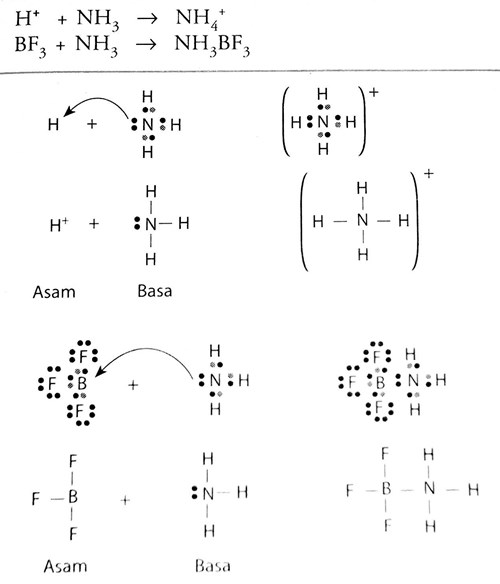
Teori AsamBasa Lewis
Baca juga: Teori Asam Basa: Pengertian Para Ahli dan Sifatnya. Menurut teori asam basa Lewis, asam adalah zat yang menerima pasangan elektron. Sedangkan basa adalah zat yang menyumbangkan atau mendonasikan pasangan elektron. Di mana transpor elektron tersebut membuat asam dan basa bereaksi, sehingga menghasilkan ikatan kovalen koordinat.

Spesi berikut yang berperan sebagai asam Lewis adalah.
Mulai dari pengertian, teori menurut para ahli, ciri-ciri, hingga contohnya. Jadi, untuk kamu yang sedang mencari informasi lengkap tentang asam & basa, simak artikel ini hingga habis, ya!. Asam menurut Lewis adalah zat yang punya kecenderungan menerima pasangan elektron basa, sedangkan basa adalah zat yang memberikan pasangan elektron.

studying chemistry belajar kimia Teori Asam Basa Lewis
Menurut Lewis, asam adalah suatu senyawa yang melakukan akseptor elektron atau menerima elektron sedangkan basa adalah senyawa yang melakukan donor elektron atau memberikan elektron. Teori asam basa Lewis ini lebih spesifik dari teori sebelumnya yang hanya mendefinisikan keberadaan ion H + dan ion OH - .

Contoh Soal Asam Basa Lewis Asam Basa Pengertian Teori Reaksi Indikatornya Lengkap Contoh
Pengertian asam menurut Arrhenius yaitu Asam Arrhenius jika berdiosiasi dalam air membentuk ion hidrogen.. Jika kita telaah lagi dari pengertian asam-basa lewis maka, dapat dikatakan bahwa semua asam dan basa Bronsted adalah asam dan basa lewis. Hal ini dikarenakan asam lewis merupakan yang menerima pasangan elektron, sedangkan asam konjugat.
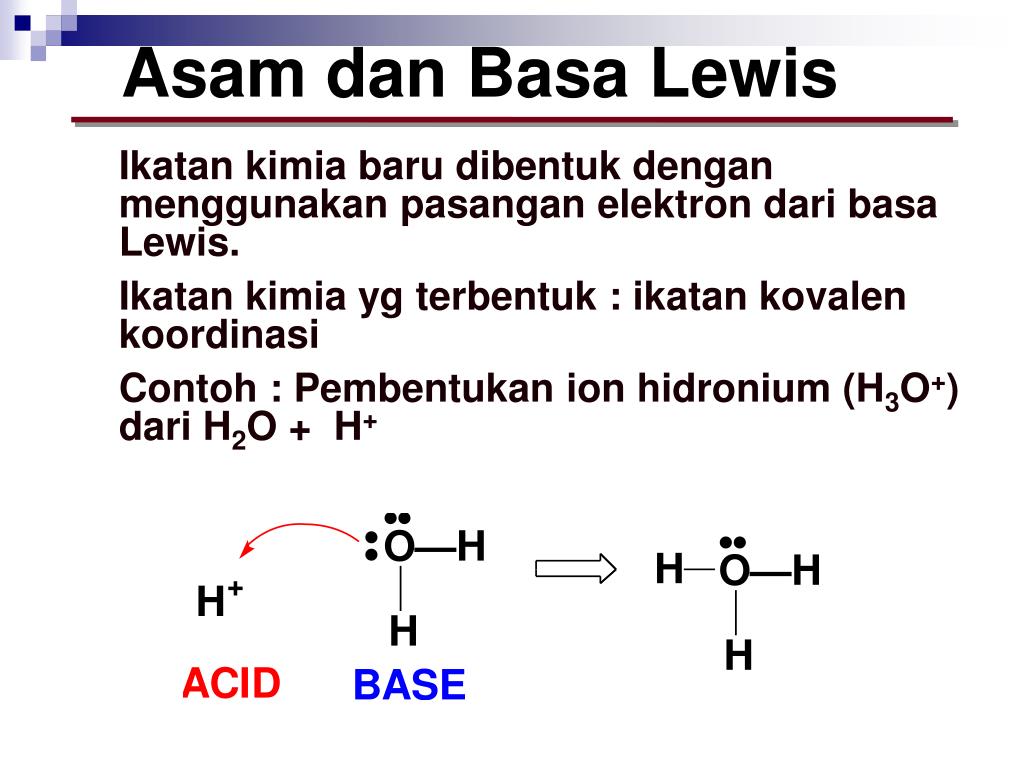
PPT ASAM DAN BASA PowerPoint Presentation, free download ID4714427
Beberapa ciri khas dari reaksi asam dan basa menurut Lewis antara lain: - Asam dan basa dapat berupa senyawa yang tidak larut dalam air, sehingga reaksi asam dan basa menurut Lewis tidak terbatas pada larutan air saja. - Reaksi asam dan basa menurut Lewis dapat terjadi tanpa adanya ion H+ (hidrogen) atau ion OH- (hidroksil) dalam reaksi.
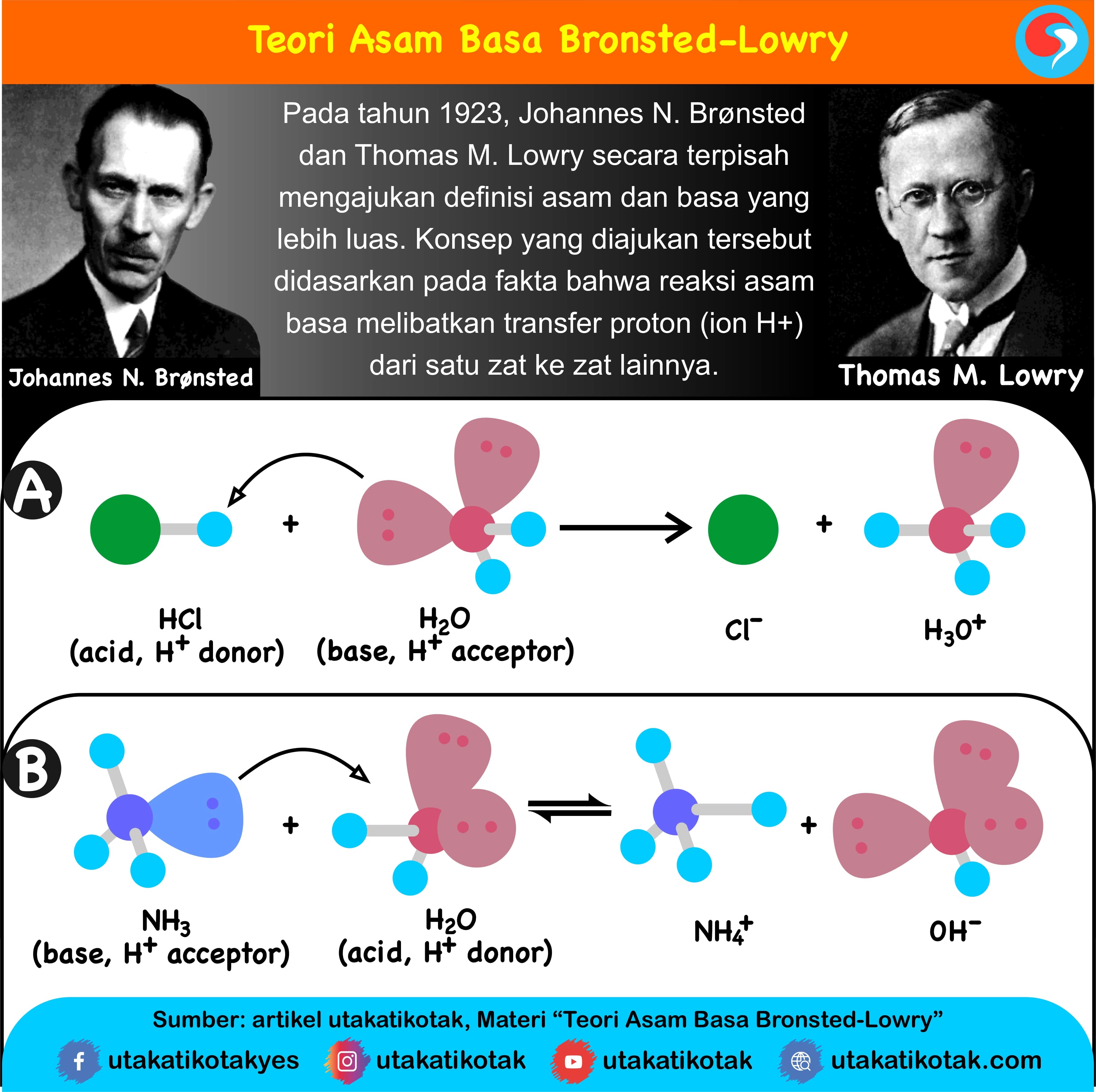
Pengertian Asam dan Basa Menurut BronstedLowr
Penjelasan Lengkap: jelaskan pengertian asam basa menurut arrhenius bronsted lowry dan lewis 1. Svante Arrhenius mengembangkan teori Asam Basa Arrhenius pada tahun 1887 yang menyatakan bahwa asam adalah senyawa yang menghasilkan ion hidrogen (H+) saat larut dalam air, sedangkan basa adalah senyawa yang menghasilkan ion hidroksida (OH-) saat larut dalam air.