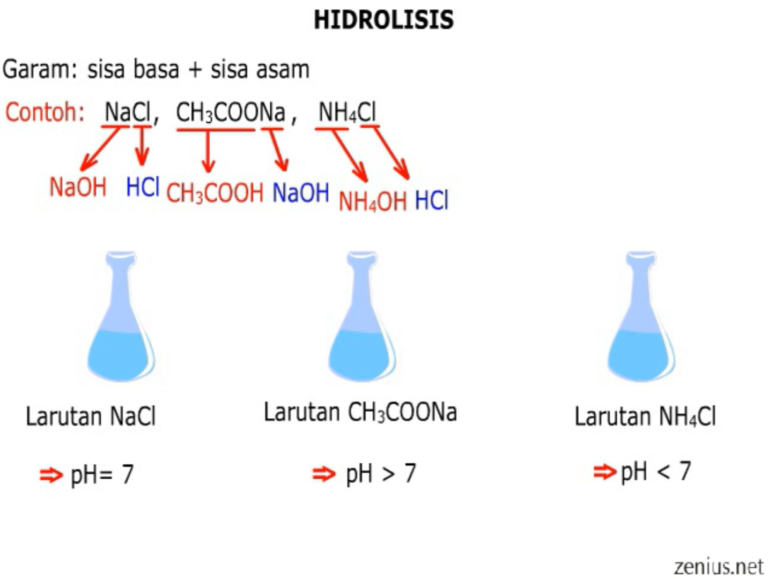
Pasangan Persamaan Reaksi Hidrolisis Untuk Garam Yang Bersifat Asam Adalah Homecare24
Contoh reaksi penghasil larutan asam adalah reaksi antara asam sulfat (H2SO4) dengan air: H2SO4 (aq) + H2O (l) → H3O+ (aq) + HSO4- (aq) Dalam reaksi ini, asam sulfat bereaksi dengan air membentuk ion hidronium (H3O+) dan anion hidrogen sulfat (HSO4-). Sehingga terbentuk larutan asam dengan konsentrasi ion H+ yang tinggi.

Trik Menentukan Pasangan Asam Basa Konjugasi KIMIA OKE PINTAR
Pasangan hidroksida yang bersifat asam adalah Si(OH) 4 dan P(OH) 5. Reaksi hidroksida asam : P(OH) 5 : asam lemah, Si(OH) 4: asam lemah, S(OH) 6: asam kuat : Cl(OH) 7 : asam kuat. NaOH : basa kuat, Mg(OH) 2 : basa lemah : Al(OH) 3 : basa yang sangat lemah. 35. Alumunium tergolong logam tahan korosi. Sifat inilah yang menyebabkan alumunium.
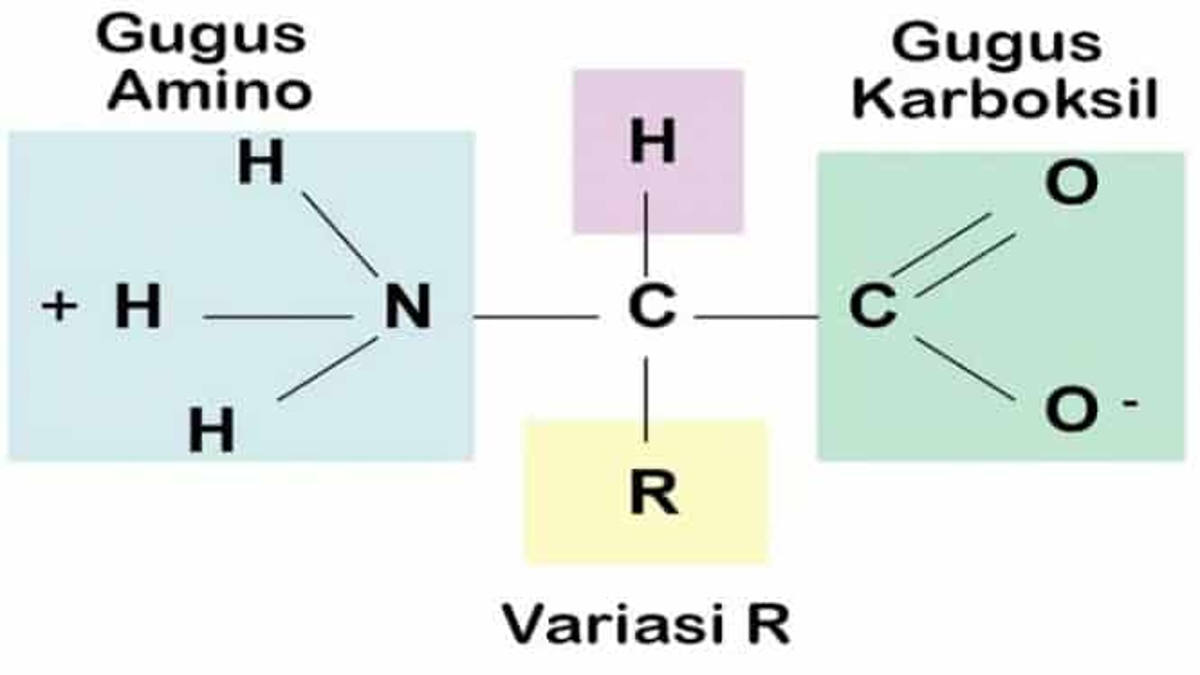
Sifat Asam Amino yang Sangat Dibutuhkan Beserta Klasifikasinya!
BASA Menurut Arrhenius, basa adalah semua zat yang jika dilarutkan dalam air akan menghasilkan ion OH- misalnya pada senyawa natrium hidroksida NaOH akan terurai menjadi Na+ dan OH-. Jika basa bereaksi dengan asam, maka dihasilkan senyawa 'garam'. Sifat yang umum pada senyawa basa dapat dilihat pada rasanya yaitu pahit serta jika diraba dengan jari akan terasa licin.

Reaksi antara asam sulfat dengan aluminium hidroksida aka...
Senyawa hidroksida bersifat asam jika senyawa tersebut melepas ion H +. hal ini berlaku untuk unsur M dengan energy ionisasi yang besar. M akan sukar melepas electron dan cenderung menggunakan electron bersama dengan O membentuk ikatan kovalen.. Beberapa hidroksida yang dimaksud adalah sebagai berikut: Si(OH) 4 -> H 2 SiO 3 + H 2 O. P(OH.

Persamaan reaksi dari kalsium hidroksida + asam klorida menghasilkan kalsium klorida dan air
Dari kedua contoh tersebut terlihat bahwa (1) asam Brønsted-Lowry harus mempunyai atom hidrogen yang dapat terlepas sebagai ion H +; dan (2) basa Brønsted-Lowry harus mempunyai pasangan elektron bebas yang dapat berikatan dengan ion H +.. Kelebihan definisi oleh Brønsted-Lowry dibanding definisi oleh Arrhenius adalah dapat menjelaskan reaksi-reaksi asam-basa dalam fase gas, padat.

Tuliskan Reaksi Ionisasi Senyawa Natrium Hidroksida Dan Asam Fosfat Belajar di Rumah
Berikut ini adalah 5 teori asam basa yang terus berkembang mengenai penggolongan suatu senyawa. 1. Teori Arrhenius. Konsep asam basa Arrhenius dikemukakan oleh Svante Arrhenius pada 1884, asam adalah suatu senyawa yang bila dilarutkan dalam air akan meningkatkan konsentrasi ion hidrogen ($\mbox{H}^{+}$) di atas nilainya dalam air murni.

Pasangan Asam Basa Konjugasi H2O + HNO2 YouTube
Pengertian zat amfoter. Istilah amfoter berasal dari Bahasa Yunani "amphoteros" atau "amphoteroi" yang berarti "masing-masing" atau "keduanya". Istilah tersebut digunakan karena zat atau senyawa amfoter adalah senyawa yang dapat bersifat asam sekaligus basa. Dilansir dari Encyclopedia Britannica, zat amfoter adalah suatu zat.
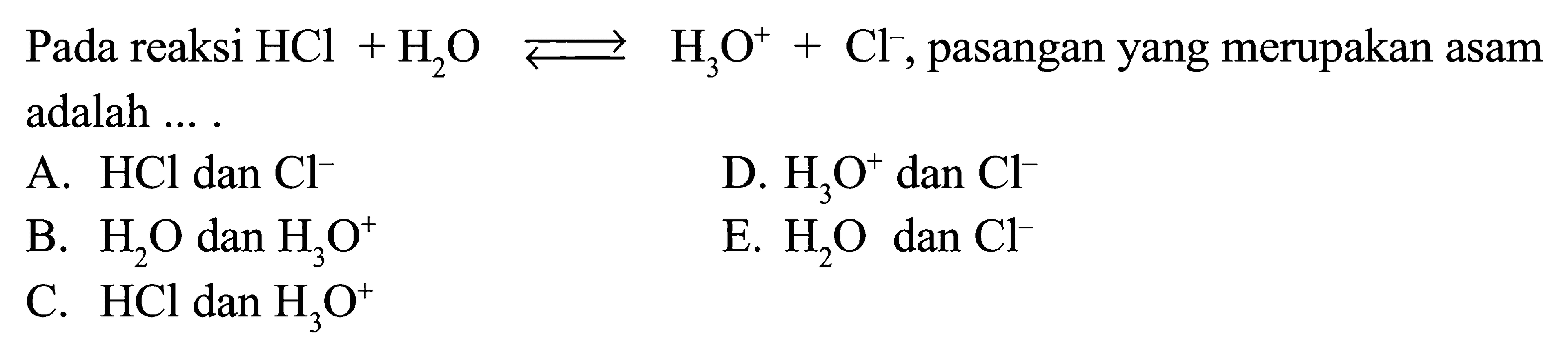
Tentukan asam dan basa menurut teori BronstedLowry dalam...
Sementara basa adalah zat yang menghasilkan ion hidroksida (OH-) dalam larutan. Asam dan basa dapat bereaksi menghasilkan air serta senyawa ionic garam. Reaksi itu disebut reaksi netralisasi. Asam dan basa merupakan dua jenis larutan yang kerap digunakan dalam kehidupan sehari-hari manusia. Asam dan basa ada yang memiliki sifat kuat dan juga lemah.

PPT TEORI ASAM DAN BASA PowerPoint Presentation, free download ID3560268
Asam dan basa adalah larutan elektrolit yang dikenal dengan ciri khasnya, seperti asam yang memiliki rasa masam dan basa yang memiliki rasa pahit. Asam dan basa pengertian menurut Kamus Besar Bahasa Indonesia (KBBI), asam adalah zat yang dapat memberikan proton, zat yang dapat membentuk ikatan kovalen dengan menerima sepasang elektron.

Pasangan persamaan reaksi hidrolisis yang bersifat basa adalah Universityku
Zat asam dan basa dijelaskan dalam teori oleh beberapa pakar kimia, di antaranya teori Arrhenius, Bronsted-Lowry, dan Lewis. Asam-basa adalah sifat kimiawi yang dimiliki oleh bahan makanan, minuman, obat-obatan, dan zat lainnya. Disebutkan dalam laman Sumber Belajar Kemdikbud, bahwa secara umum asam mempunyai rasa masam dan basa mempunyai rasa.

Cara Mencari Pasangan Asam Basa Menurut Teori Bronsted Lowry AsamBasa YouTube
Teori asam basa Bronsted-Lowry menjadikan transfer proton (H+) untuk menentukan sifat asam atau basa suatu senyawa. Definisi asam menurut Bronsted-Lowry adalah zat yang dapat menyumbangkan (donor) proton, sedangkan basa adalah zat yang dapat menerima (penerima donor) proton. Dilansir dari Khan Academy, asam mengandung hidrogen yang dapat.

20+ Contoh Soal Hidrolisis Asam Lemah Dan Basa Kuat Contoh Soal Terbaru
Pasangan hidroksida yang bersifat asam adalah#SoalKimia #KimiaKelas12 #KimiaUASBN Subscribe Channel : https://youtube.com/c/DwiPurwantoBlog : http://bit.ly/d.

Reaksi Kimia Asam Sulfat & Natrium Hidroksida 🌡 YouTube
Pengertian asam Mengutip laman emodul Kemdikbud, seorang ahli kimia Swedia bernama Svante August Arrhenius menyatakan bahwa asam merupakan senyawa elektrolit yang apabila larut dalam H2O (air) maka akan terionisasi menjadi ion hidrogen (H+) dan ion sisa asam yang bermuatan negatif. Reaksi kimianya adalah berikut: 1) HCl + air → H+ + Cl-2) CH3COOH + air → CH3COOH + H+

Contoh Asam Basa Dalam Kehidupan Sehari Hari
Hidroksida yang bersifat asam adalah senyawa kimia yang memiliki pH kurang dari 7. Contohnya adalah asam sulfat, asam nitrat, dan asam fosfat. Senyawa ini sering digunakan dalam industri untuk produksi pupuk, baterai, dan bahan kimia lainnya. Bahaya. Hidroksida yang bersifat asam sangat berbahaya bagi kesehatan manusia.

Pasangan hidroksida yang bersifat asam adalah YouTube
Hidroksida unsur periode ketiga yang bersifat basa adalah NaOH dan Mg (OH)2. NaOH bersifat basa kuat , Mg (OH)2 basa lemah. Jika keelektronegatifan unsur L besar, ikatan antar L dengan O kuat, sedangkan ikatan antara O dengan H lemah, maka ikatan O dengan H mudah putus dan terbentuk LO- dan H+ yang mengakibatkan LOH bersifat asam.

LENGKAP ‼️ Cara Mudah Menentukan Pasangan Asam Basa Konjugasi TeoriAsamBasa AsamBasaKonjugasi
Hidroksida adalah suatu ion poliatomik yang terdiri dari oksigen dan hidrogen (OH −). Ion ini bermuatan −1 dan merupakan salah satu ion poliatomik yang paling sederhana. Sebagian besar hidroksida tidak larut dalam air. Suatu kelompok basa yang mengandung hidroksida disebut basa hidroksida. Basa ini akan terdisosiasi di dalam air menjadi satu kation dan satu atau lebih ion hidroksida.