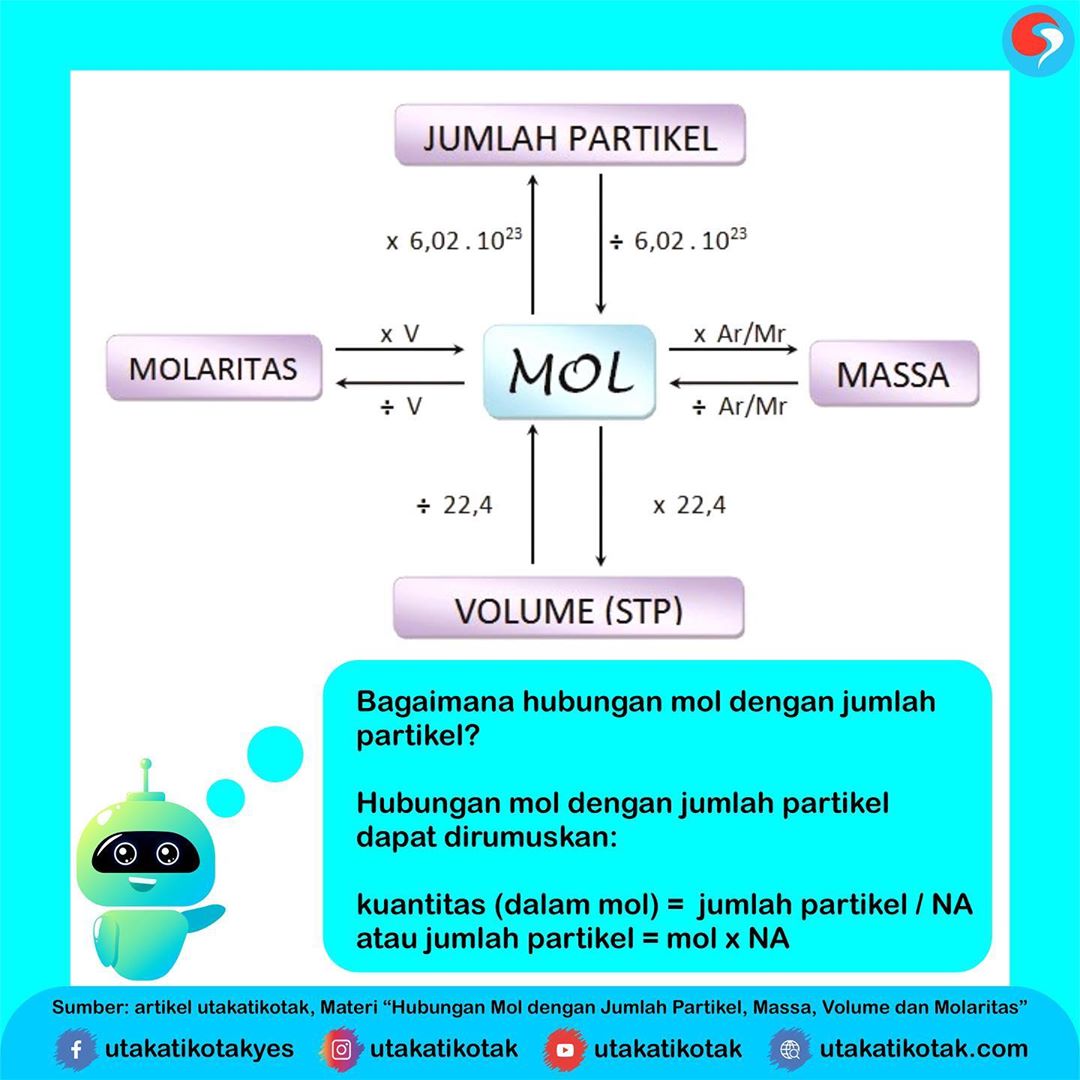
Hubungan Mol dengan Jumlah Partikel, Massa, Vo
Hitunglah jumlah partikel dan volume gas O 2 (Mr = 32) pada keadaan standar yang memiliki massa 16 gram. Jawaban: Untuk menghitung jumlah partikel pada keadaan standar, hubungkan dengan massa O 2 yang diketahui seperti berikut. jumlah partikel / 6,02 x 10 23 = massa / Mr.

2 Menghitung Mol dan Jumlah Partikel YouTube
Banyaknya partikel dinyatakan dalam satuan mol. Satuan mol sekarang dinyatakan sebagai jumlah patikel (atom, molekul, atau ion) dalam suatu zat. Para ahli sepakat bahwa satu mol zat mengandung jumlah partikel yang sama dengan jumlah partikel dalam 12,0 gram isotop C-12 yakni 6,02 x 1023 partikel.

LATIHAN SOAL STOIKIOMETRI (KONSEP MOL) MENGHITUNG JUMLAH PARTIKEL, MASSA, VOLUME, YouTube
Part 1 Cara menetukan mol jika massa senyawa /atom diketahuihttps://youtu.be/HeD_qhWjbdcPart 3https://youtu.be/vIApp9Cb7wMPembahasan lengkap mol https://yout.

Cara Menghitung Jumlah Atom Dalam Rumus Kimia Gini Caranya Hot Sex Picture
Sedangkan jumlah Avogadro adalah 6,022 x 10^23 partikel yang digunakan untuk menghitung jumlah partikel dalam suatu materi. Contoh Soal Menghitung Jumlah Partikel. Sebagai contoh, jika kita memiliki 0,5 mol karbon dioksida (CO2), kita dapat menghitung jumlah partikel (molekul CO2) menggunakan konsep jumlah Avogadro.

Tutorial Teori Gas Menghitung Jumlah Partikel YouTube
Jumlah partikel atom = 2 mol x 6,022 x 10^23 partikel/mol. Dalam contoh di atas, jumlah partikel atom dalam 2 mol atom hidrogen adalah sebanyak 1,2044 x 10^24 partikel atom. Paham akan konsep mol dan menghitung jumlah partikel atom dalam mol, kita dapat mengukur dan memahami jumlah partikel atom dalam suatu zat secara lebih akurat.

Rumus Jumlah Partikel
Jawab: a) Gas O2 adalah unsur diatomik dengan partikel berupa molekul unsur. b) Banyaknya mol O2 yang mengandung 1,505 × 1023 partikel dapat kita hitung dengan menggunakan rumus berikut. Jumlah partikel = mol × N. mol = Jumlah partikel/N. mol = 1,505 × 1023/6,02 × 1023. mol =1,505/6,02. mol = 0,25 mol.

Latihan Soal Kimia Hubungan Mol Dengan Jumlah Partikel Dan Menghitung Massa Molekul Relatif PDF
Step : Menghitung jumlah partikel. Mol = jumlah partikel / 6.022*10 23. Maka. Jumlah partikel = Mol x 6.022*10 23. Jumlah partikel = 0.05 mol x 6.022*10 23 = 3.011*10 22 partikel. Nah, demikianlah materi yang menjelaskan tentang pengertian konsep mol, perhitungan dan contoh soal konsep mol beserta jawabannya. Semoga melalui artikel ini dapat.

Menghitung Jumlah Partikel Zat YouTube
Langkah kedua, menghitung jumlah partikel dengan konsep hubungan mol dengan bilangan avogadro dan jumlah partikel: Jadi, jumlah partikelnya adalah . Perdalam pemahamanmu bersama Master Teacher di sesi Live Teaching, GRATIS! 146. 4.5 (8 rating) LA. Laili Anwar. Makasih ️. dn. dwidwi nessa. Mudah dimengerti.

Latihan Soal Stoikiometri Konsep Mol Menghitung Jumlah Partikel Images and Photos finder
Hubungan Mol dengan Jumlah Partikel. Seperti yang udah kalian tahu nih, 1 mol menyatakan banyaknya partikel dalam suatu zat, yang mana jumlahnya sama dengan jumlah partikel dalam 12 g atom C-12. Berdasarkan penelitian pak Avogadro diketahui nih kalau dalam 1 mol atau 12 g atom C-12 terkandung 6,02 x 10²³ partikel. Bilangan ini kemudian.

4.A. Jumlah partikel C4H10? B. Massa gas CO2? C. Mol air H2O? D.Volume H2O?5. Berapakah mol
Satu mol menunjukkan banyaknya partikel yang terkandung dalam suatu zat yang jumlahnya sama dengan jumlah partikel dalam 12 gram atom C-12. Memang, ada berapa sih partikel dalam 12 gram atom C-12? Seorang ilmuwan bernama Avogadro berhasil menghitung banyaknya partikel dalam 12 gram atom C-12, yaitu sebanyak 6,02 × 10 23 partikel. Sungguh.

cara menghitung jumlah atom dalam rumus kimia menghitung jumlah atom kimia kelas 10 SMA
a: Nomor atom merupakan jumlah proton. Saat netral (tidak bermuatan) akan sama dengan jumlah elektron. b: Nomor massa melambangkan jumlah proton ditambah jumlah neutron atau disebut juga jumlah nukleon. c: Muatan/bilangan oksidasi (biloks) terdiri dari melepas elektron (positif) dan menangkap elektron atau bertambah (negatif). Keterangan.

Jumlah partikel dalam 0,25 mol N2 sama dengan jumlah partikel dalam Mas Dayat
Jika tetapan Avogadro = L, banyaknya atom Nitrogen yang terkandung dalam 1 gram gas Nitrogen adalah…. Jawaban: Tentukan jumlah mol (n) dalam 1 gram Nitrogen: n = massa N : Mr N. = 1 gram : 14. = 0,71 mol. Tentukan banyak partikel (X) Natrium dalam 0,71 mol konsentrasinya: X = n x L. = 0,071 x 6,02x10^23.

Contoh soal menghitung jumlah partikel winschemistryclass TikTok Video
satuan mol dengan jumlah partikel: n = jumlah partikel 6,02 ×1023. Jumlah partikel =n × 6,02 ×1023. Soal-1. Dalam 0,1 mol H 2 SO 4, tentukan: a. jumlah partikel H 2 SO 4. b. jumlah atom H, S, dan O. c. jumlah ion H + dan ion SO 42-. Klik untuk melihat bahasan soal ini.

HUBUNGAN ANTARA MASSA, JUMLAH MOL, DAN JUMLAH PARTIKEL
Konsep mol dan hubungannya dengan jumlah partikel, massa molar, volume molar, dan molaritas dapat kita gambarkan sebagai berikut. Konsep mol digunakan untuk menghitung jumlah partikel yang ada di dalam suatu zat apapun menggunakan satuan mol. Nilai mol dinyatakan dalam tetapan avogadro yang dinotasikan dengan L. L = 6,02 x 10 23 partikel 1.

Hubungan Mol Jumlah Partikel Massa Volume (STP) YouTube
Contoh Soal Konsep Mol Beserta Jawabannya. 1. Sebanyak 4,9 gram H2SO4 H 2 SO 4 dilarutkan dalam air sehingga diperoleh 500 mL larutan. Tentukan jumlah ion yang yang terlarut dalam larutan dan tentukan konsentrasi ion H+ H +. Jawaban contoh soal konsep mol dan penyelesaiannya. nH2SO4 = m Mr = 4, 9 98 = 0, 05 mol n H 2 SO 4 = m M r = 4, 9 98 = 0.
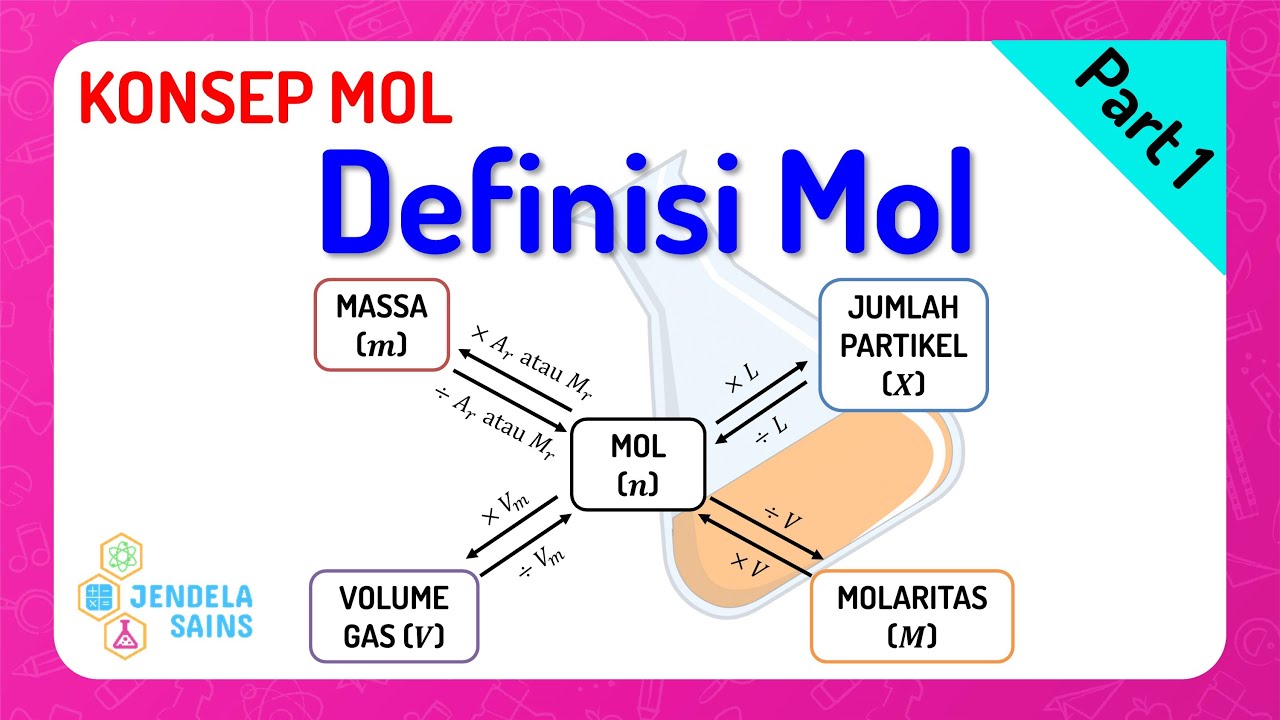
Konsep Mol Kimia Kelas 10 • Part 1 Hubungan Mol & Massa, Jumlah Partikel, Volume Gas, Molaritas
Konsep Mol Mol adalah satuan dasar SI (Satuan Internasional) yang mengukur jumlah zat. Jika Anda telah mempelajari atom, molekul dan ion sebagai partikel-partikel materi. Bagaimana caranya menghitung jumlah yang sangat banyak dari partikel-partikel materi yang berukuran sangat kecil tersebut? Untuk menyederhanakan jumlah partikel yang sangat kecil ini digunakan istilah MOL.