
PPT Reaksi oksidasi reduksi PowerPoint Presentation, free download ID924292
Cara Menentukan Reaksi Reduksi dan Oksidasi (Redoks) Dengan Berdasarkan Konsep Kenaikan dan Penurunan Bilangan Oksidasi. Pada reaksi reduksi dan oksidasi (redoks), ada beberapa unsur yang bertindak sebagai reduktor dan oksidator. Dimana, zat yang mengalami oksidasi tersebut dinamakan reduktor, sementara itu zat yang mengalami reduksi dinamakan.

LENGKAP ‼️ MENENTUKAN OKSIDATOR, REDUKTOR, HASIL OKSIDASI DAN HASIL REDUKSI YouTube
Contoh Soal Reduktor dan Oksidator. 1. Tentukan reduktor dan oksidator, hasil oksidasi, dan hasil reduksi pada reaksi redoks berikut ini: 2KMnO4 + 5H2C2O4 + 3H2SO4 → K2SO4 + 2MnSO4 + 10CO2 + 8H2O. 2KMnO 4 + 5H 2 C 2 O 4 + 3H 2 SO 4 → K 2 SO 4 + 2MnSO 4 + 10CO 2 + 8H 2 O.

Cara Cepat Menentukan Reduktor, Oksidator, Hasil Reduksi, dan Hasil Oksidasi Reaksi Redoks
Berikut ini deret unsur non logam yang bersifat reduktor kuat sampai oksidator kuat ! Si, B, As, P, C, Se, S, I, Br, N, Cl, O, F Unsur Si merupakan unsur yang bersifat reduktor kuat sedangkan unsur F merupakan unsur yang bersifat oksidator kuat. Terakhir, mari kita ulik faktor-faktor yang menentukan kekuatan oksidator dan reduktor dari senyawa.

MENENTUKAN OKSIDATOR DAN REDUKTOR PADA SUATU REAKSI REDOKS YouTube
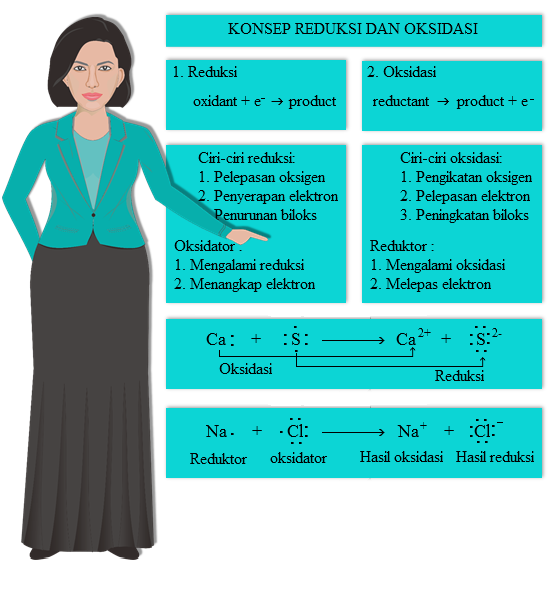
Dalam kata lain, oksidator adalah zat yang mengalami reduksi dan reduktor adalah zat yang mengalami oksidasi. Sebelum menentukan oksidator dan reduktor, kita harus mengetahui terlebih dahulu bilangan oksidasi masing-masing unsur dalam reaksi yang memungkinkan terjadi perubahan biloks. Fe +H2SO4 → Fe2(SO4)3 +H2. Biloks Fe pada Fe = 0.

cara cepat menentukan Reduktor dan Oksidator YouTube
Sebelumnya telah dibahas mengenai cara menentukan bilangan oksidasi. Anda dapat memeriksa artikel terkait untuk membaca artikel sebelumnya. Pada kesempatan ini kita akan membahasa beberapa contoh soal latihan tentang menentukan oksidator, reduktor, hasil reduksi, dan hasil oksidasi. Pada halaman paling bawah disajikan ringkasan konsep reaksi.

Menentukan Oksidator, Reduktor, Hasil Reduksi Serta Oksidasi Pada Reaksi Redoks LatihanSoal
Ciri-ciri Reaksi Redoks. 1. Ada unsur bebas misalnya Cl2 (Klorin), Cu (Cuprum), dan O2 (Oksigen). 2. Terjadi perubahan biloks (bilangan oksidasi). 3. Ada reduktor (pereduksi) adalah suatu zat yang mengalami oksidasi. 4. Ada oksidator (pengoksidasi) adalah suatu zat yang mengalami reduksi.
Tentukan reduktor, oksidator, hasil oksidasi, dan
Halo adik-adik, di video kali ini @5NChemistry hadir membawakan video tentang bagaimana cara menentukan oksidator reduktor, hasil oksidasi dan hasil reduksi.
MENENTUKAN REDUKTOR, OKSIDATOR, HASIL REDUKSI DAN OKSIDASI
Dalam reaksi redoks terdapat istilah oksidator dan reduktor. Oksidator adalah zat yang menyebabkan zat lain mengalam reaksi oksidasi sedangkan dirinya sendiri mengalami reaksi reduksi.. Dengan nilai pH dapat menentukan keasaman air, pH < 7 menunjukkan air bersifat asam, pH > 7 menunjukkan air bersifat basa dan pH=7. Tumbuhan dan hewan air.

Menentukan Apakah Suatu Reaksi Termasuk Reaksi Redoks ( Oksidator, Reduktor) Kelas X YouTube
Ada 8 aturan dalam menentukan bilangan oksidasi suatu unsur, di antaranya: 1. Bilangan oksidasi unsur bebas adalah 0. Unsur bebas adalah unsur yang tidak bergabung atau berikatan secara kimia dengan unsur lain. Unsur bebas terbagi menjadi dua, yaitu unsur bebas berbentuk atom, seperti C, Ca, Cu, Na, Fe, Al, Ne dan unsur bebas berbentuk molekul.

Contoh soal menentukan oksidator dan reduktor
Dalam reaksi redoks terdapat istilah reduktor dan oksidator. Reduktor adalah spesi yang akan mereduksi spesi (bisa berupa molekul, ion, atau atom) lain / spesi yang mengalami oksidasi.. Terdapat aturan untuk menentukan bilangan oksidasi dalam senyawa, seperti unsur bebas memiliki bilangan oksidasi 0, H memiliki bilangan oksidasi +1 (kecuali.

PPT Reaksi oksidasi reduksi PowerPoint Presentation, free download ID924292
Pengertian Oksidator dan Reduktor. Oksidator adalah senyawa yang memiliki kemampuan untuk mengoksidasi senyawa lain atau biasa dikenal senyawa menerima elektron. Oksidator adalah senyawa yang memiliki unsur dengan bilangan oksidasi tinggi seperti. H2O2, MnO4-, CrO3, Cr2O72-, OsO4, atau senyawa yang sangat elektronegatif.

PPT Reaksi oksidasi reduksi PowerPoint Presentation, free download ID924292
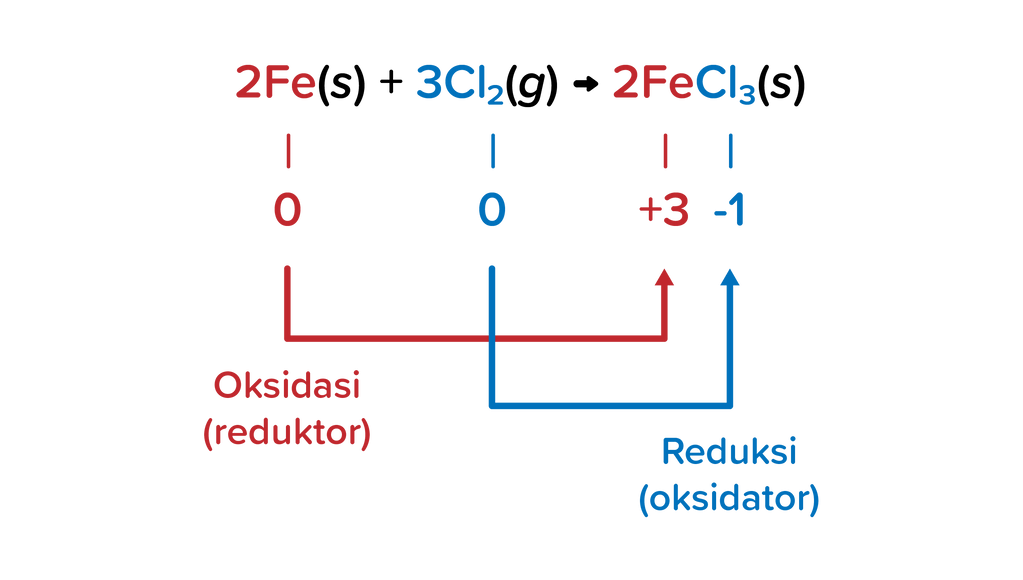
Menentukan Reaksi Reduksi dan Oksidasi Berdasarkan Konsep Kenaikan dan Penurunan Bilangan Oksidasi. Pada reaksi redoks, terdapat unsur-unsur yang bertindak sebagai reduktor dan oksidator. Zat yang mengalami oksidasi itu disebut reduktor, sedangkan zat yang mengalami reduksi disebut oksidator. Coba perhatikan contoh berikut ini!

Tentukan oksidasi, reduksi, oksidator dan reduktor dari p...
Assalamu'alaikum warahmatullahi wabarakatuh.Hai, semua!Selamat datang di channel Cerdas Kimia.Kali ini channel cerdas kimia menyajikan video tentang materi k.

Konsep Mudah Menentukan Reduksi, Oksidasi, Reduktor dan Oksidator pada Reaksi Kimia SMA YouTube
Cara membaca diagram Frost, menentukan spesi paling stabil dan menentuan spesi yang berperan sebagai reduktor-okisdator paling kuat. Cara Membaca Diagram Frost, Kestabilan Bilangan Oksidasi, Oksidator dan Reduktor Terkuat - Urip dot Info

Menentukan Oksidator Dan Reduktor PDF
Dalam reaksi redoks (reduksi dan oksidasi) dikenal adanya istilah reduktor dan oksidator. Reduktor adalah zat yang menyebabkan zat lain mengalami reduksi, se.

Cara menentukan Reduktor dan Oksidator YouTube
Oke, kita lanjut ya bahasannya! Pada reaksi redoks, terdapat unsur-unsur yang bertindak sebagai reduktor dan oksidator. Zat yang mengalami oksidasi itu disebut reduktor, sedangkan zat yang mengalami reduksi disebut oksidator. Coba perhatikan contoh berikut ini, ya! Reaksi: Mg(s) + 2HCl -----> MgCl2(aq) + H2(g) Karena Mg merupakan unsur bebas, jadi biloks Mg = 0.