
Kumpulan Soal Dan Pembahasan Kimia Kesetimbangan Reaksi Kelas 11
Untuk menentukan koefisien reaksi, maka reaksi harus setara. Persamaan reaksi dikatakan sudah setarajika zat-zat yang terlibat dalam reaksi antara ruas kiri dan ruas kanan sudah setara jumlah maupun muatannya. Penulisan persamaan reaksi harus mengikuti hukum Kekekalan Massa (jumlah zat), hukum Perbandingan Tetap (rumus kimia), serta sifat-sifat.

Soal Stoikiometri Reaksi (Pereaksi Pembatas) Urip dot Info
Dalam menentukan koefisien reaksi, jika tidak ada nomor pada bagian sebelah kiri senyawa atau zat kimia, maka koefisien reaksi tersebut akan dianggap 1. Hal seperti itu sudah menjadi ketentuan pasti dalam persamaan reaksi. Jadi, ketika kamu ingin menulis persamaan reaksi, maka harus dipastikan bahwa keempat hal itu harus ada. Jika, salah satu.

Persamaan Reaksi Penyetaraan Reaksi dan menentukan angka Koefisien (bag ke 1) Chemie
Koefisien reaksi menyatakan jumlah partikel dari setiap pereaksi dan produk reaksi. Contoh persamaan reaksi kimia adalah. 2Na (s) + Cl 2 (g) -> 2NaCl (s) Koefisien reaksi Na = 2. Koefisien reaksi Cl = 1. Koefisien reaksi NaCl = 2. Pada contoh di atas, 2 molekul Na bereaksi dengan 1 molekul Cl 2 menghasilkan 2 molekul NaCl.

Menunjukkan Apa Koefisien Dalam Suatu Persamaan Reaksi pemakaian masker spirulina
Hasil mol koefisien HCl < Fe, sehingga HCl sebagai pereaksi pembatas. Selanjutnya jumlah mol dari limiting reagent inilah yang menentukan jumlah mol reaksi/hasil reaksi. Misal dari contoh soal tersebut ditanyakan massa FeCl2 yang terbentuk, sehingga. nFeCl2 = 1 2 × mol HCl = 1 2 × 0, 1 mol = 0, 05 mol mFeCl2 = 0, 05 × 127 gram = 6, 35 gram.

Setarakan persamaan reaksi redoks berikut menggunakan car...
Koefisien reaksi adalah bilangan yang berada di sebelah kiri unsur, sedangkan indeks reaksi adalah bilangan yang terletak di sebelah kanan bawah unsur. Perhatikan contoh berikut reaksi pembentukan amonia berikut.. Sebelum menentukan jumlah mol gas CO 2, Quipperian harus mencari persamaan reaksi yang sudah setara berdasarkan keterangan pada.

Menentukan Orde Reaksi Laju reaksi kimia kelas 11 YouTube
Persamaan yang menunjukkan perubahan zat sebelum dan sesudah reaksi kimia yang dinyatakan dengan rumus kimia, koefisien reaksi dan wujud zat.. Tuliskan persamaan suatu reaksi antara larutan perak nitrat dengan larutan kalsium klorida menghasilkan endapan perak klorida dan larutan kalsium nitrat. Jawaban. Reaktan: perak nitrat : $\mbox{AgNO.

XI.4.e. Laju Reaksi dan Koefisien Reaksi (Teori) YouTube
Persamaan reaksi dapat dibuat seimbang dengan cara memberikan suatu bilangan yang dinamakan koefisien reaksi. Koefisien reaksi diletakkan di depan rumus kimia senyawa, molekul, atau unsur. Di dalam persamaan reaksi di atas, oksigen kekurangan 1 atom pada produk sehingga kita dapat meletakkan angka 2 sebagai koefisien di depan MgO.

Koefisien reaksi atau nilai a, b, c, dan d dari persamaan...
Seperti terlihat, tidak ada hubungan antara koefisien stoikiometri reaksi dengan orde masing-masing pereaksi, dimana orde ini hanya dapat ditentukan melalui eksperimen.. Menentukan Persamaan Laju Reaksi. Persamaan laju suatu reaksi tidak memiliki hubungan dengan stoikiometri reaksi, tetapi ditentukan melalui percobaan, salah satu metode yang.
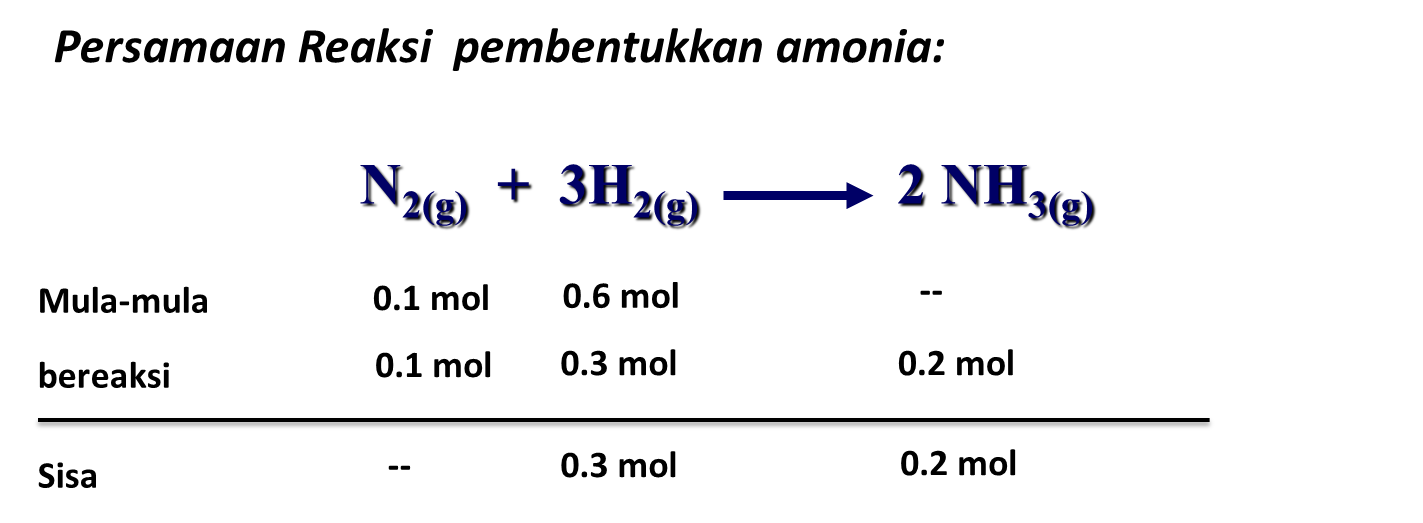
Koefisien Reaksi Dan Indeks Perhatikan Dan Lengk My XXX Hot Girl
Menentukan koefisien reaksi berdasarkan pembentukan endapan dan perubahan temperatur 2. Menentukan hasil reaksi berdasarkan konsep mol II. TEORI Ilmu kimia adalah ilmu yang mempelajari tentang materi dan perubahan materi baik secara fisik maupun materi. Pada prinsifnya materi terbagi menjadi tiga wujud yaitu padat, cair, dan gas.
Video belajar Hubungan Laju Reaksi dengan Koefisien Reaksi Kimia untuk Kelas 12
Dalam persamaan reaksi, dikenal koefisien reaksi, yaitu bilangan yang berada di sebelah kiri rumus kimia untuk mengalikan jumlah semua atom dalam rumus kimia tersebut. Contoh: 2SO 3 menunjukkan terdapat 2 molekul SO 3. Perbandingan koefisien-koefisien reaksi menunjukkan perbandingan mol zat-zat yang bereaksi dalam reaksi kimia tersebut.

Persamaan reaksi redoks Cu+aNO3^+bH^+> cCu^(2+)+dNO+4H...
Jawaban: Reaksi: Kita misalkan c= 1. Jumlah Al kanan= 2, maka Al di kiri harus 2, sehingga a= 2. Jumlah O di kanan= 3, maka O di kanan =3/2, sehingga b= 3/2. (keseluruhan reaksi kita kalikan 2) Maka, jawaban yang tepat adalah A. Baca Juga: Larutan Senyawa Ionik dan Kovalen - Materi Kimia Kelas 10. Yeay, akhirnya selesai juga materi tentang.

Cara Menentukan Koefisien Reaksi Kumpulan Cara Terbaru 37584 Hot Sex Picture
Menyetarakan persamaan reaksi adalah kemampuan yang harus kalian miliki sebelum melangkah ke bab stoikiometri dan konsep mol. Soal ini dapat keluar di soal u.

Cara Menentukan Orde Reaksi Dan Persamaan Laju Reaksi Dari Tabel Sexiz Pix
Apakah Anda ingin belajar kimia dasar dengan mudah dan menyenangkan? Tonton video ini untuk mempelajari cara mencari koefisien persamaan reaksi kimia dengan metode sederhana dan efektif. Video ini.
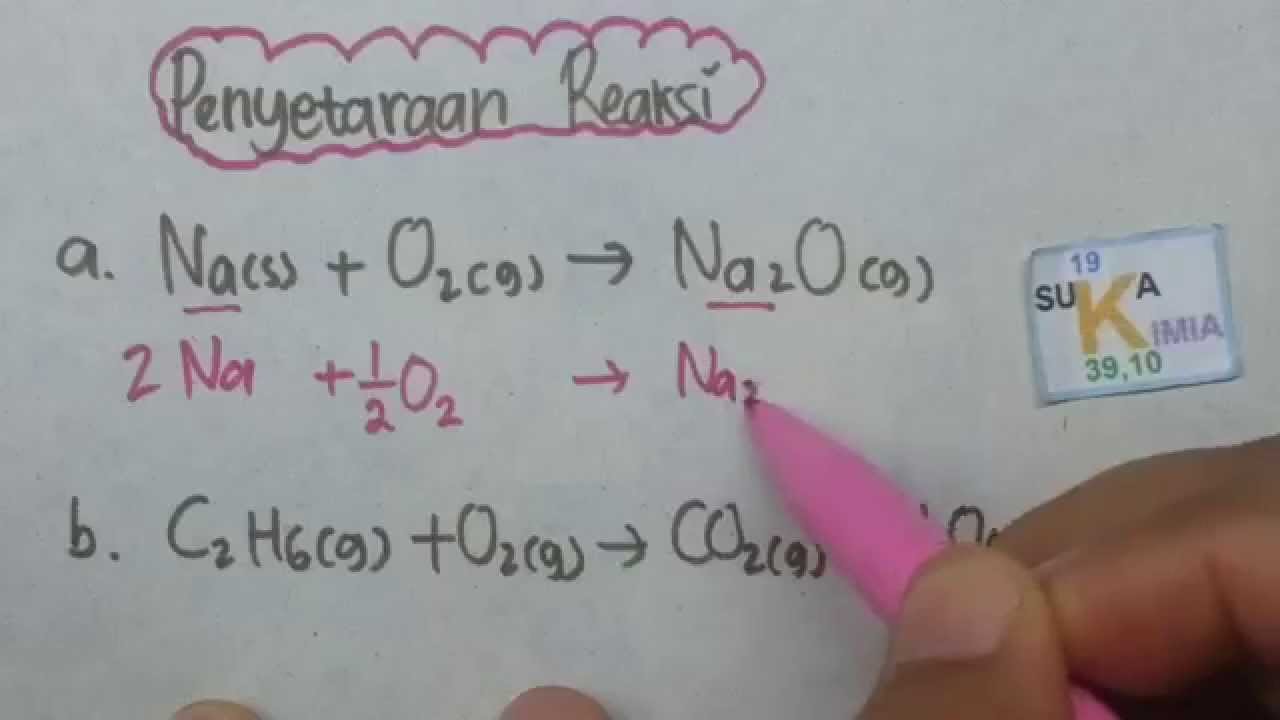
Contoh Soal Persamaan Reaksi Kimia Dan Jawabannya Contoh Soal Terbaru
1. Jika tahap-tahap reaksi elementer diketahui, maka orde reaksi sama dengan koefisien reaksi tahap paling lambat 2. Jika tidak diketahui tahap-tahap elementernya, maka orde reaksi ditentukan melalui eksperimen. Contoh persamaan laju reaksi berdasarkan hasil eksperimen adalah: • Reaksi kimia H2(q) + I2(q) → 2HI(q)

Cara Cepat menentukan Laju Reaksi Konsep Dasar tabel MTS YouTube
Berdasarkan penangkapan atau pelepasan oksigen. Oksidasi: reaksi yang melibatkan penangkapan atom oksigen. Contoh: C+ O2 → CO2. Atom C (karbon) mengalami oksidasi karena dalam reaksi atom karbon mengikat atom oksigen menjadi CO2. Reduksi: reaksi yang melibatkan pelepasan atom oksigen. Contoh: H2O2 → H2O + O2.

Cara Mudah Menentukan Penyetaraan Reaksi Kimia Kimia SMA YouTube
3. Koefisien reaksi. Koefisien reaksi adalah angka di depan unsur, molekul, senyawa, ataupun ion yang berfungsi menyetarakan atom-atom sebelum dan sesudah reaksi. Contohnya, angka 3 dan 2 yang terdapat pada persamaan reaksi N 2(g) + 3H 2(g) → 2NH 3(g). 4. Angka indeks. Angka indeks adalah angka yang terdapat pada bagian bawah atau belakang.