
Unsur yang Paling Mudah Melepas Elektron YouTube
Pembahasan. Kecenderungan suatu atom untuk melepaskan elektron dapat dilihat dari nilai energi ionisasinya. Energi ionisasi (EI) adalah energi yang dibutuhkan untuk melepaskan 1 elektron dalam keadaan gas. Nilai energi ionisasi dapat dipengaruhi oleh nomor atom. Bertambahnya nomor atom dalam satu periode dari kiri ke kanan menunjukkan semakin.
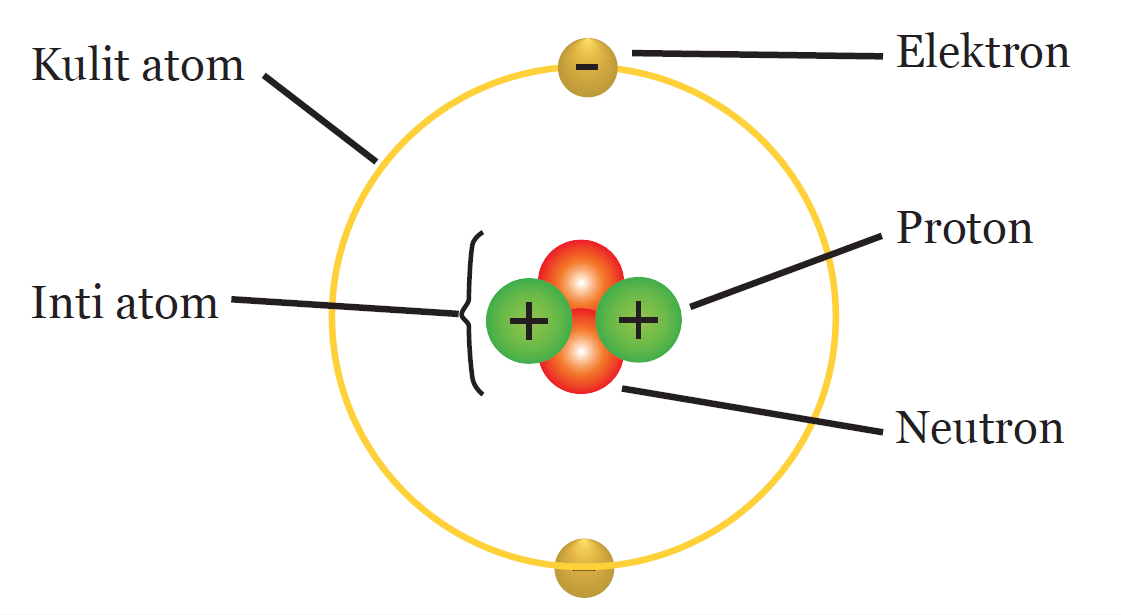
Partikel penyusun inti atom adalah Pasadena
Kestabilan ini bisa didapatkan dengan cara mendapatkan atau melepas elektron. Menurut Kossel dan Lewis, kestabilan atom ditentukan berdasarkan susunan atau konfigurasi elektron. Konfigurasi elektron akan stabil jika elektron terluarnya 2 (duplet) atau 8 (oktet). Hanya gas mulia yang memiliki konfigurasi elektron seperti ini.

Soal Sma X Melepas Dan Menerima Elektron Plus Atau Minus 2 Q2 = 12μc = 12 x 10−6 c
Baca baik-baik ya! —. 1. Pengertian. Ikatan ion terjadi akibat adanya serah terima elektron sehingga membentuk ion positif dan ion negatif yang konfigurasi elektronnya sama dengan gas mulia. Ion positif dan ion negatif diikat oleh suatu gaya elektrostatik. Senyawa yang dihasilkan disebut senyawa ion.

Prinsip Pembentukan Molekul dan Ion Ion dan Ikatan Ion, IPA Kelas 9 SMP Halaman 1 Kids
Yuk, pelajari konsep dasar reaksi redoks (reduksi-oksidasi) berdasarkan pelepasan dan pengikatan oksigen, perpindahan (transfer) elektron, dan perubahan bilangan oksidasi (biloks) dengan membaca artikel berikut! Di kehidupan sehari-hari, kita banyak menemukan fenomena-fenomena yang melibatkan reaksi kimia.

Trik Super Kilat Memahami Keelektronegatifan
2Na → 2Na + + 2e - (oksidasi) Cl 2 + 2e - → 2Cl - (reduksi) Jadi jumlah transfer elektron atau perubahan bilangan oksidasi yang terjadi pada reaksi tersebut sama dengan 2. Pada contoh-2, jumlah elektron yang dilepas H 2 = 2, dan jumlah elektron yang diterima O 2 = 4, tampak bahwa jumlah elektron yang dilepas tidak sama dengan jumlah.
√ Apabila Suatu Unsur Melepas Elektron Maka Wanjay
Atom dapat melakukan transfer elektron (melepas/menerima elektron) melalui cara berikut: Menambah elektron agar elektron terluar menjadi 8. Melepas semua elektron terluar (elektron valensi) Adanya proses transfer elektron menyebabkan terbentuk ion positif atau ion negatif. Unsur golongan IA, IIA, IIIA akan cenderung melepaskan elektron.

Bagaimanakah tahapan Rantai Transfer Elektron dan Kemiosmosis? YouTube
Pada kenyataannya, Reaksi Reduksi Oksidasi melepas dan menerima elektron berlangsung secara bersamaan. Ketika sebuah zat mengalami oksidasi dengan cara melepaskan elektron, zat lain dalam reaksi akan menerima elektron tersebut sehingga mengalami reduksi. Contoh Konsep Pelepasan dan Penerimaan Elektron Reaksi Redoks: 1.
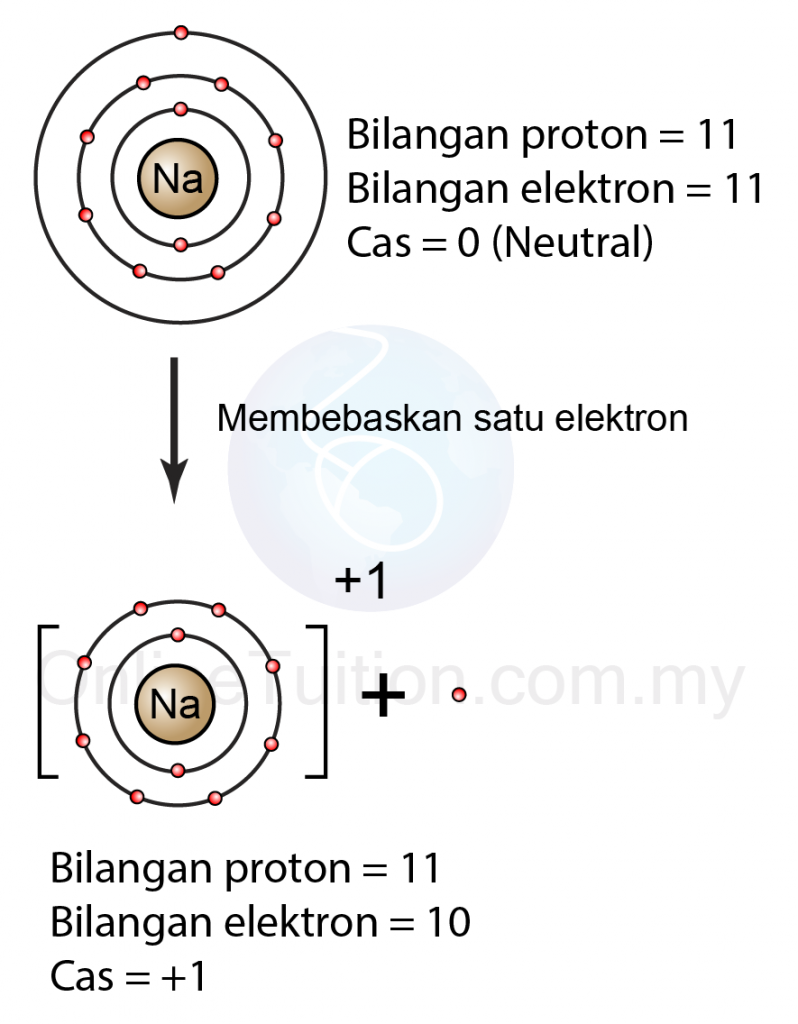
Pembentukan Ion Kimia SPM
Saat kulit elektron terluar terisi penuh, unsur tersebut akan sulit untuk melepas maupun menerima elektron dari lingkungan sehingga stabil dan tidak mudah bereaksi. Baca juga: Menghitung Reaksi antara Asam Nitrat dan Gas Amonia . Untuk atom yang memiliki elektron valensi lebih atau kurang dari 8, maka atom tersebut akan berikatan dengan atom lain.
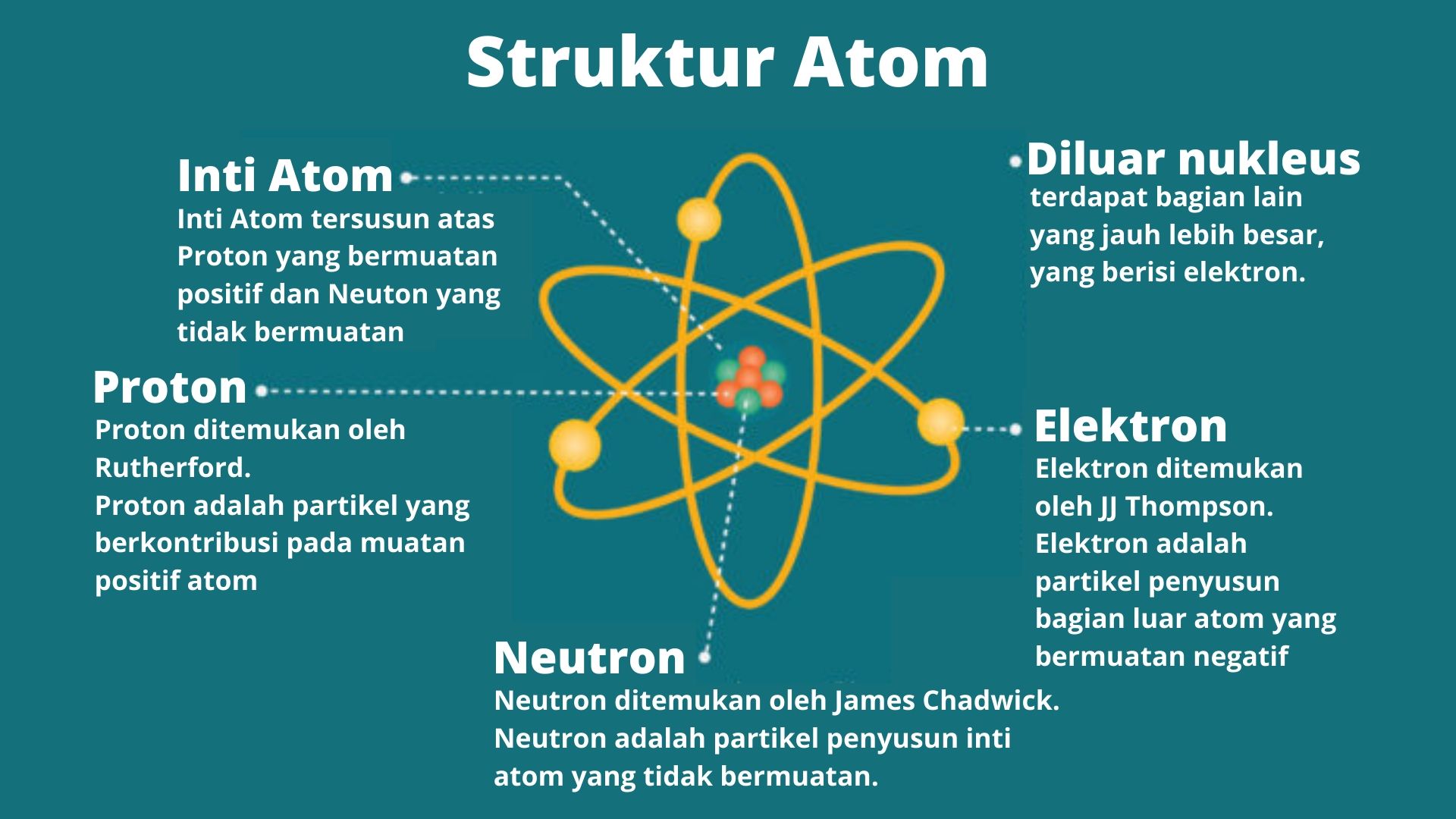
Struktur Atom Pengertian Rumus Dan Contoh Soal Dalam Kimia Jumankera Sexiz Pix
Sebagian atom cukup sulit melepas dan menerima elektron, untuk itu mereka perlu energi besar untuk memprosesnya. Maka terbentuklah konfigurasi elektron dimana atom saling berikatan lewat pemakaian pasangan elektron bersama yang terjadi pada atom nonlogam. Ikatan tersebut yang kita kenal dengan ikatan kovalen.
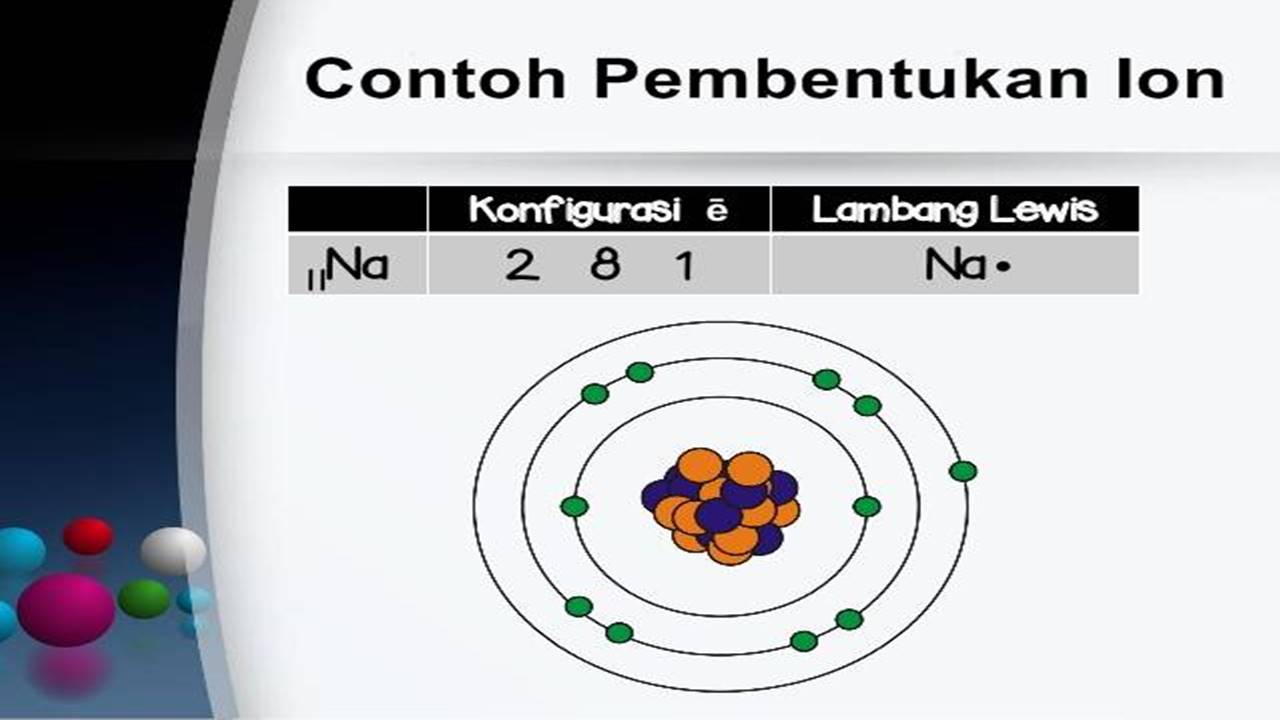
Pembentukan Ion
Pembahasan. Atom logam cenderung melepaskan elektron karena memiliki energi ionisasi yang kecil, sementara atom nonlogam cenderung menerima elektron karena memiliki afinitas elektron yang besar. Kecenderungan atom melepaskan atau menerima elektron dipengaruhi energi ionisasi dan afinitias elektron atom tersebut.

PPT Materi Minggu ke3 IKATAN KIMIA PowerPoint Presentation, free download ID7082311
Terbentuknya ikatan kimia antar unsur terjadi karena adanya interaksi antar unsur yang saling melepas dan menerima elektron valensi atau membentuk pasangan elektron bersama. Gambaran terbentuknya ikatan kimia digambarkan dengan notasi yang disebut Struktur Lewis. Struktur Lewis dilambangkan dengan memberikan titik (.) atau silang (x) di sekitar lambang atom.
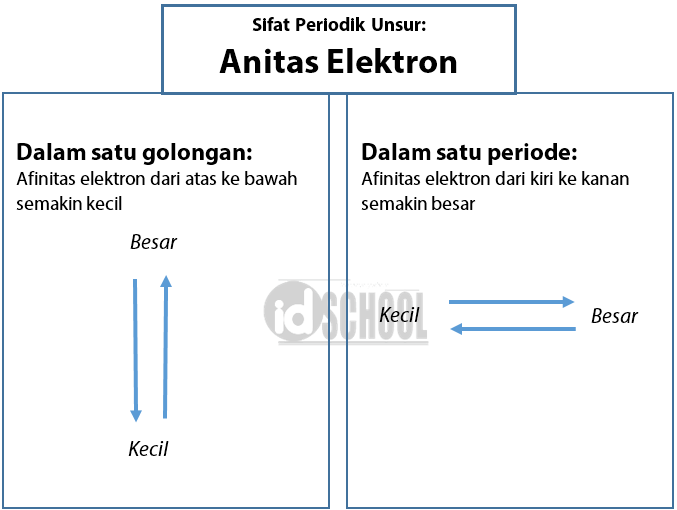
Sifat Keperiodikan Unsur Titik Leleh Dan Titik Didih Berbagai Unsur
Untuk mencapai kestabilan, suatu unsur dapat melepas dan menerima elektron pada kulit terluarnya melalui pembentukan ikatan kimia. dengan menggambarkan struktur lewisnya. Atom yang berikatan akan menggunakan elektron vasensinya masing-masing, sehingga berikatan menjadi susunan yang sempurna atau stabil dan memenuhi kaidah oktet.
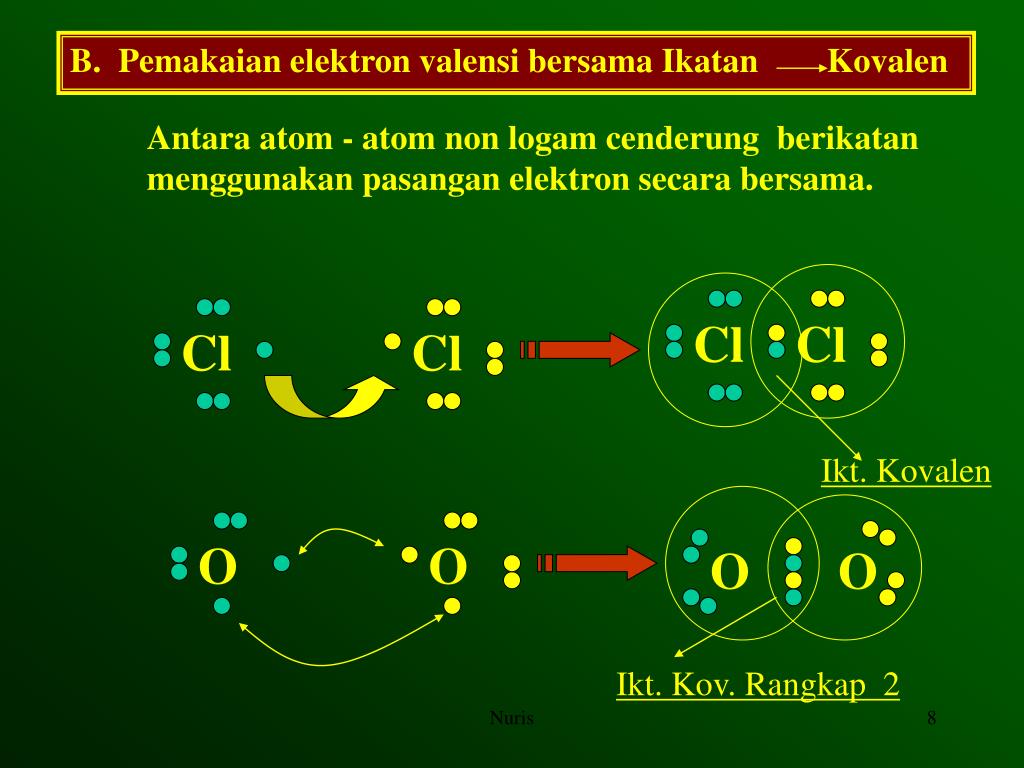
PPT IKATAN KIMIA PowerPoint Presentation, free download ID5631507
melepas dan menerima elektron Berdasarkan sifatnya, dalam sifat keperiodikan unsur, unsur atau atom dapat dibagi menjadi 3, yaitu unsur logam dan non logam serta metalloid.

Lihatlah Gambar Berikut Gambar Yang Menunjukkan Aliran Elektron Adalah serat
Pelepasan elektron menghasilkan ion positif dan penyerapan elektron menghasilkan ion negatif. Peristiwa terlepas atau masuknya ion pada sebuah atom disebut ionisasi . Contohnya, ketika atom natrium (Na) melepas satu elektron, maka akan membentuk ion Na + , atau ketika atom klorin (Cl) menerima 1 elektron, maka akan membentuk ion Cl - .

Cara Konfigurasi Elektron Anion Fluor "9F" (Cara Mekanika Kuantum) YouTube
HNO 3 adalah asam.HNO 3 melepas proton (H+) menjadi NO 3 - yang merupakan basa konjugasi. H 2 O adalah basa.H 2 O menerima proton (H+) menjadi H 3 O + yang merupakan asam konjugasi.. Maka, HNO 3 dan NO 3 - merupakan pasangan asam basa konjugasi. Serta, H 2 O dan H 3 O + merupakan pasangan asam basa konjugasi. [inline_ads] 3. Zat Amfoter. Zat amfoter adalah suatu zat yang berperan sebagai.

Atom,ion dan molekul
Hal ini dapat dilakukan dengan dua cara yaitu dengan melepas atau menerima elektron, tergantung dengan kecenderungan dalam kemudahan dan kesulitan unsur tersebut menarik dan melepas elektron. Untuk unsur yang bersifat logam, dalam suatu periode dari kiri ke kanan akan semakin kurang reaktif namun dalam suatu golongan dari atas ke bawah akan.