
Menghitung Massa Atom Relatif (Ar) YouTube
Massa atom dan massa molekul relatif sangat kecil sehingga sulit untuk diukur, namun para ilmuan menemukan bahwa massa suatu atom dapat diukur dengan membaningkannya dengan massa atom lain. Massa Atom Relatif; Massa atom relatif atau Ar adalah massa suatu atom yang didapat dari rasio perbandingan standarnya. Dilansir dari Encyclopaedia.
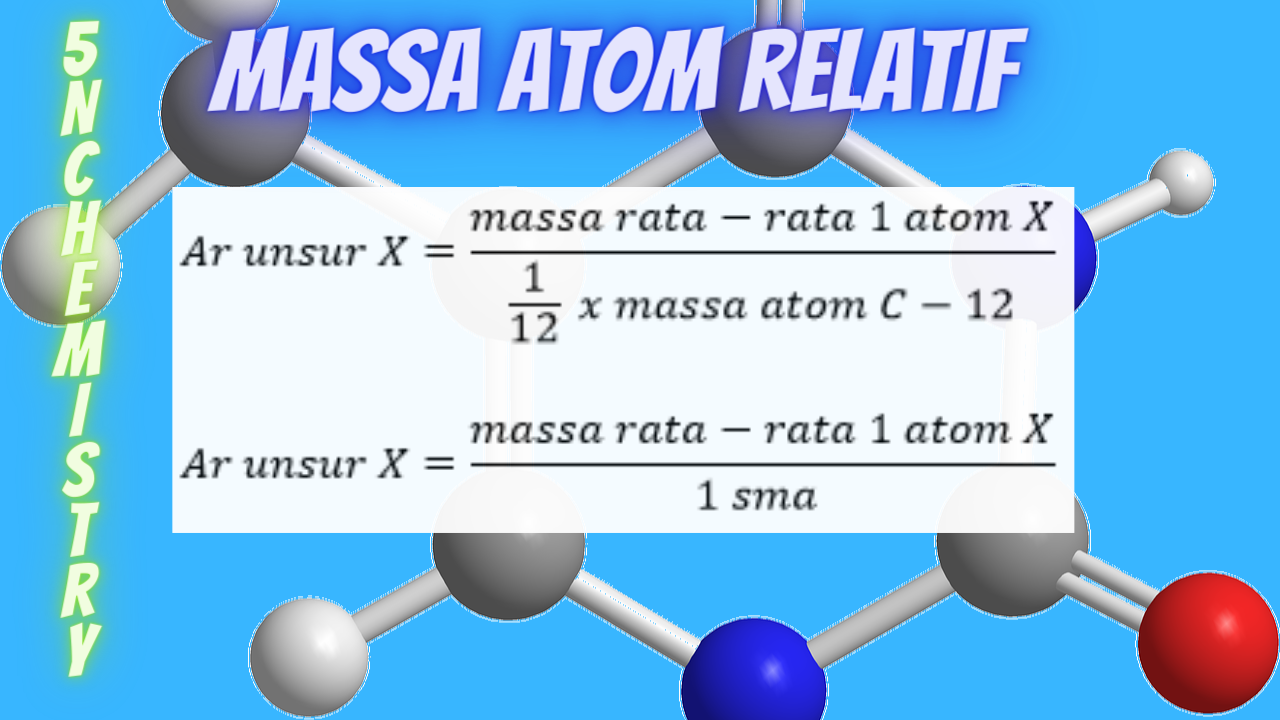
Cara Menentukan Massa Atom Relatif (Ar) Unsur 5NChemistry
8 am - 4:30 pm. Thursday. 8 am - 4:30 pm. Friday. 8 am - 4:30 pm. Saturday. Closed. Read verified clinic information, patient reviews and make an appointment at Alexandria Hearing Centers, Massa & Associates - Sherwood, 2616 Sherwood Hall Ln, Alexandria, Virginia 22306.

Diketahui massa atom relatif (Ar) O=16, Al= 27 , dan S...
Video ini berisi cara menentukan massa atom relatif ( Ar) berdasar standar masa atom C 12, dan berdasar isotop & kelimpahan di alam. #kimia, #IPA, #kimiaSMA,.

Massa atom relatif (Ar) H=1, O=16 ; tetapan Avogadro =6...
Dari definisi massa molekul relatif ini, sebenarnya sudah bisa diketahui rumusnya, yaitu: Mr molekul AxBy = (x. Ar A) + (y. Ar B) + dst. Selain itu, massa molekul relatif juga dapat ditentukan dengan rumus: Mr molekul atau zat X =. massa rata-rata satu molekul atau zat X. 1/12 x massa atom isotop C-12.

MASSA ATOM RELATIF (Ar) DAN MASSA MOLEKUL RELATIF YouTube
Sehingga perhitungan massa atom relatif suatu unsur adalah perhitungan satuan massa atom yang dibandingkan dengan 1 massa atom Karbon-12 Massa 1 atom karbon-12 itu setara dengan= 12 s.m.a, jika mengikuti satuan metrik, massa atom C-12 sebesar 2,04 x 10 -27 Kg

MASSA ATOM RELATIF KIMIA SMA KELAS 10 YouTube
Massa Atom Relatif. Pengertian massa atom relati f atau Ar adalah bilangan yang menyatakan perbandingan massa rata - rata satu atom suatu unsur terhadap 1/12 massa satu atom karbon - 12. Pemilihan atom karbon berdasarkan pada kesepakatan internasional yang menetapkan bahwa massa isotop karbon - 12 memiliki massa tepat 12 sma (satuan massa.

Massa atom relatif (Ar) H=1 dan O=16 , tetapan Avogadr...
Mr = Ʃ A Contoh 4 : Jika Ar H = 1, Ar O = 16, dan massa 1 atom 12C = 2 x 10-23 gram, tentukan massa 10 molekul air ! Jawab : Mr H2O = (2 x Ar H) + (1x Ar O) = 18 Massa.1.molekul.H 2O Mr H2O = 1 x.Massa.satu.atom.karbon − 12 12 1 Massa 1 molekul H2O = Mr H2O x x massa satu atom 12C 12 1 = 18 x x 2 x 10-23 gram 12 = 3 x 10-23 gram Massa 10.

Cara Menghitung Massa Atom Relatif Ar Dan Massa Molekul Relatif Mr My XXX Hot Girl
5 Hukum Dasar Kimia, Bunyi, Rumus, Contoh Soal dan Pembahasan 2. Para ahli kimia menggunakan isotop karbon C-12 sebagai standar dengan massa atom relatif sebesar 12. Massa atom relatif menyatakan perbandingan massa rata-rata satu atom suatu unsur terhadap 1/12 massa atom C-12. Atau dapat dituliskan sebagai berikut. 1 satuan massa atom (amu) =. 1.

Massa atom relatif (Ar) dan Massa molekul relatif (Mr) penjelasan materi KIMIA kelas X
Massa atom (m a) dari suatu unsur kimia adalah massa suatu atom pada keadaan diam, umumnya dinyatakan dalam satuan massa atom. [1] Massa atom sering disinonimkan dengan massa atom relatif, massa atom rata-rata, dan bobot atom. Walaupun demikian, terdapat sedikit perbedaan karena nilai-nilai tersebut dapat berupa rata-rata berbobot dari massa.

Tabel Massa Atom Relatif
Relative atomic mass (symbol: A r; sometimes abbreviated RAM or r.a.m.), also known by the deprecated synonym atomic weight, is a dimensionless physical quantity defined as the ratio of the average mass of atoms of a chemical element in a given sample to the atomic mass constant.The atomic mass constant (symbol: m u) is defined as being 1 / 12 of the mass of a carbon-12 atom.

Massa Atom Relatif (Stoikiometri Kimia SBMPTN, SMA) YouTube
Video ini berisi cara menentukan massa atom relatif ( Ar) berdasar standar masa atom C 12, dan berdasar isotop & kelimpahan di alam. -----.

Diketahui massa atom relatif (Ar) H=1, C=12, N=14, dan O=...
Video ini berisi penjelasan tentang massa atom relatif (Ar) yang dilengkapi dengan contoh-contoh soal.Open private class/kelompok belajar kimia SMA dan alumn.

Massa atom relatif (Ar) dan massa molekul relatif (Mr) contoh soal dan pembahasan YouTube
Definisi. Definisi IUPAC bobot atom adalah: . An atomic weight (relative atomic mass) of an element from a specified source is the ratio of the average mass per atom of the element to 1/12 of the mass of an atom of 12 C.. Suatu bobot atom (massa atom relatif) suatu unsur dari suatu sumber tertentu adalah perbandingan rata-rata massa per atom unsur terhadap 1/12 massa satu atom 12 C.

Tabel Massa Atom Relatif
#LeGurules #KimiaSMA #StokiometriKimiaVideo kali ini membahas materi Kimia SMA - Stokiometri (1) - Massa Atom Relatif, Massa Molekul Relatif, Ar, Mr (D)Tonto.

Tabel Massa Atom Relatif Dan Bilanganoksidasi Unsur
Massa atom relatif adalah massa suatu atom yang ditentukan dengan cara membandingkan massa atom standar. Massa atom relatif ini disimbolkan dengan Ar dan tidak memiliki satuan . Dalam teori atom Bohr , disebutkan bahwa atom-atom dari unsur tertentu di alam dapat memiliki massa yang berbeda-beda.

Massa Atom Relatif dan Contoh Perhitungannya
Interactive periodic table showing names, electrons, and oxidation states. Visualize trends, 3D orbitals, isotopes, and mix compounds. Fully descriptive writeups.