
Konfigurasi Elektron, Aturan Aufbau, Larangan Pauli dan Aturan Hund YouTube
Larangan Pauli. Larangan Pauli ditemukan oleh seorang ilmuwan asal Austria, yaitu Wolfgang Pauli. Larangan ini menyatakan bahwa dalam satu atom, tidak ada elektron yang memiliki bilangan kuantum sama.. Gas mulia adalah gas golongan VIIIA yang cukup stabil, sehingga sulit untuk bereaksi dengan unsur lain. Golongan unsur gas mulia terdiri dari.

SMA Kimia Konfigurasi Elektron Larangan Pauli YouTube
Konfigurasi elektron yang pertama kali dipikirkan adalah berdasarkan pada model atom model Bohr.Adalah umum membicarakan kelopak maupun subkelopak walaupun sudah terdapat kemajuan dalam pemahaman sifat-sifat mekanika kuantum elektron. Berdasarkan asas larangan Pauli, sebuah orbital hanya dapat menampung maksimal dua elektron.Namun pada kasus-kasus tertentu, terdapat beberapa orbital yang.

Andaikan larangan Pauli membolehkan terdapat tiga elektro...
Asas larangan Pauli adalah prinsip mekanika kuantum yang dirumuskan oleh fisikawan Austria Wolfgang Pauli pada tahun 1925. Dalam bentuk yang paling sederhana untuk elektron pada atom tunggal, aturan ini menyatakan bahwa tidak ada dua elektron yang memiliki bilangan kuantum yang sama. Jadi bila n, l, dan ml kedua elektron semuanya sama, ms haruslah berbeda, sehingga kedua elektron tersebut.

Konfigurasi Elektron Memahami Aturan Aufbauf, Aturan Hund dan Larangan Pauli YouTube
Konfigurasi Elektron Menurut Larangan Pauli - Pada tahun 1928, Wolfgang Pauli (1900 - 1958) mengemukakan bahwa tidak ada dua elektron dalam satu atom yang boleh mempunyai keempat bilangan kuantum yang sama. Dua elektron yang mempunyai bilangan kuantum utama, azimuth, dan magnetik yang sama dalam satu orbital, harus mempunyai spin yang berbeda.

struktur atom 6 asas larangan pauli YouTube
Konfigurasi elektron adalah susunan atau gambaran yang menunjukan penempatan elektron dalam suatu atom. Susunan elektron-elektron tersebut berdasarkan kulit atau orbital.. Asas larangan Pauli. Setiap orbital diisi maksimum 2 elektron dengan spin yang berlawanan. Kemungkinan 2 elektron akan memiliki 3 bilangan kuantum n, l, dan m sama.

Asas Larangan Pauli PDF
KOMPAS.com - Ada beberapa konsep yang mendasari konfigurasi elektron suatu atom, salah satunya adalah larangan Pauli.Apa yang dimaksud dengan konsep larangan Pauli?Berikut adalah penjelasannya! Dilansir dari Encyclopedia Britannica, larangan Pauli adalah konsep yang dikemukakan oleh fisikawan asal Austria bernama Wolgang Pauli pada tahun 1925 dalam rangka memperhitunkan pola emisi cahaya atom.

Kenali Apa Itu Tes Pauli Beserta Fungsi, Tips, dan Cara Mengerjakannya Blog Ekrutes
Larangan Pauli adalah tradisi yang terkenal di dunia permainan catur. Terletak di Bayern, Jerman, Larangan Pauli mengacu pada aturan yang melarang seorang raja bergerak ke sebuah kotak yang dapat diambil oleh musuh, sehingga catur berkembang menjadi satu strategi yang menggambarkan kekacauan dan ketelitian. Temukan lebih lanjut tentang sejarah dan strategi Larangan Pauli di artikel ini.

Konfigurasi Elektron Prinsip Aufbau, Larangan Pauli, dan Aturan Hund
Aturan ini disebut Prinsip larangan Pauli. Makna dari larangan Pauli adalah jika elektron-elektron memiliki ketiga bilangan kuantum (n, A, m) sama. maka elektron-elektron tersebut tidak boleh berada dalam orbital yang sama pada waktu bersamaan. Akibatnya, setiap orbital hanya dapat dihuni maksimum dua elektron dan arah spinnya harus berlawanan.

Konfigurasi Elektron
Dari tabel di atas dapat kita ketahui bahwa elektron valensi dari Lithitum (3 Li) adalah 1 dan elektron valensi dari Sulfur (16 S) adalah 6. B. Aturan dalam Konfigurasi Elektron. Berdasarkan model atom mekanika kuantum, terdapat tiga aturan yang berlaku pada konfigurasi elektron yaitu: Asas larangan Pauli (Wolfgang Linus Pauli (1926))

tentukan azas aufbau,kaidah hund,larangan pauli, bilangan kuantum utama, bilangan kuantum
Asas Larangan Pauli - Pengertian Orbital Atom , Konfigurasi Elektron Atom Berelektron Banyak, Dan Sistem Periodik Unsur. Lantanida (unsur tanah- langka) adalah unsur-unsur dengan sub kulit terdaiam 4f terisi kemudian setelah sub kulit 'terluar' 6s. Karena sub kulit f dengan 7 orbital diisi maksimum 14 elektron, maka Lantanida hanya.
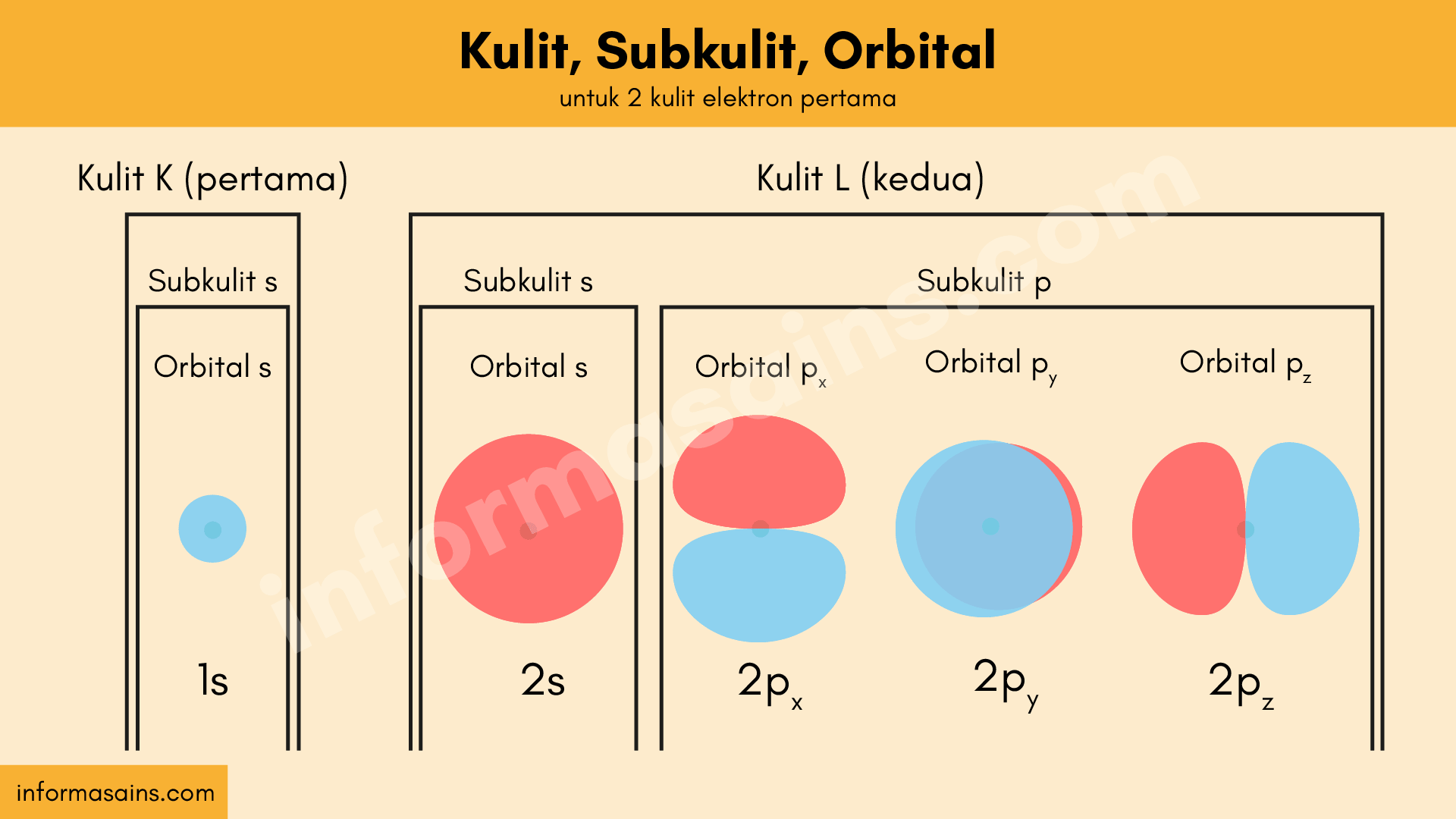
orbital Arsip InformasainsEdu
Larangan Pauli. Berdasarkan larangan Pauli, dalam suatu atom tidak boleh terdapat dua elektron yang memiliki keempat bilangan kuantum (n, l, m, dan s) yang sama.. Gas mulia adalah unsur-unsur yang memiliki kestabilan yang sangat tinggi dan dalam sistem periodik terdapat pada golongan VIIIA.

Pauli Test Pengertian Tujuan Dan Cara Mengerjakannya Accurate Online Riset
Pengertian Larangan Pauli. Larangan Pauli menyatakan bahwa tidak ada dua elektron dapat memiliki empat bilangan kuantum yang sama.. dan yang lain akan mempunyai spin ke bawah (-½). Tiga bilangan kuantum pertama adalah n=1, l=0, m=0. Hanya dua elektron yang sesuai, yang akan berupa s=-½ atau s =+½. Pelajari lebih lanjut: Sifat Paramagnetik.

√ Tes Pauli Pengertian, Contoh dan Cara Mengerjakannya!
Berdasarkan Prinsip Larangan Pauli tersebut dapat disimpulkan bahwa jumlah elektron yang menempati sebuah orbital paling banyak dua elektron dengan arah rotasi yang saling berlawanan. Hal tersebut berarti bilangan kuantum n, ℓ, dan m sebuah orbital pasti sama, namun berbeda halnya dengan s. Sehingga dapat disimpulkan jumlah elektron maksimum.
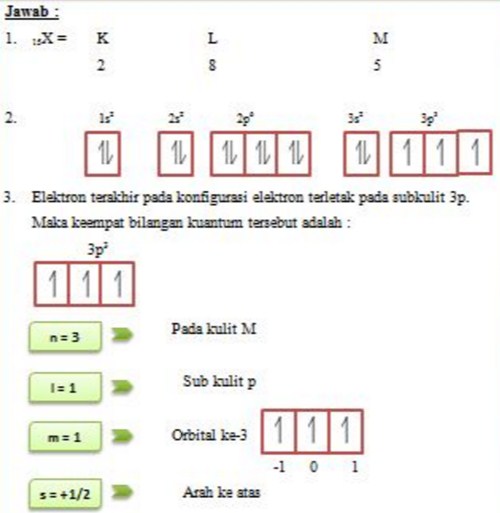
Konfigurasi Elektron Menurut Larangan Pauli Rumus Kimia
Asas Larangan Pauli. Terakhir, aturan konfigurasi elektron mekanika kuantum adalah berdasarkan asas larangan Pauli. Asas ini menyebutkan bahwa elektron-elektron dalam menyusun atom memiliki masing-masing empat bilangan kuantum yang berbeda. Jadi, gak bisa tuh ada yang sama bilangan kuantumnya di dalam satu atom.

Larangan Pauli
Prinsip Aufbau, larangan Pauli, dan aturan Hund adalah aturan yang harus diikuti dalam menentukan konfigurasi elektron yang benar. Orbital dikenal memiliki penyimpangan dalam konfigurasi elektron. Orbital d stabil pada keadaan setengah penuh atau penuh, sehingga dalam beberapa unsur golongan transisi terdapat penyimpangan dalam konfigurasi.

PPT Struktur Atom PowerPoint Presentation, free download ID3882274
Yang memenuhi aturan Hund adalah penulisan pada nomor (ii), karena elektron harus mengisi seluruh orbital terlebih dahulu sebelum berpasangan. 3. Larangan Pauli. Berdasarkan larangan Pauli, dalam suatu atom tidak boleh terdapat dua elektron yang memiliki keempat bilangan kuantum (n, l, m, dan s) yang sama.