
Derajat Ionisasi Larutan Elektrolit YouTube
Larutan elektrolit adalah larutan yang dapat menghantarkan arus listrik karena mengandung ion-ion yang bergerak bebas. Ion-ion itulah yang menghantarkan listrik melalui larutan.. Ilustrasi HCl termasuk elektrolit kuat. Foto: iStock. K2SO4, dan CaCL2. 2. Elektrolit Lemah. Larutan elektrolit lemah memiliki daya hantar listrik yang buruk.

Show the formation of K2SO4 by electron transfer method Science Metals and Nonmetals
Kata Pengantar. Dalam ilmu kimia, elektrolit adalah zat yang dapat menghantarkan arus listrik ketika dilarutkan dalam pelarut tertentu. Salah satu zat yang termasuk dalam kategori ini adalah k2so4 atau kalium sulfat. Meskipun mungkin kurang dikenal dibanding dengan elektrolit lainnya seperti natrium klorida, k2so4 memiliki sifat elektrolit yang sangat penting untuk berbagai aplikasi industri.

Mengenal Larutan Elektrolit dan Non Elektrolit Kimia Kelas 10
Kalium sulfat (K2SO4) adalah salah satu jenis pupuk yang sering digunakan oleh petani untuk meningkatkan produktivitas tanaman. Namun, masih banyak yang bingung apakah kalium sulfat termasuk dalam kategori elektrolit atau bukan. Dalam artikel ini, kami akan membahasnya dengan lebih rinci. Elektrolit dan Non-Elektrolit

Contoh Larutan Elektrolit Kuat Lemah Beserta Perbedannya Riset
Pada reaksi elektrolisis K2SO4, terjadi oksidasi dan reduksi. Oksidasi terjadi pada anoda, di mana ion sulfat (SO4 2-) dioksidasikan menjadi oksigen (O2) dan ion sulfat (SO4 2-). Reduksi terjadi pada katoda, di mana ion kalium (K+) direduksi menjadi kalium (K) dan ion kalium hidroksida (KOH).

Larutan NaCl, KCl, MgSO4, K2SO4, dan H2SO4 masingmasing...
NaCl (s) → Na+ (aq) + Cl− (aq) Perlu elo ingat bahwa larutan elektrolit kuat selalu terdiri dari asam kuat, basa kuat dan garam. Nah, larutan NaCl (garam) bukan satu-satunya yang tergolong ke dalam larutan elektrolit kuat. Karena terdapat beberapa larutan yang dapat menghantarkan arus listrik adalah NaOH (soda api), H2SO4 (asam sulfat), HCl.

Larutan Elektrolit dan Nonelektrolit
Larutan elektrolit yang memberikan gejala berupa lampu menyala dan membentuk gelembung gas disebut elektrolit kuat. Contohnya yaitu HCl, air aki, air laut, dan air kapur. Adapun elektrolit yang tidak memberikan gejala lampu menyala tetapi menimbulkan gelembung gas termasuk elektrolit lemah. Contohnya yaitu larutan amonia, larutan cuka,dan.

Memahami Larutan Elektrolit dan Nonelektrolit beserta Contohnya Kimia Kelas 10
Hai Michael, kakak bantu jawab pertanyaanmu ya. Jawaban: Reaksi ionisasi K2SO4: K2SO4 (aq) → 2K^+ (aq) + SO4^2- (aq) Larutan elektrolit kuat adalah larutan yang baik dalam menghantarkan arus listrik. Kemampuan suatu larutan menghantarkan arus listrik dipengaruhi oleh zat terlarut pada larutan elektrolit yang terdisosiasi.

Reaksi ionisasi asam sulfat (air aki) yang benar adalah.
Pada larutan non elektrolit, senyawa dalam air tidak mengalami proses ionisasi. Larutan non-elektrolit tidak dapat terionisasi dalam air, maka 𝛼 = 0. Larutan non-elektrolit terdiri atas kelompok senyawa organik molekular yang larut. Tidak menghantarkan arus listrik; Contoh larutan non-elektrolit diantaranya: Sukrosa (C₁₂H₂₂O₁₁)

Larutan Elektrolit dan Non Elektronik Beserta Contoh Elektrolit Belajar IPA
Reaksi elektrolisis larutan encer dengan elektrode grafit. Hasil elektrolisisnya adalah gas oksigen di anode dan gas hidrogen di katode. 2. Reaksi elektrolisis larutan dengan elektrode tembaga. Oleh karena anodenya dari Cu (anode reaktif), maka anode tersebut mengalami oksidasi dan hasilnya adalah ion di anode dan gas hidrogen di katode. Nah.

Elektrolit Kuat dan Elektrolit Lemah (Kimia SBMPTN, UN, SMA) YouTube
Reaksi berikut dapat menjelaskan mengapa larutan Al2(SO4)3 termasuk larutan elektrolit kuat. Reaksi ionisasi dari larutan tersebut adalah. A. Al2(SO4)3 → 2Al3+ + 3S2- + 12O2- B. Al2(SO4)3 → 2Al + S + 4O C. Al2(SO4)3 → H2O + Al2(SO4)3 D. Al2(SO4)3 → 2A3+ + 3SO4²⁻ E. Al2(SO4)3 → Al2⁺ + SO42-. elektrolit kuat berarti.

Penyetaraan Reaksi Redoks KI + H2SO4 → K2SO4 + I2 + H2S + H2O Serba Ada
Nilai kapasitansi spesifik KATK dalam larutan elektrolit Li2SO4, Na2SO4 dan K2SO4. Kata kunci: Tempurung Kemiri, Aktivator KOH, Li2SO4, Na2SO4, K2SO4, Kapasitansi Spesifik. Item Type: Thesis (Skripsi) Subjects: Q Science > QD Chemistry: Depositing User: sangiasseri abubakar: Date Deposited: 08 Dec 2020 00:58.
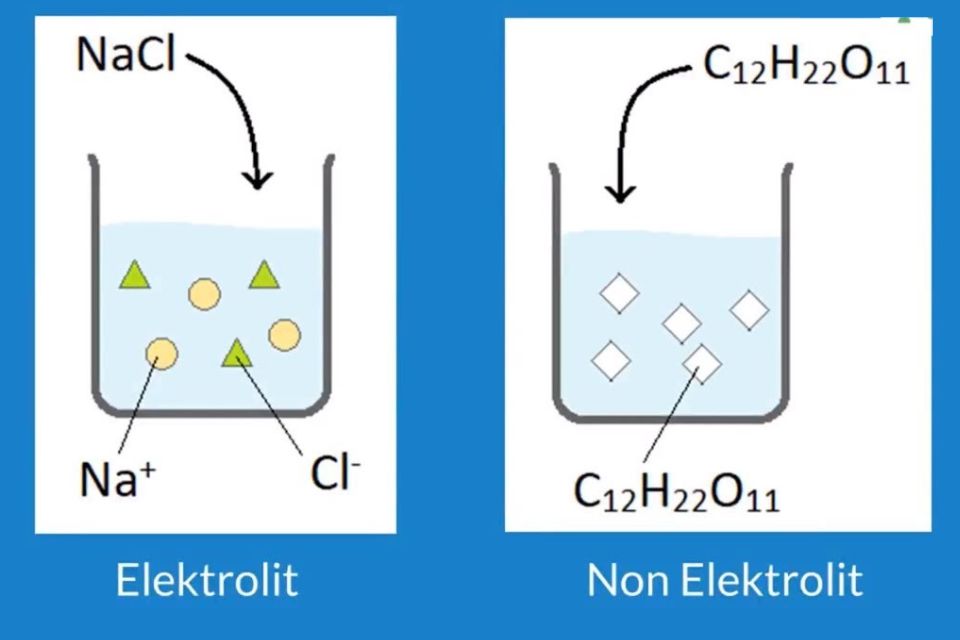
Mengenal Pengertian Larutan Elektrolit dan Non Elektrolit, Sifat, Ciriciri, dan Cara Membedakan
K2SO4 atau kalium sulfat adalah senyawa kimia yang termasuk dalam elektrolit, karena mampu menghasilkan ion-ion dalam larutan. Dalam aplikasinya, k2so4 dapat digunakan sebagai pupuk yang berguna untuk meningkatkan kesuburan tanah dan pertumbuhan tanaman. Mengetahui bahwa k2so4 adalah elektrolit sangat penting untuk memahami sifat dan fungsi senyawa ini dalam berbagai bidang.
Di bawah ini yang termasuk ke dalam larutan elektrolit ad...
K2SO4 termasuk larutan elektrolit atau bukan? 1 Lihat jawaban Iklan Iklan dimasprasetyo71 dimasprasetyo71 Jawaban: Elektrolit kuat. Penjelasan: K2SO4 itu terdiri dari campuran KOH (Basa kuat) dan H2SO4 (asam kuat) maka terbentuk garam kuat yaitu elektrolit kuat. bantu subscribe dan like channel youtube : Studio Tutorial Pembelajaran.
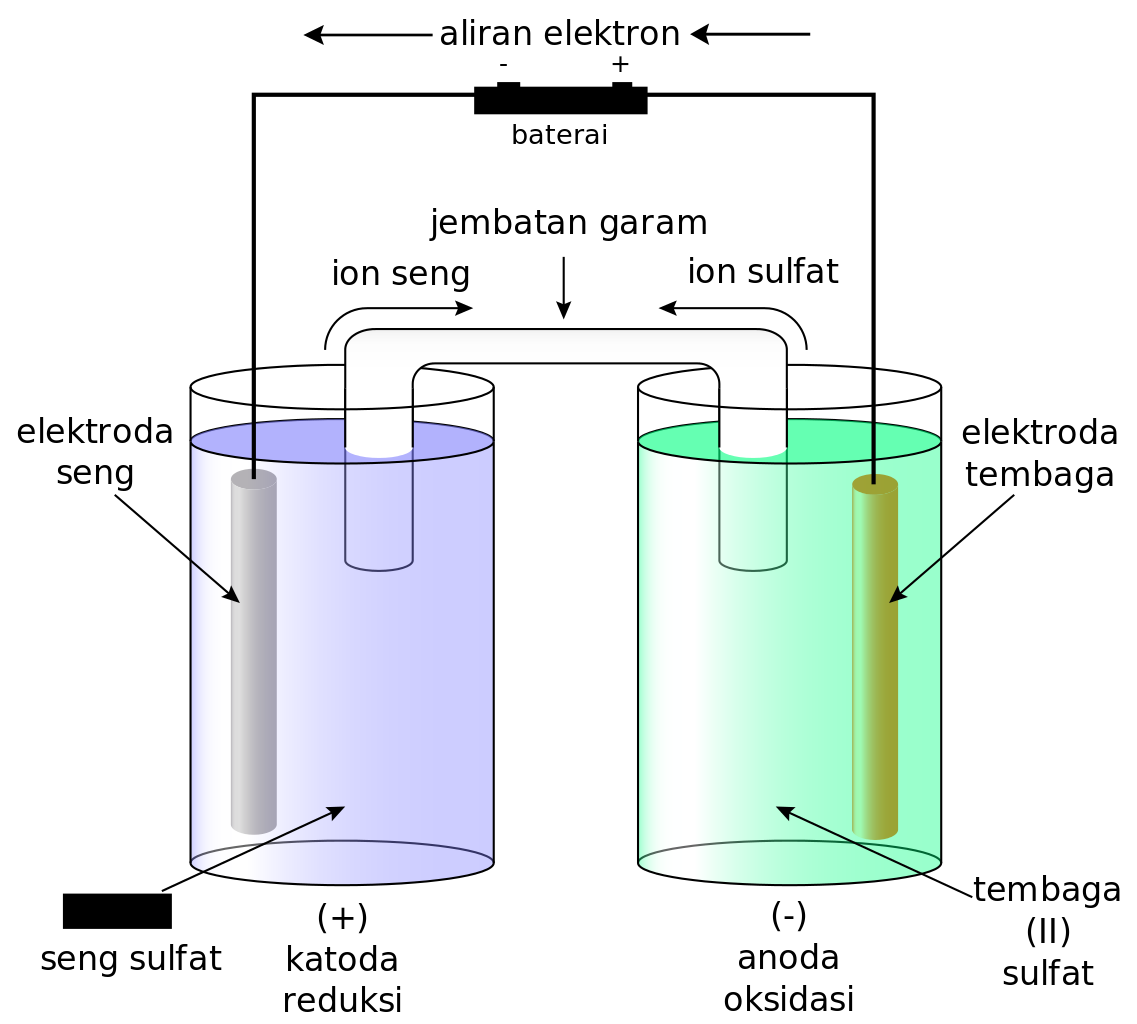
Chemistry ELEKTROLISIS
Elektrolit, Ketahui Jenis dan Manfaatnya untuk Tubuh. Elektrolit adalah mineral bermuatan listrik yang terdapat di dalam sel, jaringan, dan cairan tubuh, termasuk darah, urine, dan keringat. Ada banyak jenis elektrolit dengan fungsinya masing-masing. Agar semua organ tubuh dapat berfungsi dengan baik, diperlukan asupan elektrolit yang cukup.
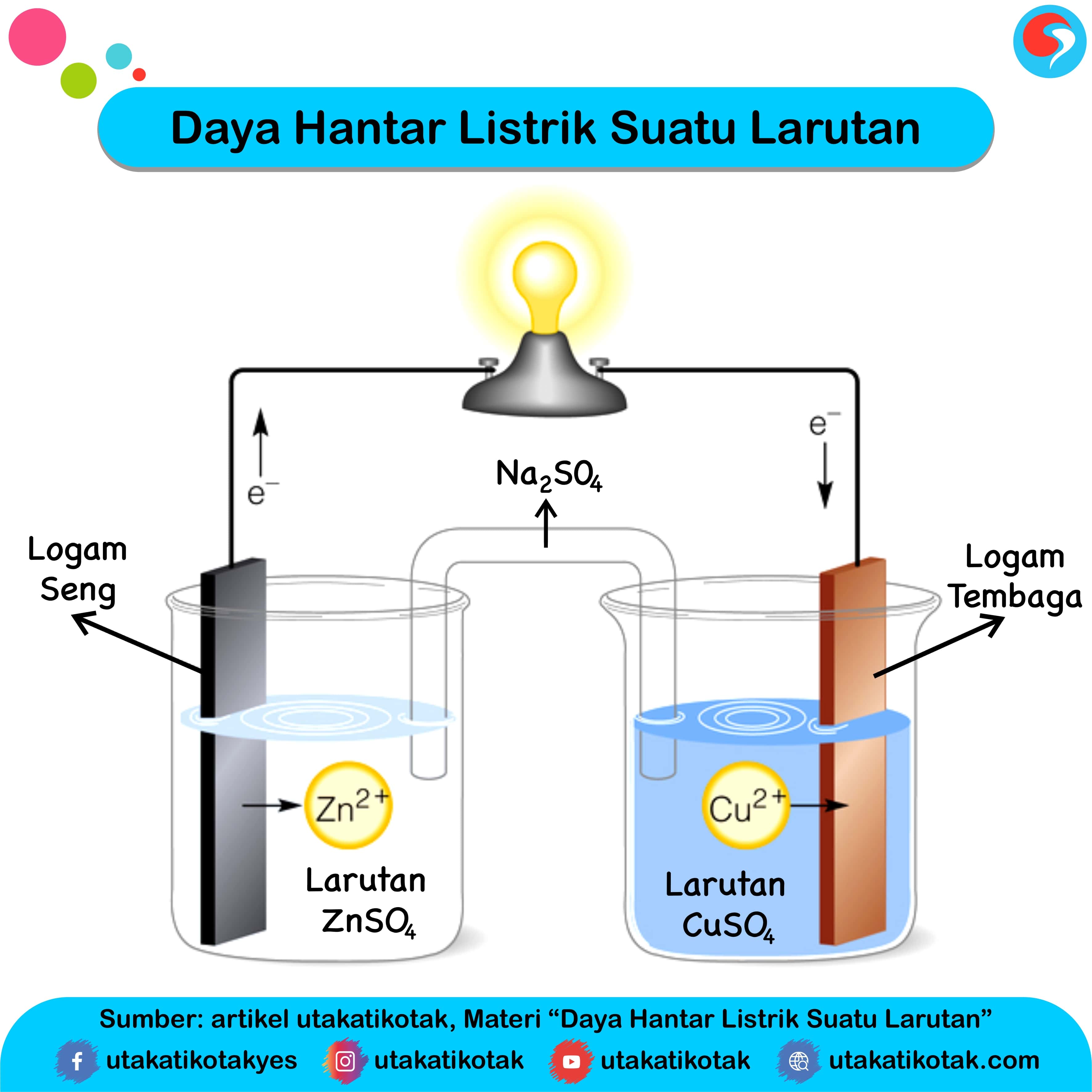
Daya Hantar Listrik Suatu Larutan
5. Tentukan jumlah ion elektrolit-elektrolit dari CaCO 3 adalah… A. 1 B. 3 C. 2 D. 4 E. 5. Pembahasan: CaCO 3 Ca 2+ + CO 3 2-Jumlah Ca 2+ adalah 1 Jumlah CO 3 2- adalah 1 Jumlah ion adalah 2 (elektrolit biner). Jadi, jawabannya adalah C. 6. Larutan natrium hidroksida mempunyai derajat ionisasi 1, artinya… A. Tidak Terionisasi B. Terionisasi.

Contoh Elektrolit Kuat Dan Lemah
The balancing goes around the 4 e X −. I thought it was in order to make OH- and H+ to dovetail into water nicely, and forgot about electron balancing. - CowperKettle. May 5, 2016 at 13:39. 1. It seems to me that there is a typo in the first equation. It should be. 2 H X 2 O + 2 e X − ↽ − − ⇀ H X 2 ↑ + 2 O H X −. - MaxW.