
Jumlah Maksimum Elektron Yang Dapat Menempati Kulit L Adalah JumlahID
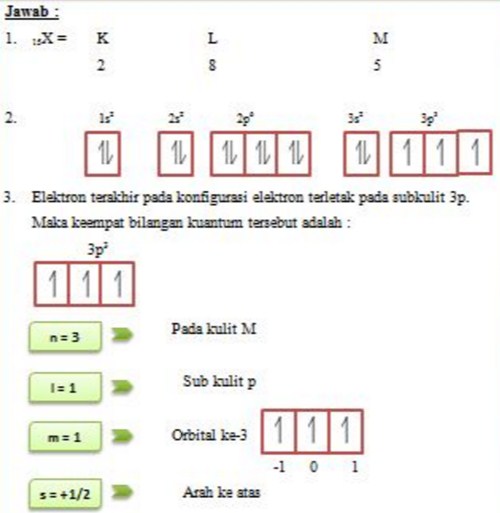
Nah sekarang kita akan menggambarkan konfigurasi elektron memakai diagram orbital, teman. Sebenarnya gambarnya cukup mudah kok. Suatu subkulit punya sejumlah orbital. Orbital itu digambarkan sebagai persegi dan berisi garis setengah panah yang mewakili elektron. Subkulit s punya 1 orbital, p punya 3 orbital, d punya 5 orbital, dan f 14 orbital.
Konfigurasi Elektron Menurut Larangan Pauli Rumus Kimia
Artinya, ada jumlah maksimal elektron yang dapat menempati suatu kulit. Baca juga: Teori Kulit Elektron Bohr. Jumlah maksimal elektron dalam kulit atom dapat dihitung menggunakan rumus 2(n²). Jumlah elektron maksimum pada kulit K = 2n² = 2(1²) = 2; Jumlah elektron maksimum pada kulit L = 2n² = 2(2²) = 2 × 4 = 8

Jumlah Elektron Maksimum Pada Kulit P Adalah Cara Golden
Jumlah elektron maksimum yang dapat ditampung oleh suatu kulit adalah sebagai berikut: Kulit K (n = 1): jumlah elektron maksimum = 2(1). elektron yang mengorbit suatu atom terlebih dahulu mengisi tingkat energi yang lebih rendah sampai penuh sebelum mengisi tingkat energi yang lebih tinggi. Urutan pengisian elektron berdasarkan tingkat.
Teori Elektron Mekanik Alat Berat
Kulit yang paling dekat dengan inti atom adalah kulit K (n = 1) yang dapat ditempati paling banyak oleh 2 elektron. Semakin besar nomor kulit (n), jumlah elektron yang dapat menempati kulit tersebut akan semakin banyak.Urutan kulit dalam atom, yaitu: Kulit K = n = 1. Kulit L = n = 2. Kulit M = n = 3.

Perhatikan data jumlah elektron, jumlah neutron, dan juml...
Jumlah maksimal partikel elektron yang dapat menempati kulit m bergantung pada rumusan 2n^2, di mana n merupakan nomor kulit. Maka dari itu, untuk kulit m (dalam hal ini, kulit ketiga), partikel elektron maksimal yang dapat menempatinya adalah 2 x (3^2) = 18 partikel elektron.

Menghitung Jumlah Proton, Elektron, dan Neutron dari Tabel Periodik KnK Land
Jumlah Elektron Maksimum pada Kulit n dalam Atom Besi. Pada atom besi, kulit n pada atomnya mampu menampung hingga 18 elektron berdasarkan aturan pengisian kulit elektron. Besi memiliki 26 proton dan 26 elektron dalam keadaan netralnya. Dalam hal ini, 18 elektron akan mengisi kulit n sehingga atom besi mencapai konfigurasi elektron yang stabil.

Jumlah orbital yang terisi electron pada kulit ke3 ataom...
Elektron-elektron akan mengisi kulit-kulit elektron pada atom dimulai dari kulit K yang merupakan level energi terendah. Setiap kulit elektron hanya dapat terisi sejumlah tertentu elektron. Jumlah maksimum elektron yang dapat terisi pada kulit elektron ke-n adalah 2n 2. Namun, jumlah maksimum elektron pada kulit terluar dari suatu atom adalah 8.

Lengkapilah tabel berikut! Unsur Nomor Atom Konfigurasi E...
Nilai l = 2 menunjukkan elektron terdapat pada subkulit d. Jumlah orbital pada subkulit d adalah 5, sehingga jumlah elektron maksimalnya adalah: Oleh karena itu,jumlah elektron maksimal yang dapat mengisi sub kulit dengan l = 2 adalah 10. Jadi, jawaban yang benar adalah E.

Konfigurasi elektron berdasarkan kulit Get Canva
Jumlah maksimum elektron yang dapat terisi pada kulit elektron ke-n adalah 2n 2, di mana n adalah nomor kulit atau bilangan kuantum utama. Cara Menentuan Elektron Valensi. Elektron-elektron akan mengisi kulit-kulit elektron pada atom dimulai dari kulit pertama yang terdekat dengan inti, yaitu kulit K yang merupakan level energi yang terendah.

Jumlah elektron valensi dan golongan unsur berikut adalah...
Lapisan l terdiri dari sublapisan yang disebut sublapisan s. Sublapisan s hanya memiliki satu orbital dengan bentuk bola. Setiap orbital hanya dapat menampung maksimal dua elektron. Maka dari itu, jumlah maksimum elektron yang bisa mengisi sublapisan s pada kulit l adalah 2. Rumus untuk Menentukan Jumlah Maksimum Elektron dalam Kulit l. Rumus.
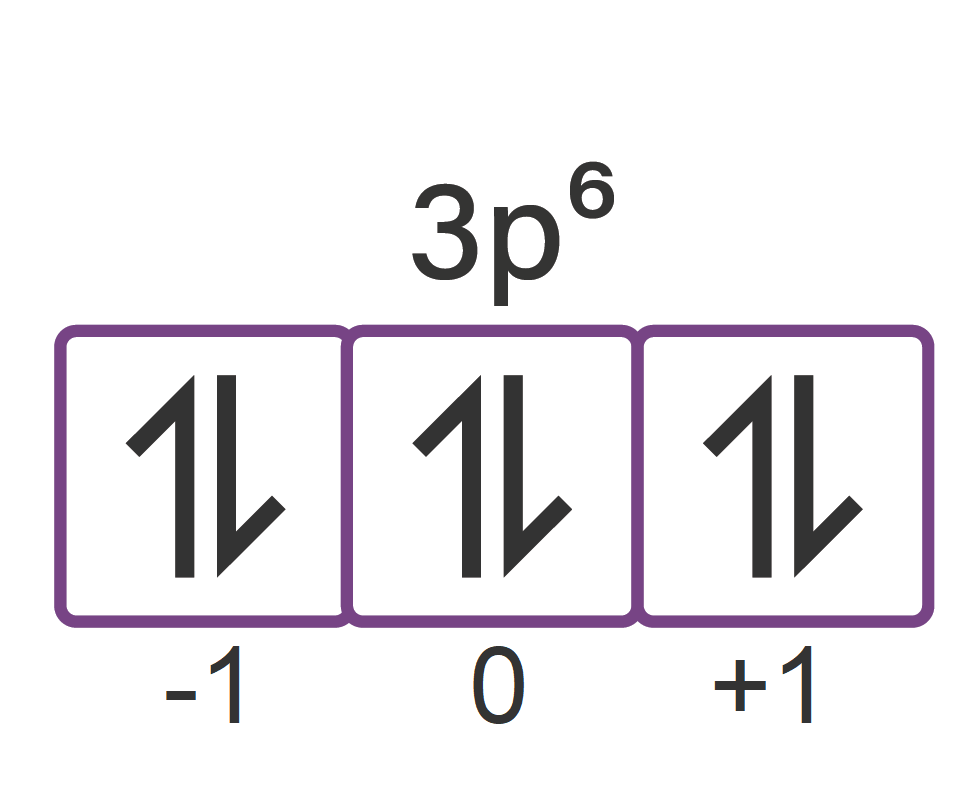
Dalam suatu atom, jumlah maksimum elektron yang me...
Setiap kulit elektron hanya dapat terisi sejumlah tertentu elektron. Jumlah maksimum elektron yang dapat terisi pada kulit elektron ke-n adalah 2n 2, di mana n adalah nomor kulit atau bilangan kuantum utama.. Kulit K (n = 1) maksimum terisi 2 × 1 2 = 2 elektron.; Kulit L (n = 2) maksimum terisi 2 × 2 2 = 8 elektron.; Kulit M (n = 3) maksimum terisi 2 × 3 2 = 18 elektron.

Jumlah maksimum elektron yang terdapat pada kulit M adala...
Dengan berinteraksi antara elektron di kulit n, unsur-unsur dapat membentuk ikatan kimia dengan unsur lainnya. Menghitung Jumlah Elektron Maksimum pada Kulit n dengan Rumus 2n^2. Untuk mengetahui jumlah elektron maksimum pada kulit n, kita dapat menggunakan rumus 2n^2. Di dalam rumus ini, n mewakili nomor kulit elektron yang ingin diketahui.

Jumlah Elektron Yang Menempati Kulit N Adalah pohon dadap daun dadap serep
Jumlah maksimum elektron yang dapat mengisi setiap kulit dirumuskan dengan 2n² (n= kulit yang ditempati elektron). Jumlah elektron secara maksimal yang dapat ditempati pada setiap kulit yaitu kulit pertama (kulit K) memiliki 2 elektron, kulit kedua (kulit L) memiliki 8 elektron, kulit ketiga (kulit M) memiliki 18 elektron, dan kulit keempat.

Jumlah Elektron Maksimum Yang Terdapat Pada Kulit N Adalah JumlahID
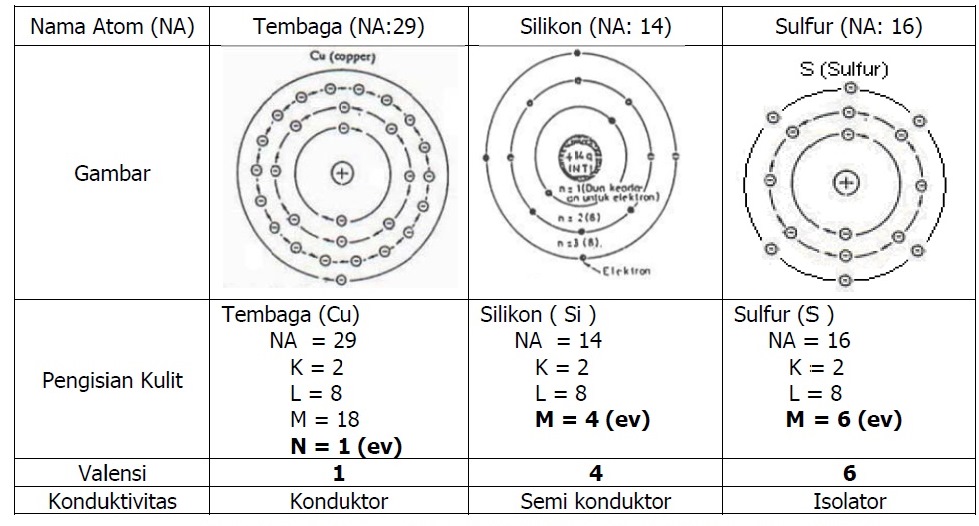
Valensi biasanya jumlah elektron yang dibutuhkan untuk mengisi kulit terluar atom. Karena ada pengecualian, definisi valensi yang lebih umum adalah jumlah elektron yang dengannya atom tertentu umumnya terikat atau jumlah ikatan yang dibentuk atom. (Pikirkan besi, yang mungkin memiliki valensi 2 atau valensi 3.)

Tentukan jumlah elektron maksimum dalam suatu atom yang e...
Pertanyaan. Jumlah maksimum elektron yang menempati kulit ketiga ( n = 3) dalam suatu atom adalah.. 10 elektron. 16 elektron. 18 elektron. 32 elektron. 40 elektron. Iklan. IS.

Jumlah maksimum elektron yang menempati kulit ketiga (n
Banyaknya jumlah elektron terluar (elektron valensi) dari suatu atom menentukan sifat-sifat kimia suatu unsur. Konfigurasi elektron dapat dituliskan dengan cara: 1. Berdasarkan Kulit. Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2n2 2 n 2, di mana n menunjukkan kulit atom. Contoh: 11Na 11 N a: 2, 8, 1.