
Larutan Elektrolit dan Nonelektrolit
Glukosa = C6H12O6. Sukrosa = C12H22O11. Etanol = C2H2OH. Contoh reaksi larutan non-elektrolit. C6H12O6 (s) C6H12O6 (aq) Itulah Ulasan tentang Larutan Elektrolit : Pengertian, Ciri, Dan Jenis Beserta Contohnya Secara Lengkap Semoga apa yang diulas diatas bermanfaat bagi pembaca. Sekian dan Terima Kasih.

Larutan elektrolit dan non elektrolit
Penghantaran arus listrik. Larutan elektrolit terdapat ion-ion yang berbeda muatan dan bergerak bebas. Bila arus listrik dihubungkan, kation bergerak menuju katode dan anion bergerak menuju anode sehingga arus listrik mengalir dalam sistem tersebut. 5. Sifat - sifat dari larutan elektrolit dan non elektrolit.

Materi Kimia Elektrolit dan Non Elektrolit YouTube
Sejarah Larutan Elektrolit Dan Non Elektrolit. Pada tahun 1884, Svante Arrhenius, ahli kimia terkenal dari Swedia mengemukakan teori elektrolit yang sampai saat ini teori tersebut tetap bertahan padahal ia hampir saja tidak diberikan gelar doktornya di Universitas Upsala, Swedia, karena mengungkapkan teori ini.

Soal Larutan Elektrolit Dan Nonelektrolit Satu Trik
NaCl (s) → Na+ (aq) + Cl− (aq) Perlu elo ingat bahwa larutan elektrolit kuat selalu terdiri dari asam kuat, basa kuat dan garam. Nah, larutan NaCl (garam) bukan satu-satunya yang tergolong ke dalam larutan elektrolit kuat. Karena terdapat beberapa larutan yang dapat menghantarkan arus listrik adalah NaOH (soda api), H2SO4 (asam sulfat), HCl.

Larutan Elektrolit dan Non Elektrolit (Kimia SBMPTN, UN, SMA) YouTube
Di sisi lain, pada larutan non elektrolit senyawa dalam air tidak mengalami ionisasi. Oleh karena itu, larutan ini tidak mampu menghantarkan listrik. Kekuatan Larutan Elektrolit Kekuatan larutan elektrolit dapat dibedakan menjadi 2, yaitu larutan elektrolit kuat dan larutan elektrolit lemah. Penjelasannya adalah sebagai berikut. 1.

Larutan Elektrolit dan Reaksi Redoks Kelas 10 • Part 1 Larutan Elektrolit dan Nonelektrolit
Konsep larutan elektrolit dan non-elektrolit pertama kali dijelaskan oleh ahli kimia asal Swedia, Svante August Arrhenius, pada tahun 1884. Menurut Arrhenius yang dikutip dari Kimia Dasar II oleh Elvy Rahmi Mawarnis, senyawa elektrolit dalam air akan terurai menjadi partikel-partikel yang berupa atom atau gugus atom bermuatan listrik yang.

30 Contoh Larutan Elektrolit dan Non Elektrolit
Larutan Elektrolit dan Non-Elektrolit: Sejarah Penemuan Larutan Elektrolit dan Non-Elektrolit. Penemuan larutan elektrolit dan non-elektrolit ternyata berhubungan dengan ilmuwan asal Swedia, Svante August Arrhenius (1859-1927). Kala itu ia tengah melakukan presentasi disertasi untuk gelar PhD-nya di Universitas Uppsala tahun 1884.

SifatSifat Larutan Elektrolit dan Nonelektrolit Memotivasi Diri
Pada larutan non elektrolit, zat non elektrolit yang terlarut tidak dapat terurai menjadi ion-ion, sehingga tidak terdapat ion-ion bebas yang dapat menghantarkan arus listrik. Sebagai contoh, larutan gula sukrosa (C 12 H 22 O 11 ) merupakan larutan non elektrolit.

Larutan Elektrolit dan Non Elektrolit (Komponen Larutan)
Larutan elektrolit dalam sebuah baterai. Elektrolit adalah suatu zat yang larut atau terurai ke dalam bentuk ion-ion dan selanjutnya larutan menjadi konduktor elektrik, ion-ion merupakan atom -atom bermuatan elektrik. Elektrolit bisa berupa air, asam, basa atau berupa senyawa kimia lainnya. Elektrolit umumnya berbentuk asam, basa atau garam.

Memahami Larutan Elektrolit dan Nonelektrolit beserta Contohnya Kimia Kelas 10
Perbedaan Larutan Elektrolit dan Non Elektrolit Masmiani dalam uraian "Larutan Elektrolit, Larutan Non Elektrolit, dan Asam Basa" menyatakan bahwa larutan elektrolit mengandung partikel bermuatan kation dan anion. Jika larutan elektrolit dialirkan listrik (elektron), akan terjadi suatu proses yang dinamakan elektrolisis.

LARUTAN ELEKTROLIT DAN NON ELEKTROLIT YouTube
Larutan elektrolit dan non elektrolit memiliki karakteristik sifat yang berbeda. Perbedaannya adalah sebagai berikut: Sifat larutan elektrolit: Dapat menghantarkan listrik. Memiliki derajat ionisasi yang berkisar antara 0 < α ≤ 1. Jika dinyalakan uji daya hantar listrik: gelembung gas yang dihasilkan banyak, lampu menyala.

Larutan Elektrolit dan Non Elektrolit (Kompone
Larutan elektrolit yang memberikan gejala berupa lampu menyala dan membentuk gelembung gas disebut elektrolit kuat. Contohnya yaitu HCl, air aki, air laut, dan air kapur. Adapun elektrolit yang tidak memberikan gejala lampu menyala tetapi menimbulkan gelembung gas termasuk elektrolit lemah. Contohnya yaitu larutan amonia, larutan cuka,dan.
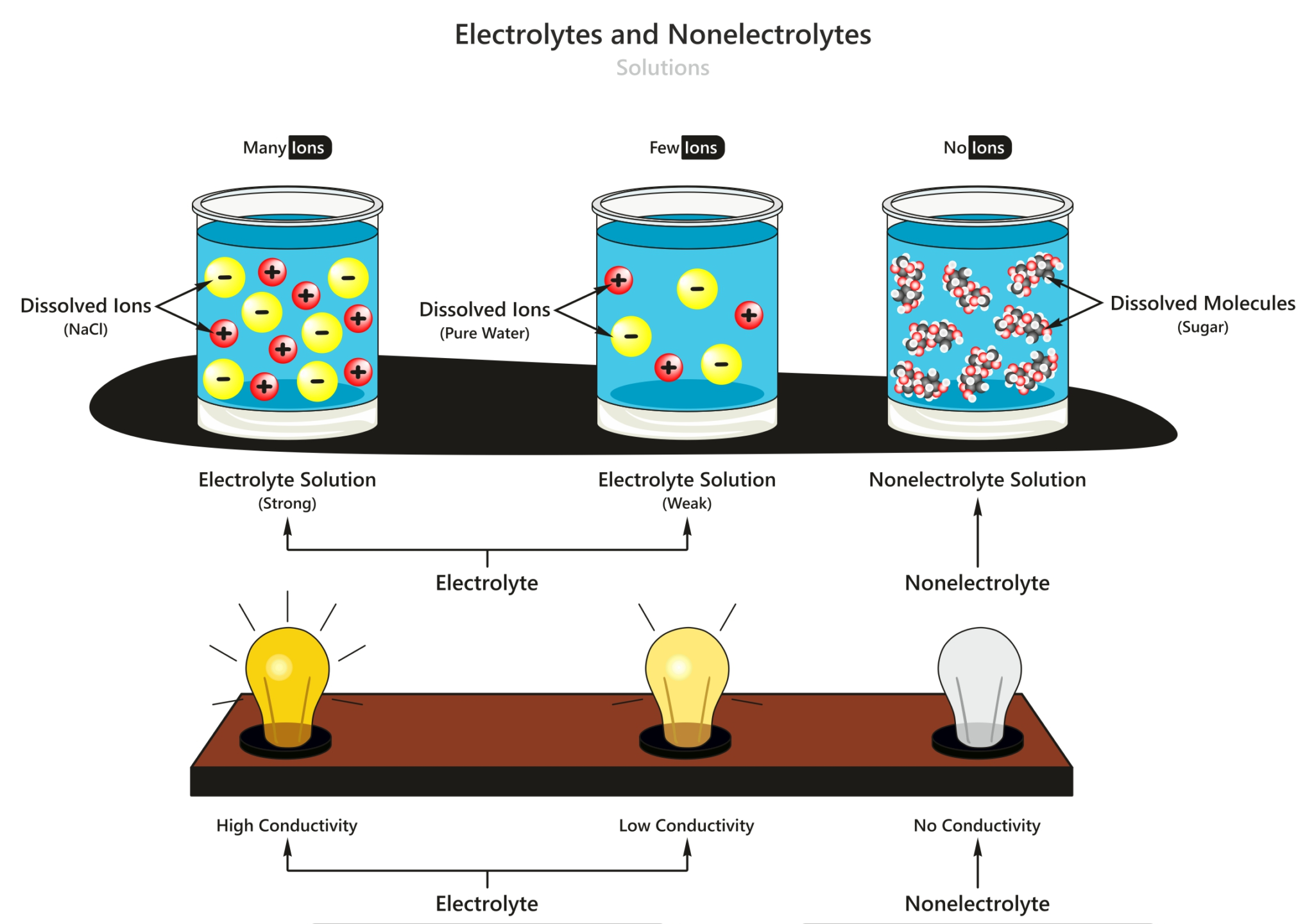
Larutan Elektrolit dan Non Elektrolit Materi Kimia Kelas 10
1. Larutan elektrolit adalah larutan yang dapat mengkonduktivitas listrik karena adanya ion. 2. Larutan non-elektrolit adalah larutan yang tidak dapat mengkonduktivitas listrik karena tidak mengandung ion. 3. Larutan elektrolit dapat digunakan untuk pembuatan baterai, pengolahan air dan pelarut untuk senyawa kimia. 4.
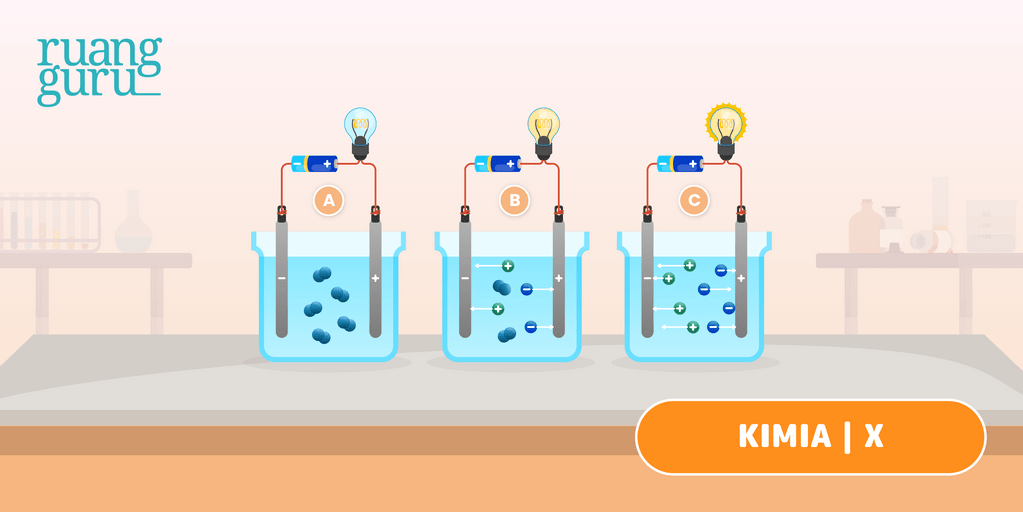
Memahami Larutan Elektrolit dan Nonelektrolit beserta Contohnya Kimia Kelas 10 Belajar
Larutan seperti ini disebut larutan elektrolit. Sebaliknya, larutan yang tidak bisa menghantarkan arus listrik disebut larutan non elektrolit. Keduanya memiliki manfaat yang sangat penting dalam kehidupan manusia, bahkan larutan elektrolit dibutuhkan tubuh agar organ tubuh, seperti otak, saraf, dan otot dapat berfungsi dengan baik.

VIRTUAL LABORATORIUM Larutan Elektrolit dan Non Elektrolit YouTube
Contoh Larutan Non Elektrolit. Larutan selain asam, basa, dan garam, contoh: gula, alkohol, glukosa, urea, dll. Baca Juga : Benzena dan turunannya serta Penjelasannya. Demikian artikel mengenai Larutan ELektrolit dan Non Elektrolit Serta Penjelasannya. Semoga artikel ini dapat bermanfaat dan menambah wawasan anda mengenai pelajaran Ilmu.
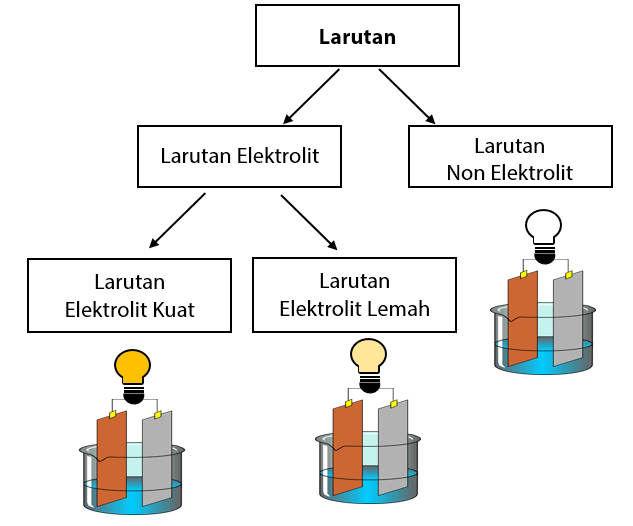
Larutan Elektrolit dan Non Elektrolit
Pengertian Larutan Elektrolit dan Non-Elektrolit Pengertian Larutan Elektrolit. Larutan elektrolit merupakan jenis larutan yang mampu mengalirkan arus listrik karena mengandung ion-ion yang bergerak secara bebas. Keberadaan ion-ion inilah yang bertanggung jawab atas konduktivitas listrik dalam larutan tersebut.. Jelaskan alasan Anda. Jawaban.