
KIMIA KELAS 10 SEMESTER 1, IKATAN KOVALEN YouTube
IKATAN KOVALEN. Berbeda dengan ikatan ion, pada ikatan kovalen atom-atom saling menyumbangkan elektron valensinya untuk dipakai bersama-sama dalam membentuk suatu ikatan. Ikatan Kovalen adalah ikatan yang terbentuk karena pemakaian bersama elektron-elektron terluar dari dua atau lebih atom yang berikatan. Ikatan kovalen dapat juga diartikan.

3 contoh senyawa ion kovalen dan logam Alexandra Springer
Contoh ikatan kovalen jenis ini adalah pembentukan senyawa HCl dan CH4. a. Pembentukan HCl. Konfigurasi elektron 1H : 1s1 sehingga elektron valensinya = 1. Untuk mencapai konfigurasi elektron yang stabil (sesuai kaidah duplet) diperlukan 1 elektron. Konfiguarsi elektron 17Cl adalah 1s2 2s2 2p6 3s2 3p5 sehingga CI dan mempunyai elektron valensi = 7.
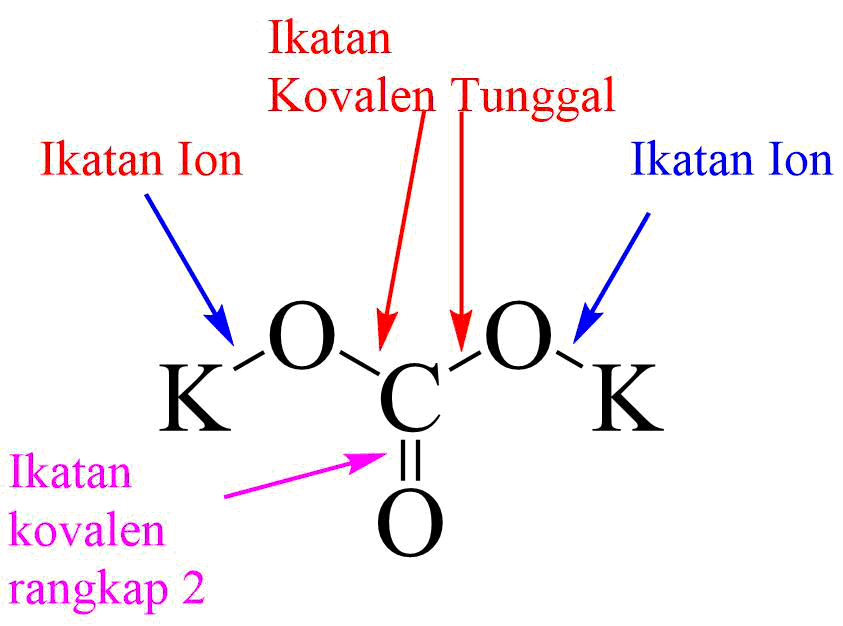
19 Contoh Senyawa yang Mempunyai Ikatan Ion dan Kovalen Sekaligus Materi Kimia
Berikut ini adalah penjelasan mengenai ikatan ion dan ikatan kovalen. 1. Ikatan Ion. Ikatan ion (elektrovalen) adalah ikatan yang terjadi antara ion positif dan ion negatif dalam suatu senyawa, dan terjadi serah terima elektron dari satu atom ke atom lain. Pada umumnya ikatan ion terbentuk antara atom logam yang mudah melepaskan elektron (ion.

Contoh Dari Senyawa Ion Dan Kovalen Garam dari unsur logam seperti licl , kcl ,mgcl2 , srbr2
Cara membuat Struktur Lewis sangat penting untuk memahami Ikatan Ion dan Ikatan Kovalen. Struktur Lewis adalah penggambaran distribusi elektron dalam struktur molekul dengan menggunakan tanda elektron.Tanda elektron bisa berupa tanda $\times$, tanda titik $\bullet$, dan lain-lain. Setiap unsur memiliki kecenderungan untuk mencapai konfigurasi.

IKATAN KIMIA Cara mudah belajar Ikatan Ion dan Ikatan Kovalen YouTube
untuk video lebih lengkap https://youtu.be/6D9tUV5urqosoal latihan 1: https://youtu.be/C2LOUZ7MV8M2:https://youtu.be/lzGbdwGVztY3:https://youtu.be/2EZytR_JqS.
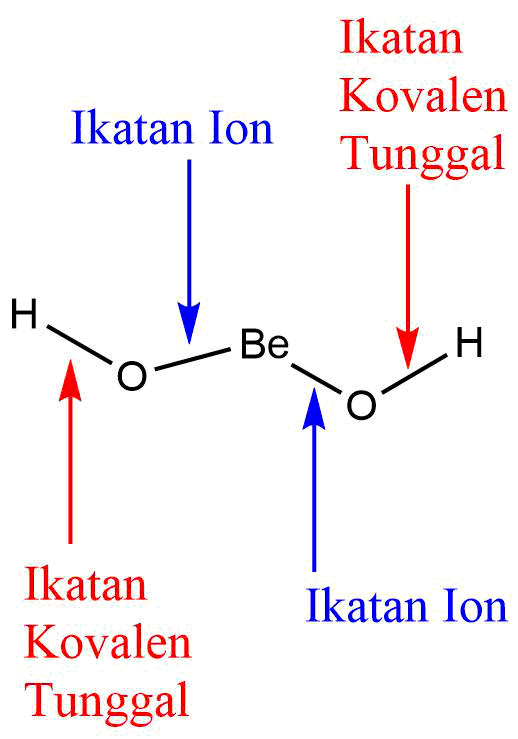
Ikatan Ion dan Kovalen Be(OH)2 MateriKimia
Ikatan Kovalen. Penyusun sesama atom unsur non logam. Tidak ada atom unsur logamn. N 2, CCl 2 , HCl, F 2 (tidak ada unsur logamnya, sehingga kovalen) Sedangkan NaCl = Na merupakan logam (ikatan Ion) Itulah ulasan tentang Ikatan Kovalen : Pengertian, Jenis, Dan Proses Pembentukan Beserta Contoh Secara Lengkap.
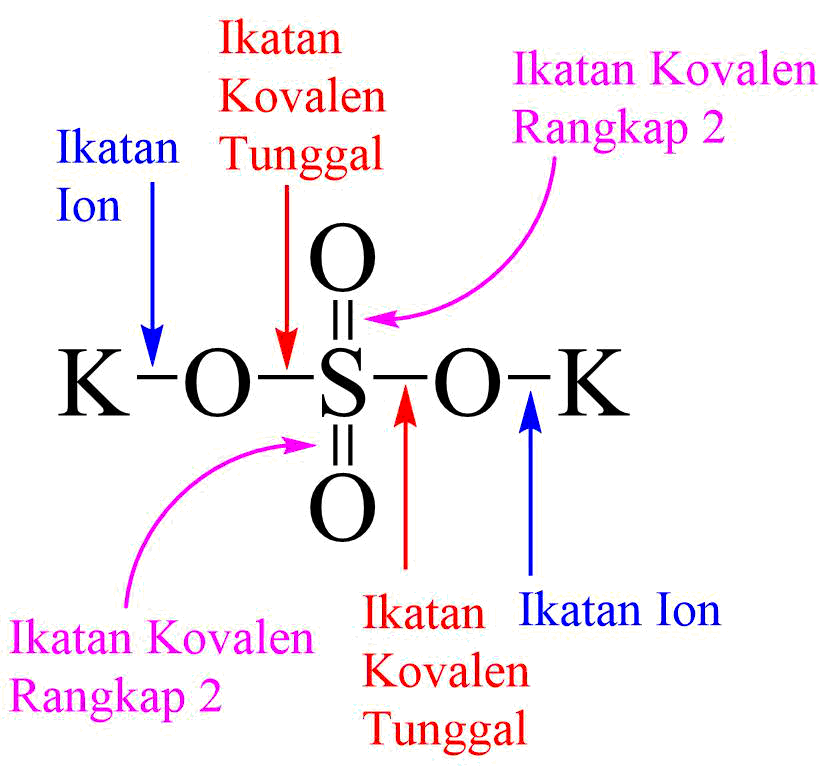
19 Contoh Senyawa yang Mempunyai Ikatan Ion dan Kovalen Sekaligus Materi Kimia
LAPORAN RESMI KIMIA SENYAWA ION DAN SENYAWA KOVALEN Oleh Kelompok 10 : Deya Hetri Safira (16030654022) Annisa Aura Lelyani (16030654028) Febrina Hanif Addaafi (16030654041) Karennina Putri A. (16030654057) UNIVERSITAS NEGERI SURABAYA JURUSAN IPA 2016/2017 FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM 1 Bab I Pendahuluan 1.1 Latar Belakang Di sekitar kita terdapat banyak zat ataupun senyawa.

Belajar Kimia Perbedaan Ikatan Kovalen dan Ikatan Ion antomatika
Ada tiga jenis ikatan Kimia, yaitu ikatan kovalen, ikatan logam dan ikatan ion. Sementara itu, dalam membentuk ion, suatu atom akan melepas atau mengikat elektron. Atom-atom yang mempunyai energi ionisasi rendah, misalnya atom-atom dari unsur golongan IA dan IIA dalam sistem periodik unsur akan mempunyai kecenderungan untuk melepaskan elektronnya.
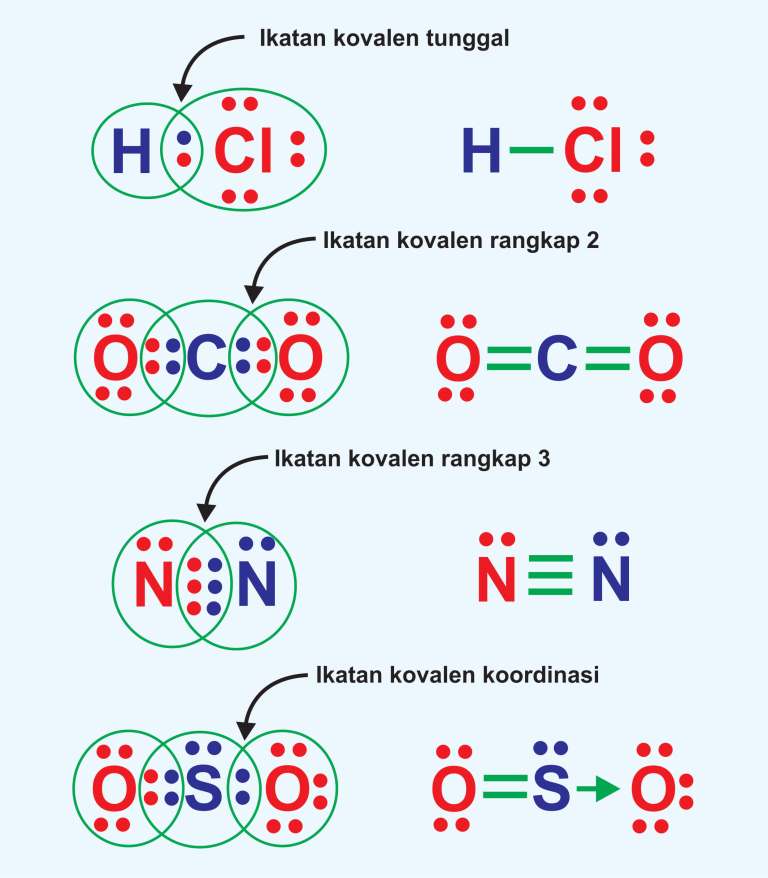
Ikatan Kimia Pengertian, Jenis, Sifat Fisis
Satu-satunya ikatan kovalen tulen berlaku antara atom yang sama. Biasanya, terdapat beberapa kekutuban (ikatan kovalen polar) di mana elektron dikongsi, tetapi menghabiskan lebih banyak masa dengan satu atom daripada yang lain. Ikatan ion terbentuk antara logam dan bukan logam. Ikatan kovalen terbentuk antara dua bukan logam.
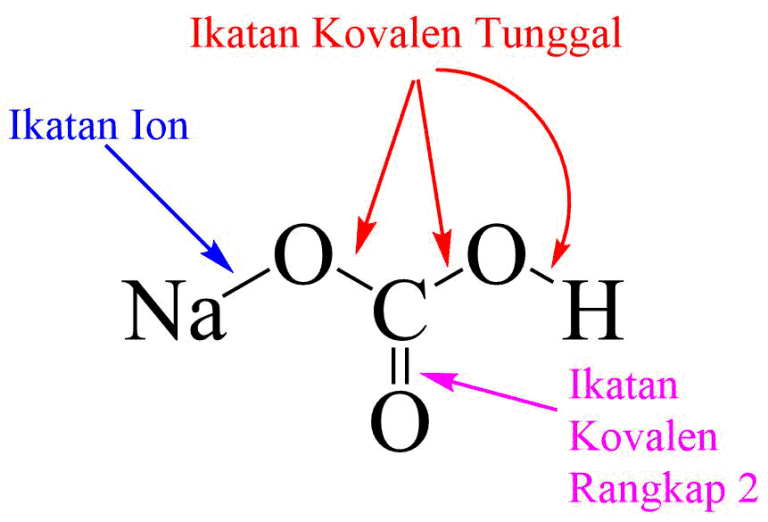
19 Contoh Senyawa yang Mempunyai Ikatan Ion dan Kovalen Sekaligus Materi Kimia
Kelebihan Ikatan Ion. 1. Ikatan ion cenderung memiliki kekuatan ikatan yang lebih kuat dan lebih stabil dibandingkan ikatan kovalen. 2. Senyawa dengan ikatan ion cenderung memiliki titik leleh dan titik didih yang tinggi, sehingga umumnya berwujud padat pada suhu kamar. 3.

Ikatan Ion Beserta Contoh Ikatannya Rumus Kimia
Kelebihan Senyawa Ion: 1. Stabilitas: Senyawa ion cenderung lebih stabil daripada senyawa kovalen karena adanya ikatan ionik yang kuat dan tidak mudah terurai. 2. Kekuatan: Senyawa ion memiliki kekuatan ikatan yang tinggi karena adanya tarikan elektrostatik antara ion-ion positif dan negatif. 3.
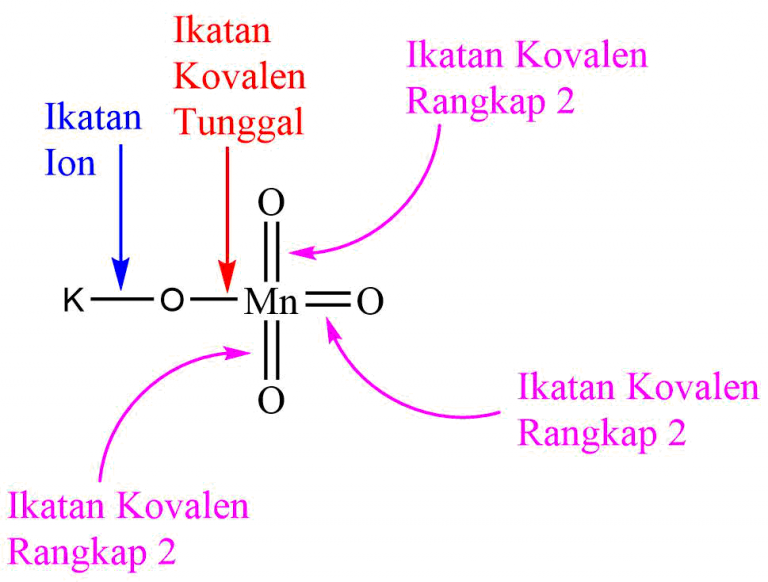
Ikatan Ion dan Kovalen KMnO4 MateriKimia
Satu-satunya ikatan kovalen murni terjadi antara atom identik. Biasanya, ada beberapa polaritas (ikatan kovalen polar) di mana elektron digunakan bersama, tetapi menghabiskan lebih banyak waktu dengan satu atom daripada yang lain. Ikatan ion terbentuk antara logam dan nonlogam. Ikatan kovalen terbentuk antara dua nonlogam.

perbedaan senyawa ion dan kovalen dan contohnya Pippa Poole
Perbedaan antara Ionik dan Kovalen adalah sementara keduanya adalah proses ikatan kimia, yang pertama mengacu pada ikatan di mana atom menarik atom-atom yang berlawanan dengan gaya tariknya.. Proses ini sebagian besar terjadi antara ion logam dan non-logam karena keduanya memiliki muatan yang berlawanan. Sedangkan di sisi lain, ikatan.
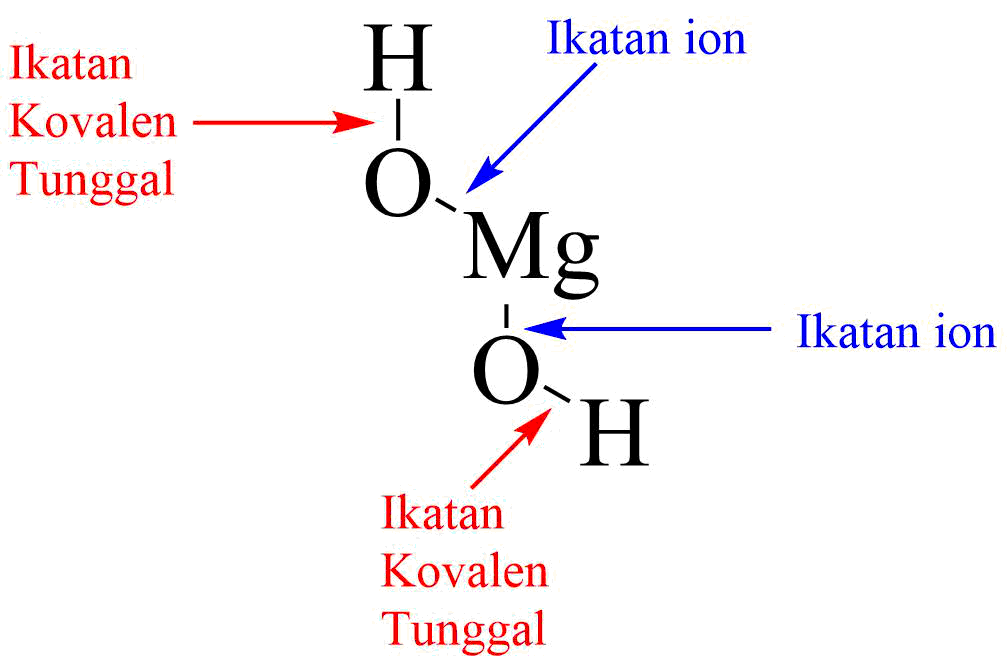
19 Contoh Senyawa yang Mempunyai Ikatan Ion dan Kovalen Sekaligus Materi Kimia
Temukan perbedaan mendasar antara ikatan ion dan kovalen dalam dunia kimia. Ikatan ion terbentuk melalui transfer elektron antara atom, sementara ikatan kovalen terjadi melalui pembagian elektron. Kenali sifat-sifat uniknya dan pengaruhnya pada stabilitas dan sifat kimia zat-zat yang membentuknya. Pelajari juga contoh-contoh konkrit dari kedua jenis ikatan ini untuk pemahaman yang lebih.

Ikatan Kimia Kelas 10 • Part 6 Pembahasan Contoh Soal Ikatan Ion dan Kovalen (1) YouTube
Contoh senyawa ion meliputi garam dapur (NaCl) dan natrium sulfat (Na2SO4), sementara contoh senyawa kovalen mencakup air (H2O) dan metana (CH4). Senyawa ion umumnya ditemukan dalam mineral, sementara senyawa kovalen banyak terkandung dalam zat organik dan molekul biologis. 7. Reaktivitas Kimia.

Ikatan Ionik dan Kovalen, dan Cara Membaca Diagram Energi Pembentukan Ikatan YouTube
Semua yang ada di dunia ini memiliki sifat-sifatnya masing-masing. Begitu juga dengan senyawa ion dan kovalen. Mereka juga memiliki sifatnya sendiri sehingga bisa menjadi pembeda dengan senyawa yang lain. Sifat senyawa ion maupun sifat senyawa kovalen dapat kita jabarkan sebagai berikut. 1. Sifat-sifat senyawa ion Titik didih dan titik leleh tinggi Mudah larut dalam pelarut