
DipolDipolWechselwirkung • Ursache, Dipolmoment · [mit Video]
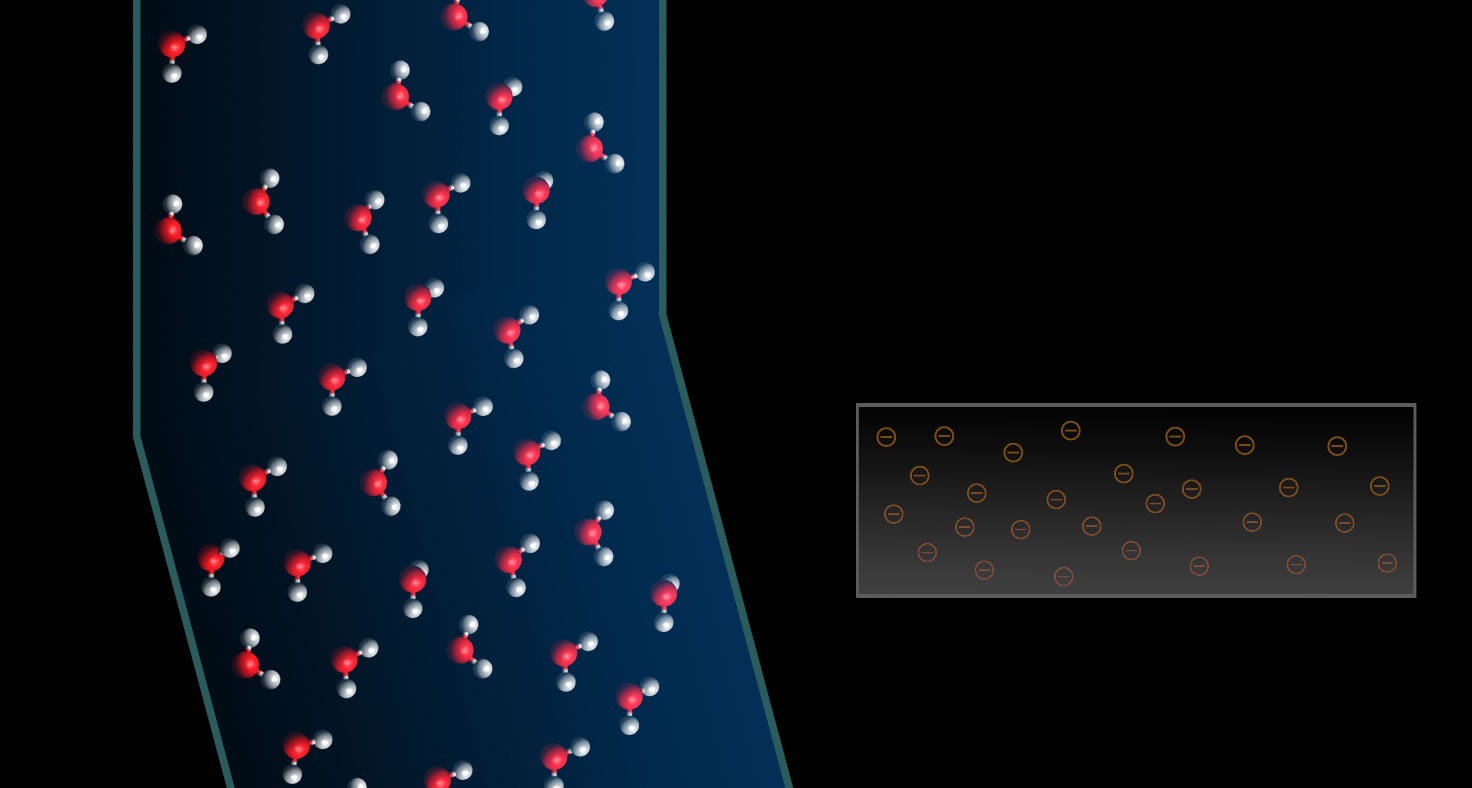
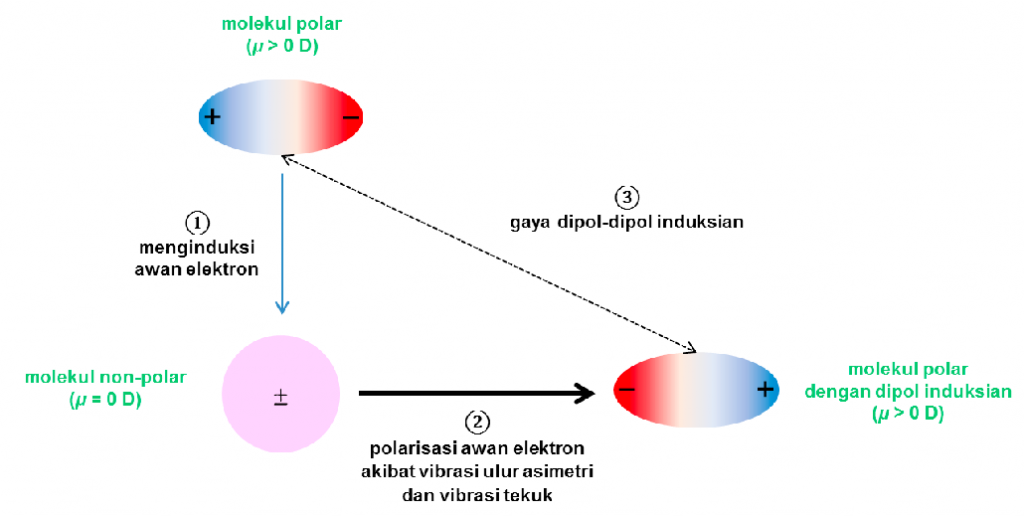
Interaksi dipol-dipol terinduksi. Molekul dipol dapat membuat molekul netral lain yang bersifat dipol terinduksi sehingga terjadi interaksi dipol-dipol terinduksi dan ikatannya relatif lemah sehingga prosesnya berlangsung secara lambat.Antar aksi dipol terinduksi-dipol terinduksi (gaya london) Gaya Van der Waals bersifat permanen sehingga lebih.
MATERI KELAS 10 GAYA INTERAKSI MOLEKUL
Interaksi ion-dipol; Interaksi ini terjadi karena adanya tarik-menarik antara ion dengan molekul polar yang relatif kuat. Interaksi ini digunakan untuk menentukan kelarutan. Interaksi dipol-dipol; Gaya dipol dipol ini terjadi antar sesama molekul polar yang terjadi pada ekor dan kepala molekul itu sendiri.
DipolDipolWechselwirkung
Suatu contoh interaksi dipol-dipol dapat dilihat pada asam klorida (HCl), dimana ujung positif suatu molekul polar akan saling menarik dengan ujung negatif molekul lain dan mempengaruhi posisinya. Untuk semakin memahami interaksi dipol-dipol permanen, Wardaya College memberikan beberapa pembelajaran yang bisa kamu gunakan sebagai pedoman. Tak.

(PDF) CONTOH INTERAKSI DIPOLDIPOL PADA ANTAR MOLEKUL POLAR Hanif Ratih Academia.edu
In chemical bonding: Dipole-induced-dipole interaction..type of attractive interaction, the dipole-induced-dipole interaction, also depends on the presence of a polar molecule. The second participating molecule need not be polar; but, if it is polar, then this interaction augments the dipole-dipole interaction described above.

gaya interaksi dipoldipol!!!!. YouTube
Video kali ini kita akan membahas tentang konsep interaksi dari ion-dipol. Secara general interaksi ion-dipol terbagi menjadi 2 yaitu bagaimana suatu ion ber.
PPT Chapter 11 PowerPoint Presentation, free download ID5852920
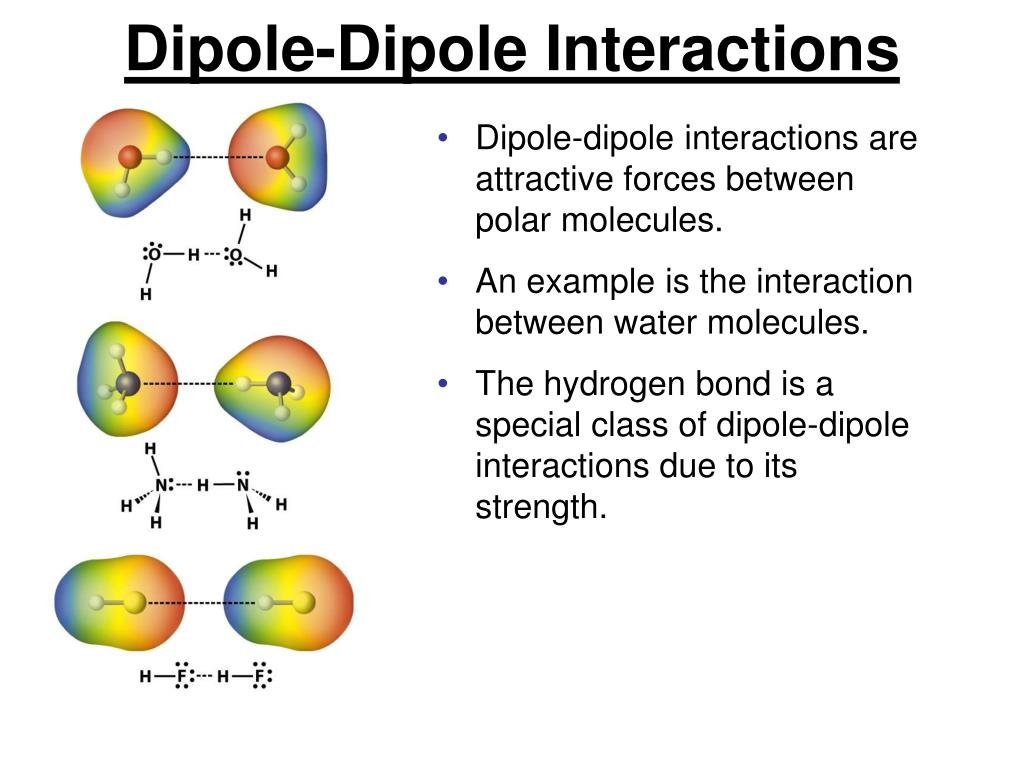
Interaksi dipol-dipol adalah interaksi yang diamati antara dipol positif dari satu molekul polar dan dipol negatif dari yang lain. Dalam ikatan kovalen polar, atom dengan elektronegativitas tertinggi menarik elektron ke arah dirinya sendiri, membentuk dipol negatif di sekitarnya. Dalam atom dengan elektronegativitas lebih rendah, dipol yang.

INTERAKSI IONDIPOL YouTube
Other articles where dipole-dipole interaction is discussed: chemical bonding: Dipole-dipole interaction:.interactions discussed here is the dipole-dipole interaction between polar molecules. It will be recalled that a polar molecule has an electric dipole moment by virtue of the existence of partial charges on its atoms. Opposite partial charges attract one another, and, if two polar.
DipoleDipole Interactions — Definition & Overview Expii
KOMPAS.com - Gaya antarmolekul adalah gaya yang terjadi di antara atom-atom sehingga dapat membentuk molekul ataupun senyawa tertentu.. Gaya antarmolekul terdiri dari gaya London atau dipol-dipol, gaya Van der Waals, dan ikatan hidrogen.Simak penjelasannya seperti dikutip dari Encyclopaedia Britannica:. Gaya London. Gaya london adalah gaya tarik menarik antaratom karena adanya dipol sesaat.
DipolDipolWechselwirkung
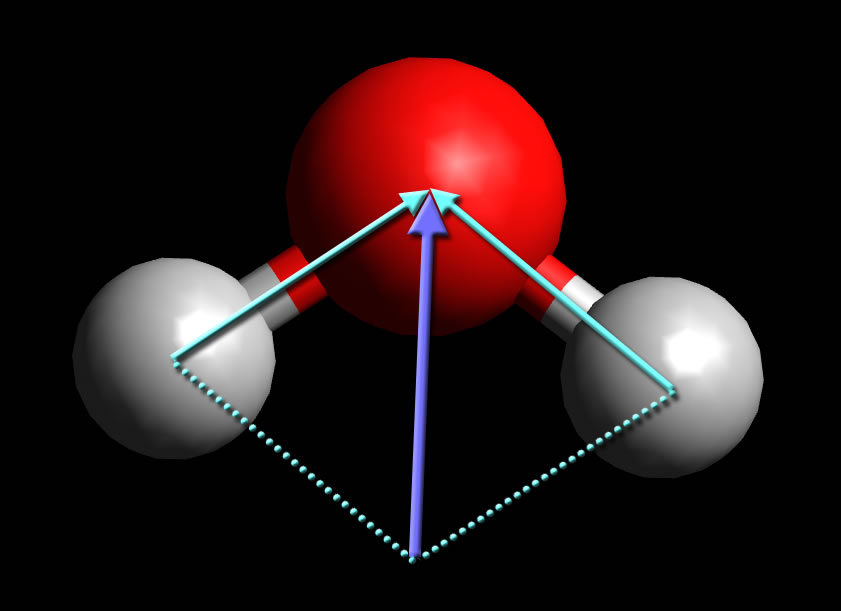
A molecule's overall dipole is directional, and is given by the vector sum of the dipoles between the atoms. If we imagined the Carbon Dioxide molecule centered at 0 in the XY coordinate plane, the molecule's overall dipole would be given by the following equation: μ cos(0) + −μ cos(0) = 0. (1) (1) μ cos ( 0) + − μ cos ( 0) = 0.
PPT Chapter 11 Intermolecular Forces, Liquids, and Solids PowerPoint Presentation ID3613054
Pengertian Gaya Dipol-dipol Gaya dipol-dipol adalah gaya tark menarik antara sisi positif molekul polar dengan sisi negatif molekul polar lainnya. Gaya dipol-dipol mempunyai kekuatan yang berkisar antara 5-20 kJ per mol. Gaya ini lebih lemah dibandingkan ikatan kovalen atau ikatan ion, dan mempunyai pengaruh yang signifikan hanya ketika molekul-molekul saling berdekatan. Perhatikan gaya dipol.

(DOC) GAYA ANTAR MOLEKUL PADATAN DAN CAIRAN A.GAYA DIPOLDIPOL Indra Christian Academia.edu
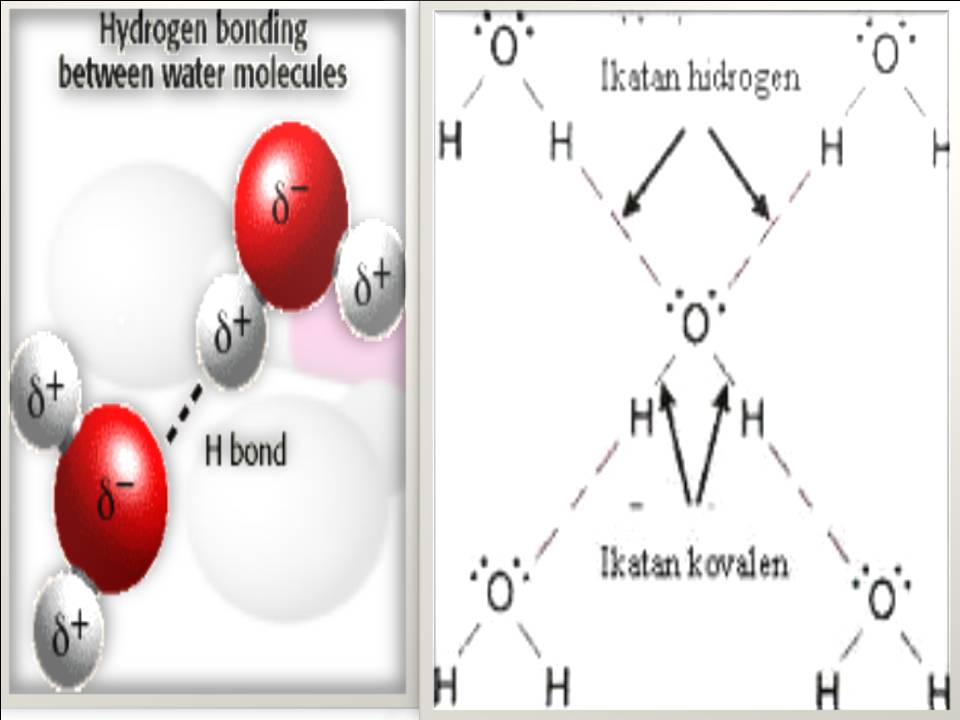
Melaui pengamatan ini semua, dapat kita pahami bahwa ikatan hidrogen adalah jenis ikatan yang terbentuk dari interaksi dipol-dipol yang memiliki atom H yang terikat pada N, O, dan F seperti pada H 2 O, NH 3, HF, CH 3 OH, dll. Pembahasan Laba-laba dan Jarum. Laba-laba Berdiri di Atas Permukaan Air:

Dipoldipolbindningar YouTube
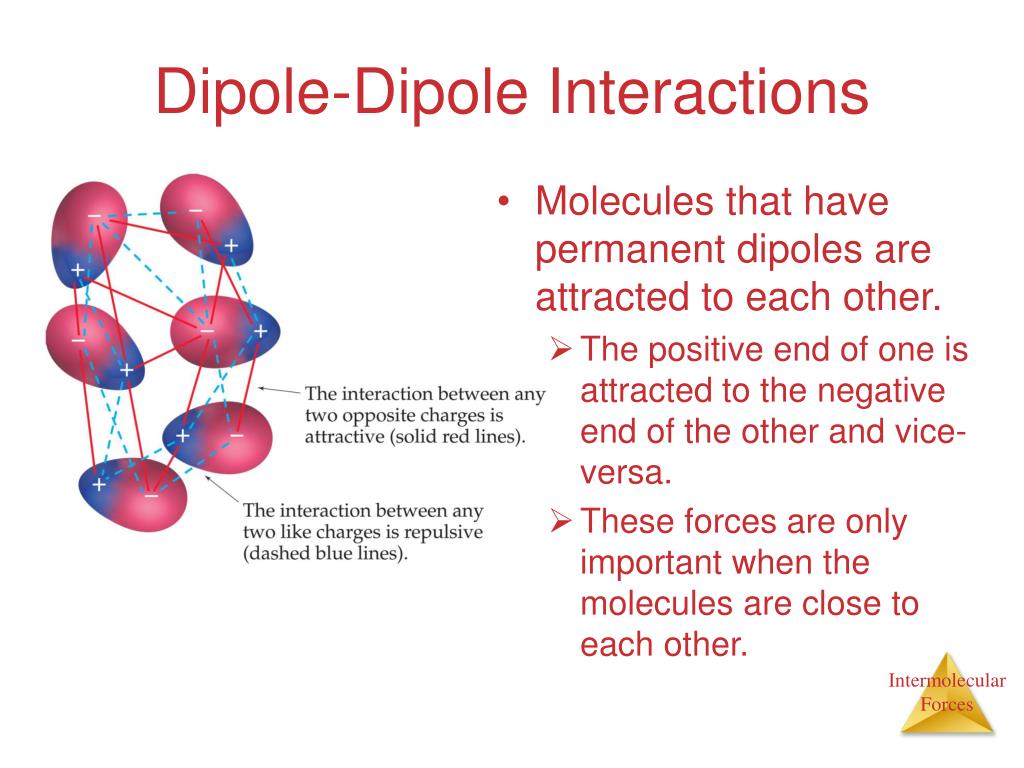
Dipole-dipole forces are attractive forces between the positive end of one polar molecule and the negative end of another polar molecule. Dipole-dipole forces have strengths that range from 5 kJ to 20 kJ per mole. They are much weaker than ionic or covalent bonds and have a significant effect only when the molecules involved are close together.

Ikatan dipol momen Interaksi dipoldipol Gaya antarmolekul Kimia, lainnya, sudut, teks
Interaksi Dipol Permanen. Selamat Datang dan Selamat Belajar di Wardaya College! Di sini, kamu akan belajar tentang Interaksi Dipol Permanen melalui latihan soal interaktif dalam 3 tingkat kesulitan (mudah, sedang, sukar). Apabila materi ini berguna, bagikan ke teman atau rekan kamu supaya mereka juga mendapatkan manfaatnya.
Memahami Senyawa Koordinasi dari Ikatan Kovalen dan Ikatan NonKovalen
Dipol-Dipol adalah gaya tarik menarik antara molekul polar dengan molekul polar. Contohnya, interaksi antar molekul HCl. Ion-dipol adalah gaya tarik menarik antara ion dengan molekul polar. Contohnya, interaksi antara molekul air dengan ion Al 3+ dalam larutan AlCl 3. Setiap ion Al 3+ akan dikelilingi oleh 6 molekul air.

Intermolecular Forces Description, Types of Forces Embibe
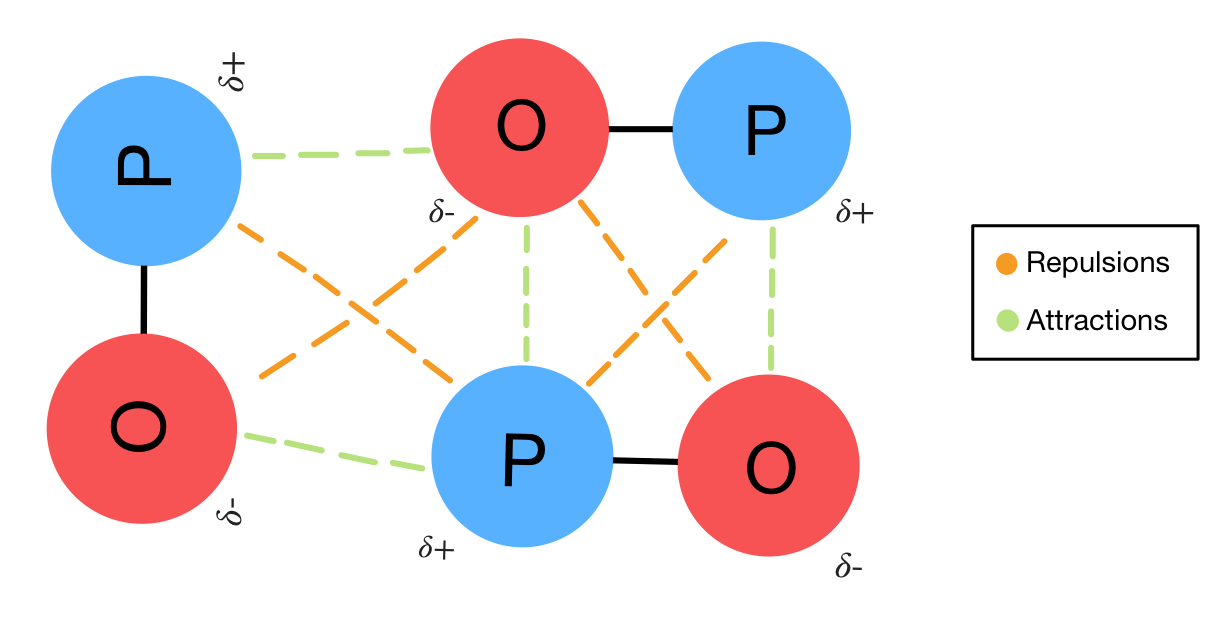
Gaya dipol-dipol Gaya dipol-dipol merupakan interaksi elektrostatik antara molekul-molekul polar (dwikutub). Dua orientasi dipol-dipol dengan muatan yang berlawanan menghasilkan gaya dipol-dipol. Gaya dipol-dipol ini lebih lemah dari ikatan ion dan ikatan kovalen, sehingga memiliki titik didih dan titik leleh lebih rendah.
DipolDipol Etkileşimleri Ders Kitabı Cevapları
Latihan Soal Gaya Dipol Permanen (Sedang) Pertanyaan ke 1 dari 5. 1. Pertanyaan. Berikut ini hubungan yang tepat antara interaksi antar dipol dan gaya London sehubungan dengan sifat fisis senyawa adalah.. 1. Titik didih hanya dipengaruhi oleh gaya London. 2. Titik didih hanya dipengaruhi oleh interaksi antar dipol.