
Ikatan Kovalen Koordinasi Kimia Kelas 10 YouTube
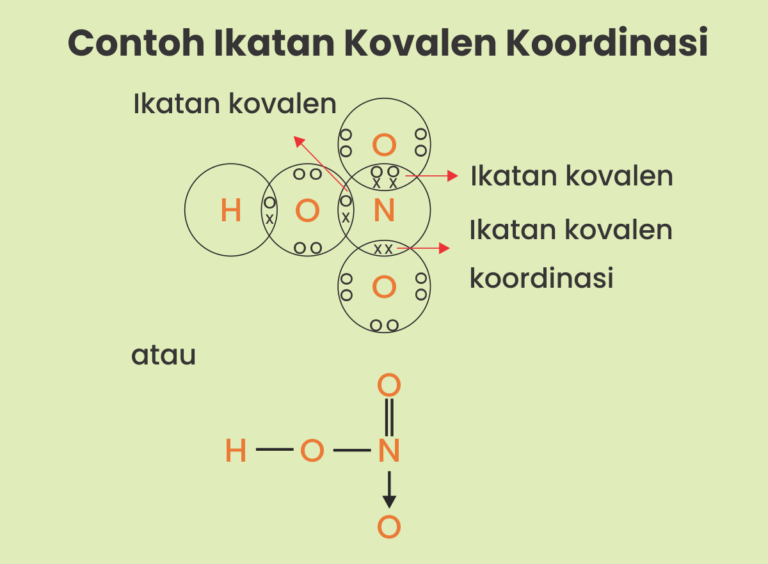
Contoh senyawa dengan ikatan kovalen koordinasi adalah HNO3 atau yang lebih dikenal sebagai asam nitrat. Dalam molekul HNO3 terdapat 3 ikatan kovalen dan 1 ikatan kovalen koordinasi. Baca juga: Jenis-Jenis Ikatan Kimia. NH4Cl. Senyawa NH4Cl terbentuk dari ion NH4+ dan ion Cl-. Ion NH4+ terbentuk dari molekul NH3 dan ion H+. Sedangkan, ion H+.

Contoh Soal Ikatan Kovalen Koordinasi Dan Pembahasannya Gif Auto My XXX Hot Girl
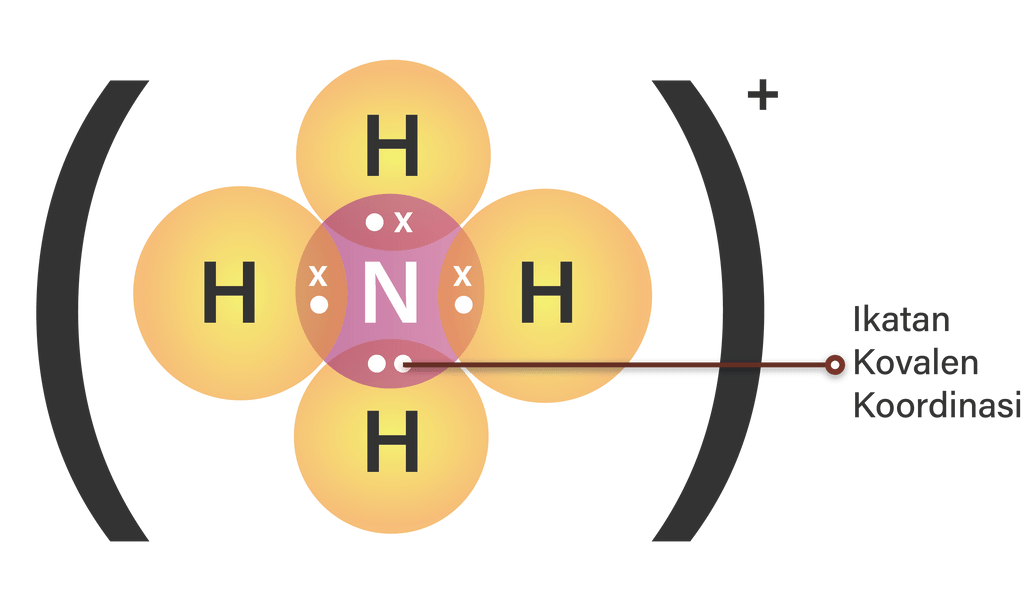
Contoh. Sebagai contoh ikatan kovalen koordinasi adalah senyawa amonia, NH 3, terdiri atas tiga pasangan elektron sekutu untuk tiga ikatan kovalen tunggal N-H. Namun karena atom N memiliki lima elektron valensi, maka masih tersedia sepasang elektron bukan ikatan atau sepasang elektron menyendiri (lone pair electron).Jika molekul NH 3 bergabung dengan ion H + (hidrogen tanpa elektron) membentuk.

Cara Identifikasi Keberadaan Ikatan Kovalen Koordinasi pada Suatu Molekul Serba Ada
Ikatan kovalen adalah ikatan yang terbentuk dari pemakaian bersama pasangan elektron oleh dua atau lebih atom non logam. Ikatan kovalen ini dibedakan berdasarkan jumlah pasangan elektron dan kepolarannya. Agar lebih jelas, artikel ini akan membahas seputaran ikatan kovalen, mulai dari pengertian, jenis, sifat, hingga cara menggambar ikatan ini.

Diantara kelompok senyawa berikut yang kesemuanya terdapat ikatan kovalen koordinasi adalah
Ikatan kovalen koordinasi adalah interaksi antara basa Lewis dengan Asam Lewis. Basa Lewis yang memiliki pasangan elektron bebas menyumbang elektronnya kepada Asam Lewis. seperti NH3 terhadap ion H+ membentuk NH4+. contoh2 diatas H2SO4, HNO3 dsb bukan merupakan ikatan KOvalen koordinasi. ikatan kovalen koordinasi umum nya terjadi senyawa.
Ikatan Kovalen Nonpolar, Polar dan Koordinasi Siswapedia
Ikatan kovalen koordinasi; Ikatan kovalen polar dan nonpolar; Ikatan tersebut selanjutnya akan dijabarkan yaitu sebagai berikut. a. Ikatan Kovalen Tunggal. Ikatan kovalen tunggal adalah ikatan kimia yang terjadi karena penggunaan satu pasang elektron secara bersama-sama oleh atom penyusunnya. Ikatan ini dituliskan dengan garis tunggal.

Ikatan Kovalen Koordinasi, Kenali Pengertian dan Contohnya
Contoh senyawa yang memiliki ikatan kovalen koordinasi adalah HNO3, NH4Cl, SO3, dan H2SO4. Ciri dari ikatan kovalen koordinasi adalah pasangan elektron bebas dari salah satu atom yang dipakai secara bersama-sama seperti pada contoh senyawa HNO3 berikut ini. Tanda panah ( —>) menunjukkan pemakaian elektron dari atom N yang digunakan secara.

Cara mudah menentukan Ikatan Kovalen Koordinasi YouTube
Ikatan kimia adalah sebuah proses fisika yang bertanggung jawab dalam interaksi gaya tarik menarik antara dua atom atau molekul yang menyebabkan suatu senyawa diatomik atau poliatomik menjadi stabil.. Ikatan kovalen koordinasi Ikatan kovalen koordinasi, kadang kala disebut sebagai ikatan datif, adalah sejenis ikatan kovalen yang keseluruhan.
Ikatan kovalen koordinasi dijumpai pada molekul io...
Kovalen Koordinasi adalah salah satu topik dalam bab Ikatan Kimia kelas 10 kurikulum 2013. Video ini membahas ikatan kovalen koordinasi pada HNO3 dan SO3..

Animasi Ikatan Kovalen Koordinasi YouTube
Untuk molekul dan ion poliatomik, bilangan koordinasi suatu atom ditentukan cukup dengan menghitung jumlah atom yang terikat dengan atom pusat (oleh ikatan tunggal atau ganda). [1] Contohnya, di dalam kompleks [Cr (NH 3) 2 Cl 2 Br 2] −, Cr 3+ adalah kation pusatnya dan memiliki bilangan koordinasi sebesar 6.
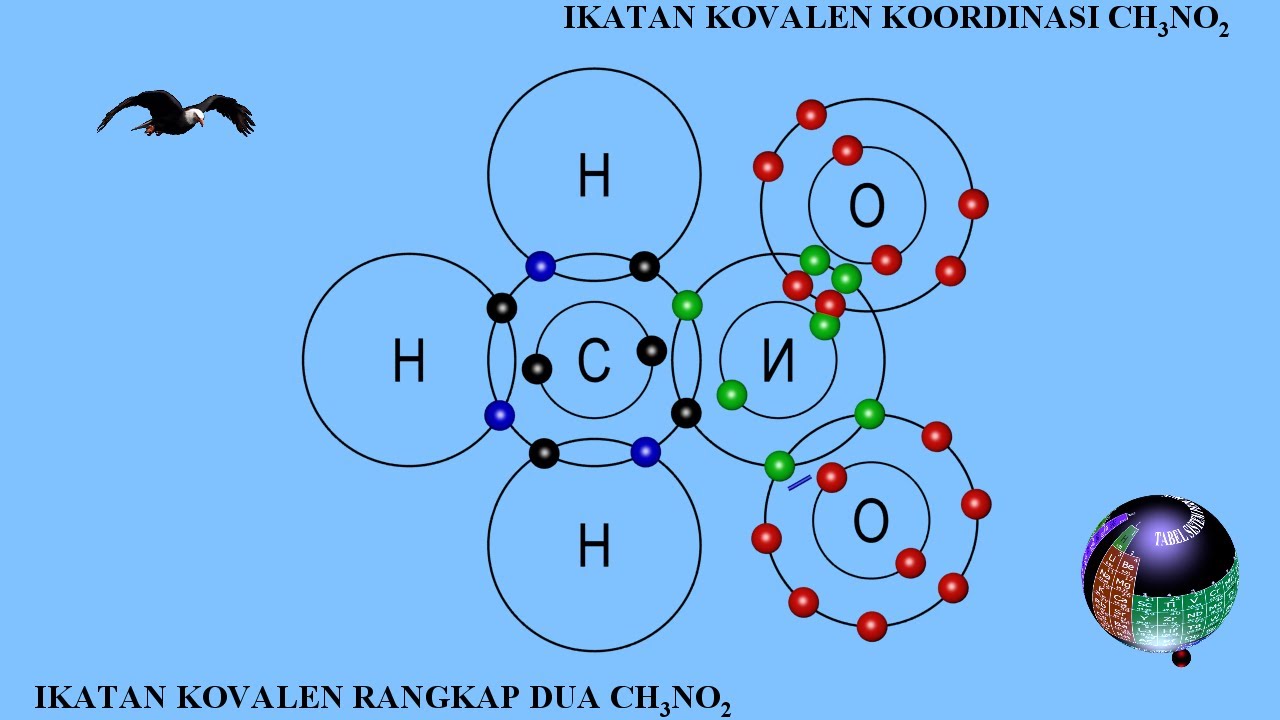
IKATAN KOVALEN KOORDINASI DAN IKATAN KOVALEN RANGKAP DUA CH3NO2 (NITRO METANA) YouTube
Ikatan kovalen koordinasi. Ikatan kovalen koordinasi adalah ikatan yang memakai pasangan elektron bersama, namun elektronnya hanya berasal dari salah satu atom. Contohnya adalah pembentukan ozon atau O3. Agar semua atom dapat memenuhi aturan oktet, maka salah satu atom yang berada di tengah harus menyumbangkan dua elektronnya untuk digunakan.

Menentukan Ikatan Kovalen Koordinasi YouTube
Ikatan kovalen koordinasi merupakan jenis ikatan kovalen yang dapat dibedakan dari sumber elektron dengan penggunaannya bersamaan. Ikatan ini terjadi apabila ada satu atom yang memberikan pasangan elektron. Sehingga atom pasangannya tidak dapat memberikan elektron. Jenis ikatan ini hanya akan terjadi pada unsur-unsur non logam.

Kimia Kelas X Ikatan Kovalen Koordinasi. YouTube
Ketika dua atom atau ion "berpegangan" dengan sangat erat, dapat dikatan bahwa di antaranya terdapat suatu ikatan kimia. Dalam pembentukannya, yang berperan adalah elektron valensi, yaitu elektron yang berada pada kulit terluar.Untuk memudahkan penggambaran elektron valensi pada atom suatu unsur dan ikatan yang terbentuk dapat digunakan simbol Lewis (simbol titik-elektron Lewis).

Bagaimana Ikatan Kovalen Koordinasi SO3 (Sulfur Trioksida) Terbentuk ? YouTube
Ikatan kovalen koordinasi, juga disebut sebagai ikatan datif, ikatan dipolar, atau ikatan koordinat adalah suatu jenis ikatan kovalen dua pusat, dua elektron yang kedua elektron tersebut berasal dari atom yang sama. Pengikatan ion logam pada ligan melibatkan jenis interaksi ini. Jenis pengikatan ini menjadi hal yang penting pada teori asam-basa Lewis.
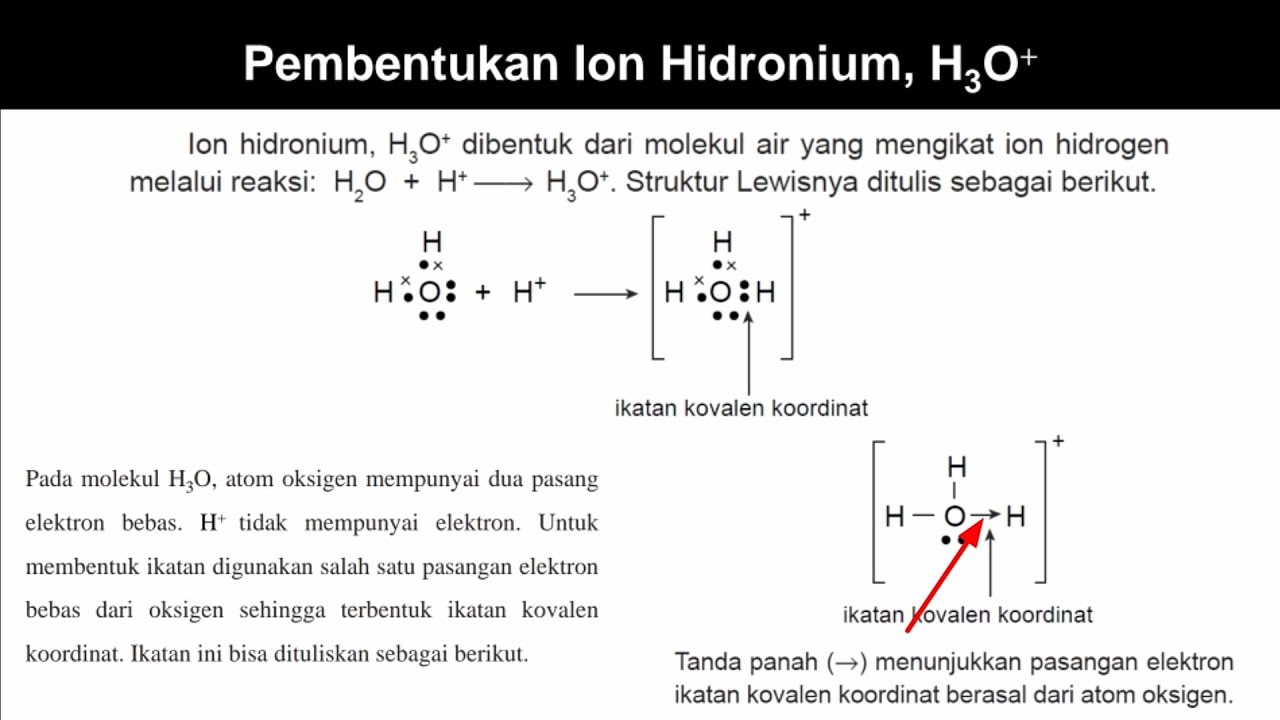
Bagaimana Ikatan Kovalen Koordinasi H3O+ (Hidronium) Terbentuk ? YouTube
Ikatan kovalen koordinasi. Ikatan kovalen koordinasi, [1] juga disebut sebagai ikatan datif, [2] ikatan dipolar, [3] atau ikatan koordinat [4] adalah suatu jenis ikatan kovalen dua pusat, dua elektron yang kedua elektron tersebut berasal dari atom yang sama. Pengikatan ion logam pada ligan melibatkan jenis interaksi ini. [5]

IKATAN KOVALEN & IKATAN KOVALEN KOORDINASI YouTube
Sebagai contoh ikatan kovalen koordinasi adalah senyawa amonia, NH 3, terdiri atas tiga pasangan elektron sekutu untuk tiga ikatan kovalen tunggal N-H. Namun karena atom N memiliki lima elektron valensi, maka masih tersedia sepasang elektron bukan ikatan atau sepasang elektron menyendiri (lone pair electron).
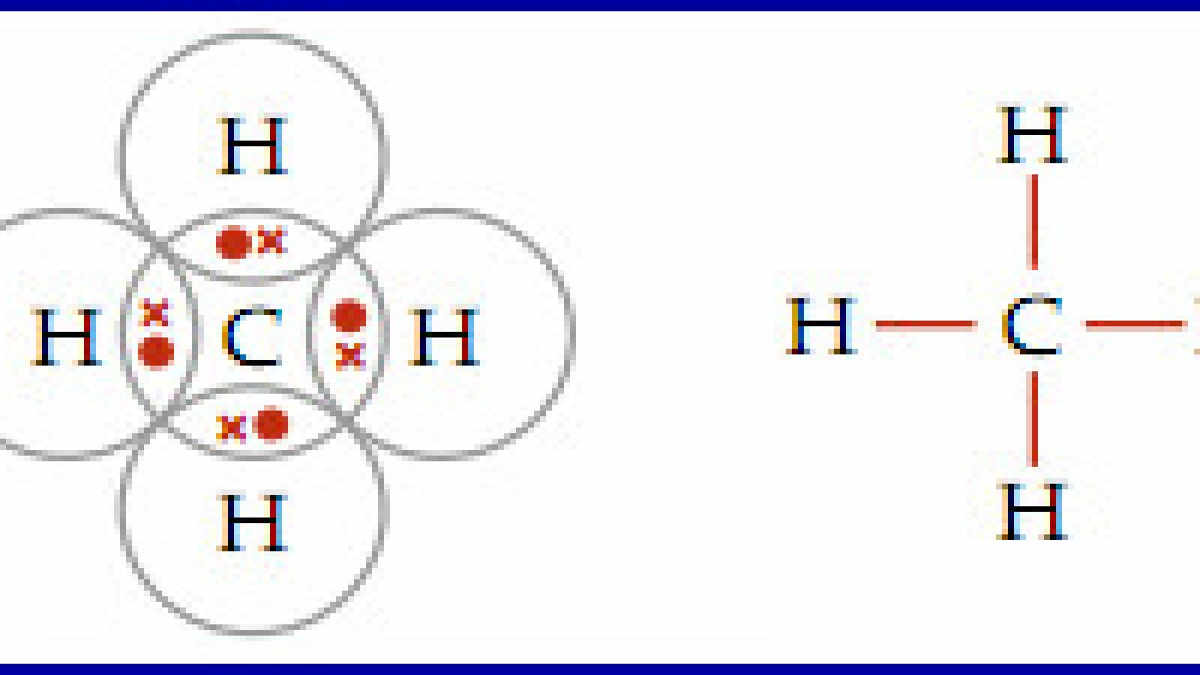
Senyawa yang Memiliki Ikatan Kovalen Tunggal dan Koordinasi
Ikatan kovalen koordinasi terjadi ketika elektron-elektron yang digunakan untuk berikatan berasal dari salah satu unsur yang berikatan. Contoh ikatan kovalen koordinasi terdapat pada ion-ion dan senyawa-senyawa berikut. NH4+, HNO3, SO3, H2SO4, H3O+, H3NBF3, POCl3, HClO4, SO2Br2, N2O. 1. Ikatan Kovalen Koordinasi NH4+ 2. Ikatan Kovalen Koordinasi HNO3 3.