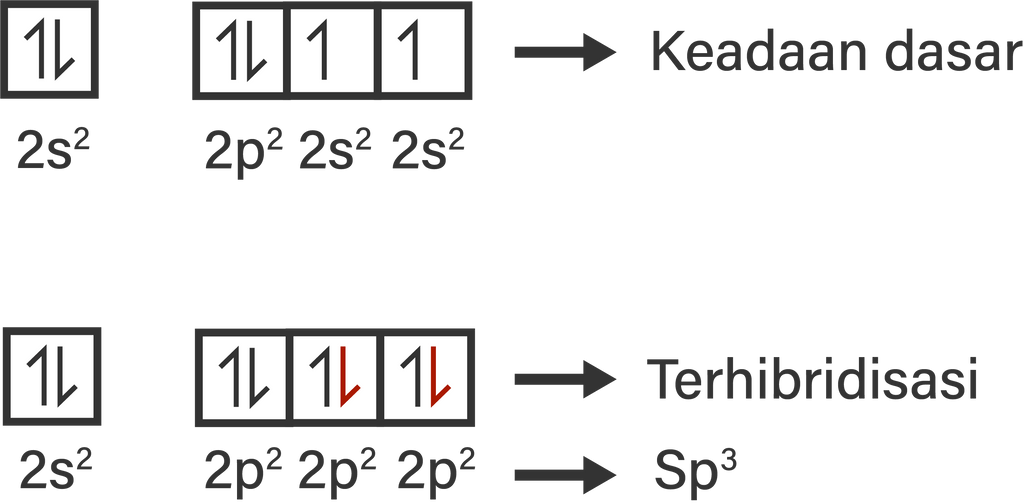
Tentukan hibridisasi yang terjadi pada atom pusat
Bentuk hibridisasi dari SF6 (nomor atom S=16) adalah. O Sp3d1 O Sp3d2 O Sp4d3 O Sp3 O Sp2. Untuk menentukan hibridisasi dapat menggunakan 2 cara, berikut adalah uraiannya: Cara 1: 🔸Konfigurasi atom pusat Atom pusat pada senyawa SF₆ adalah unsur S, maka konfigurasi elektronnya adalah ₁₆S = [Ne] 3s² 3p⁴ 🔸 Hibridisasi pada.
.jpg)
Hibridisasi Sf4 Brain
Bentuk molekul salah satunya dapat ditentukan berdasarkan teori hibridisasi. Berdasarkan teori hibridisasi, ada 5 bentuk molekul yaitu: Linear (sp), trigonal planar (sp²), tetrahedral (sp³), segitiga bipiramida (sp³d), dan oktahedral (sp³d²). Dengan demikian, karena hibridisasi SF6 adalah sp³d² maka bentuk molekulnya adalah oktahedral.

BENTUK MOLEKUL SENYAWA VSEPR dan HIBRIDISASI YouTube
Elo bisa coba berlangganan Zenius Aktiva karena ada ratusan soal tentang bentuk molekul mulai dari CO2, SF6, BeCl2 dan beragam bentuk molekul lainya. Klik banner di bawah ya! Sekian materi tentang hibridisasi molekul dari gue, semoga dengan membaca artikel ini elo jadi lebih paham dan bisa mendapat nilai maksimal ketika ujian.

Kimia Kelas X Pembahasan Soal Materi Bentuk Geometri Molekul, Teori Domain elektron
SF6 (Sulphur Hexafluoride) - Characteristics, Hybridization and Geometry. Sulphur hexafluoride is a non-toxic, non-flammable greenhouse gas that is colorless and odorless. It is inorganic and non-polar. SF6 is normally made by exposing or combining S8 with F2.
Menentukan Jenis Hibridisasi, Bentuk Molekul dan Letak Atom O dalam Molekul SOF4 Urip dot Info
Ini sesuai keunikan S yang memiliki subkulit 3d yang kosong. S {-6+6} + 6 (F {-1+1}) ⇒ SF 6. Hibridisasi Atom S, Bentuk Molekul, dan Kepolaran SF2. Detil yang khusus membahas tentang hibridisasi, bentuk molekul, dan kepolaran senyawa silakan disimak di sini. Bentuk dasar (geometri elektron, semua pasangan elektron diperhatikan) SF 2.

Bentuk molekul 10 SMA (Teori hibridisasi molekul) YouTube
SF6 Geometry and Hybridization. Sulfur is the central atom: There are 6 + 6×7 = 48 valence electrons, and 12 are taken for making 6 covalent bonds. Each fluorine takes three lone pairs, so there are no electrons left: 48 - (12 + 6×6) = 0. The central atom has 6 atoms connected to it, and no lone pairs, therefore, both geometries are octahedral:
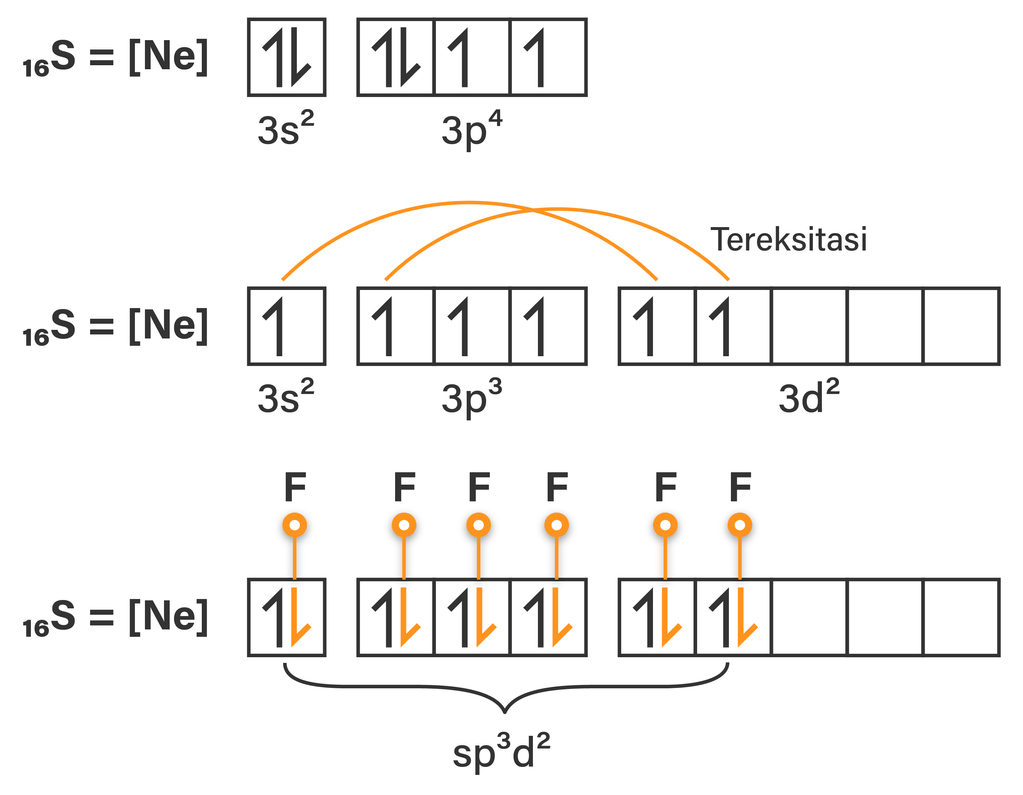
jelaskan proses hibridisasi molekul SF6...
Sulfur hexafluoride or sulphur hexafluoride (British spelling) is an inorganic compound with the formula SF 6.It is a colorless, odorless, non-flammable, and non-toxic gas.SF 6 has an octahedral geometry, consisting of six fluorine atoms attached to a central sulfur atom. It is a hypervalent molecule.. Typical for a nonpolar gas, SF 6 is poorly soluble in water but quite soluble in nonpolar.

Sf6 Molecule
The Lewis structure of SF6 (sulfur hexafluoride) consists of a central sulfur atom bonded to six fluorine atoms.The sulfur atom has six valence electrons, while each fluorine atom contributes one valence electron.; The Lewis structure shows that SF6 has a total of 12 valence electrons, with all atoms achieving an octet configuration.; SF6 is a highly stable and nonpolar molecule due to its.

Teori Hibridisasi Pelajaran Kimia
Hello Guys!Today in this video, we are going to learn the hybridization of the SF6 molecules. It is a chemical formula for Sulfur Hexafluoride. To understand.
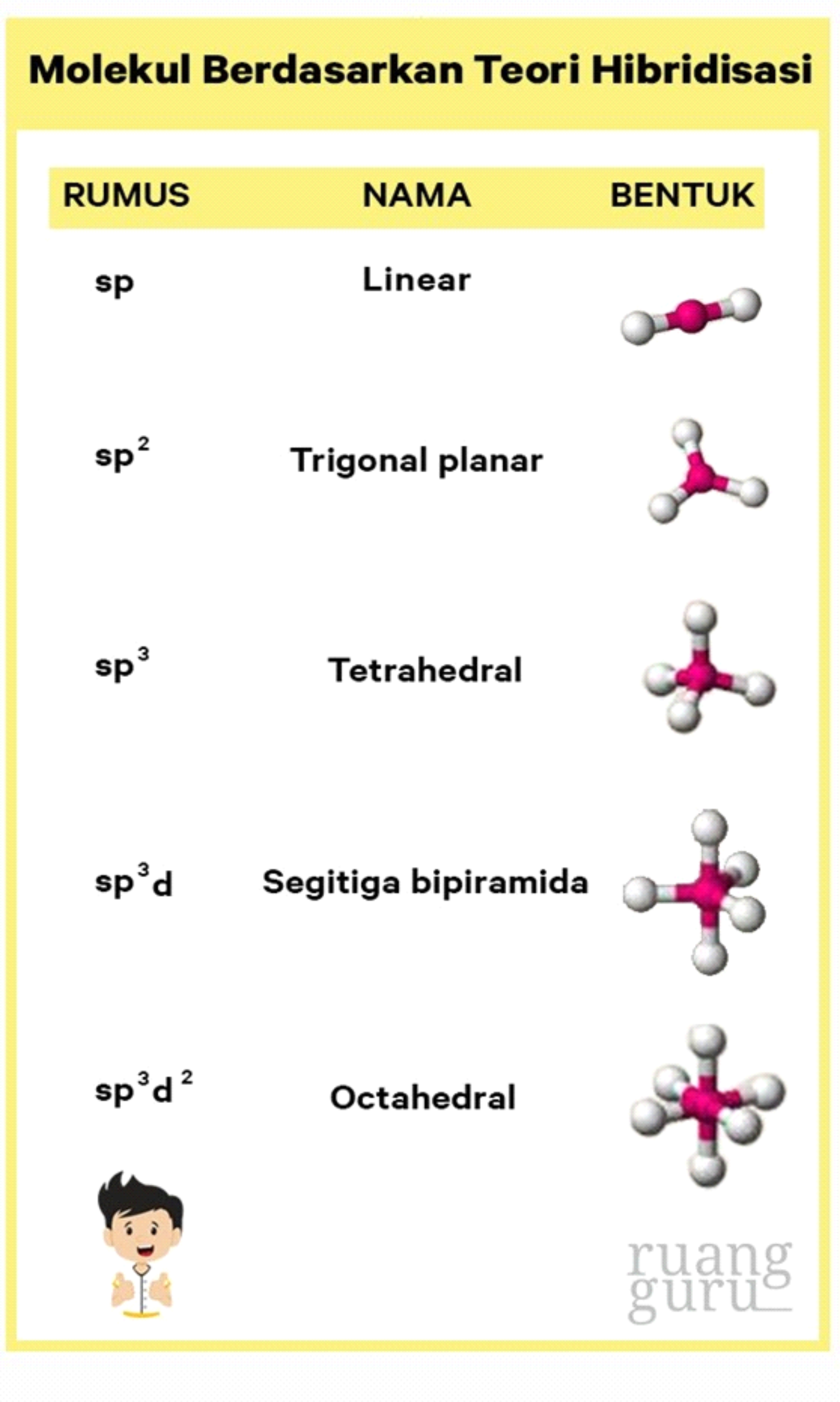
Mengenal Apa Itu Hibridisasi Pengertian Teori Dan Macam Macamnya Kids Images
This organic chemistry video tutorial explains the hybridization of atomic orbitals. It discusses how to determine the number of sigma and pi bonds in a mol.
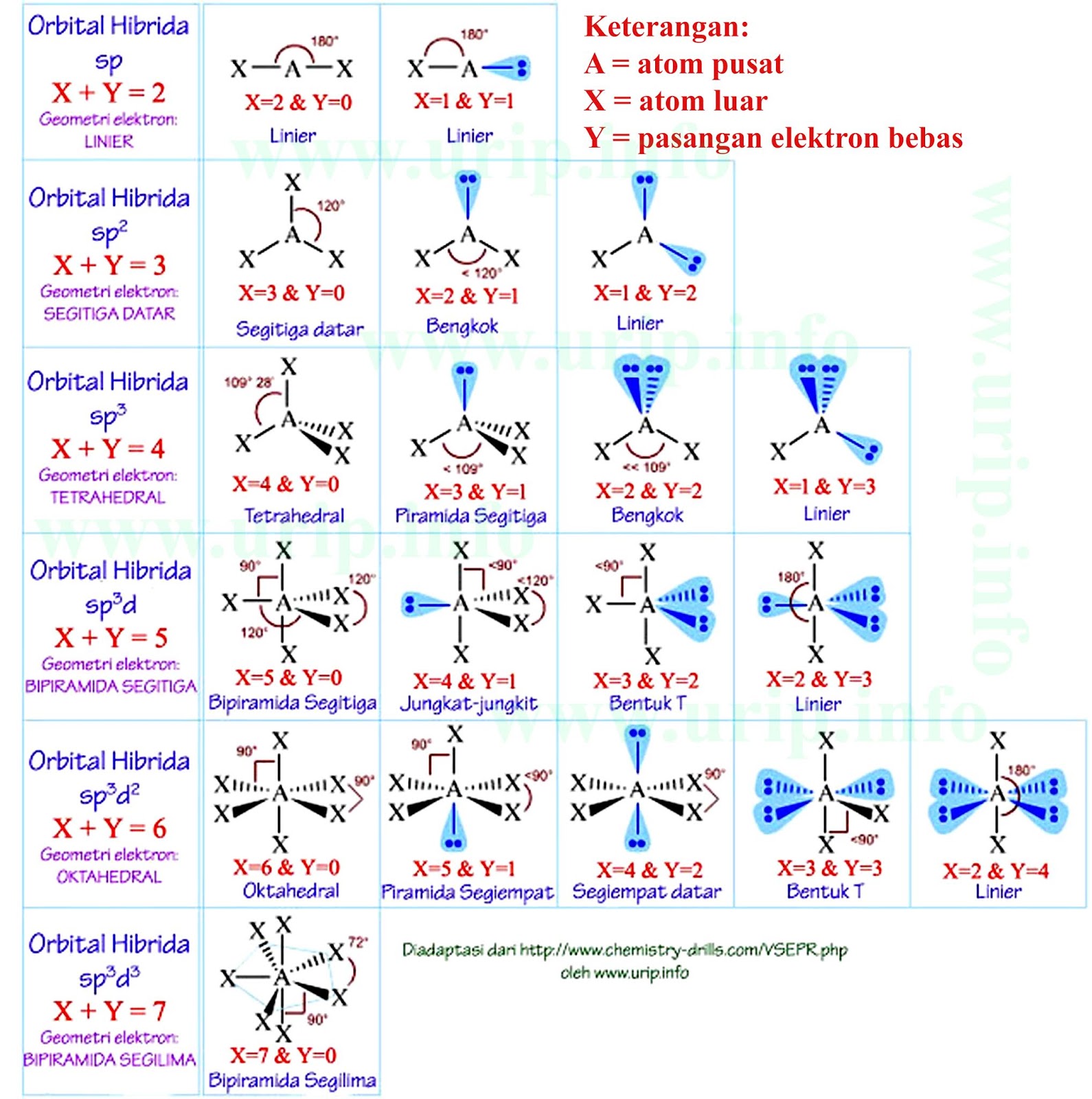
Senyawaan Belerang, Ikatan Kimia, Hibridisasi, Bentuk Molekulnya Markas Belajar
14-5 This video explains the bonding structure in PCl5 and SF6 by invoking sp3d and sp3d2 hybridization schemes

Ikatan Kimia Kelas 10 • Part 13 Tipe Molekul, Bentuk Molekul, Hibridisasi, dan Kepolaran IF3
6 Macam Hibridisasi dan Contohnya. Oleh Ilmu Kimia Diposting pada 11 Desember 2021. Hibridisasi terjadi ketika orbital dalam teori atom bercampur membentuk orbital atom baru. Orbital baru dapat menampung jumlah total elektron yang sama dengan yang lama. Sifat-sifat dan energi orbital hibridisasi yang baru adalah 'rata-rata' dari orbital.
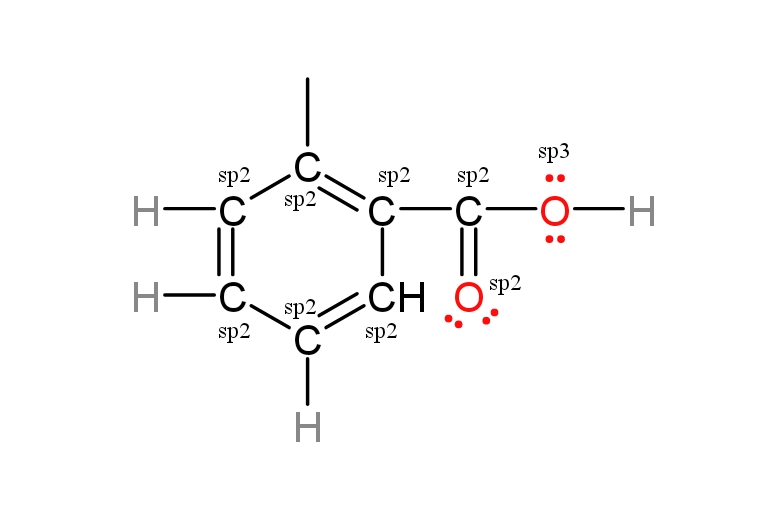
Tentukan hibridisasi dari struktur berikut ini
Orbital hybridisation. In chemistry, orbital hybridisation (or hybridization) is the concept of mixing atomic orbitals to form new hybrid orbitals (with different energies, shapes, etc., than the component atomic orbitals) suitable for the pairing of electrons to form chemical bonds in valence bond theory. For example, in a carbon atom which.

Hibridisasi YouTube
SF6 is an inorganic colorless greenhouse non-flammable gas with an octahedral geometry in which one sulfur atom is attached with six fluorine atoms. It has an orthorhombic crystalline structure and hypervalent in nature. In SF6, the S-F single bond length is 156.4 pm. ad. Let's focus on the structure, hybridization, formal charge and some.

Hybridization sp3d sp3d2 sp3d3 Formation of PF5, SF6 and IF7 Chemical Bonding
Hibridisasi Kimia Kelas 10 - Pengertian, Tipe, Cara Menentukan, dan Contoh Soal. Hibridisasi adalah proses bergabungnya orbital atom pusat dengan orbital atom lainnya sehingga terbentuk orbital hibrida. Sedangkan bentuk molekul merupakan susunan atom-atom di dalam molekul dalam bentuk tiga dimensi. Artikel ini akan membahas bentuk molekul dan.
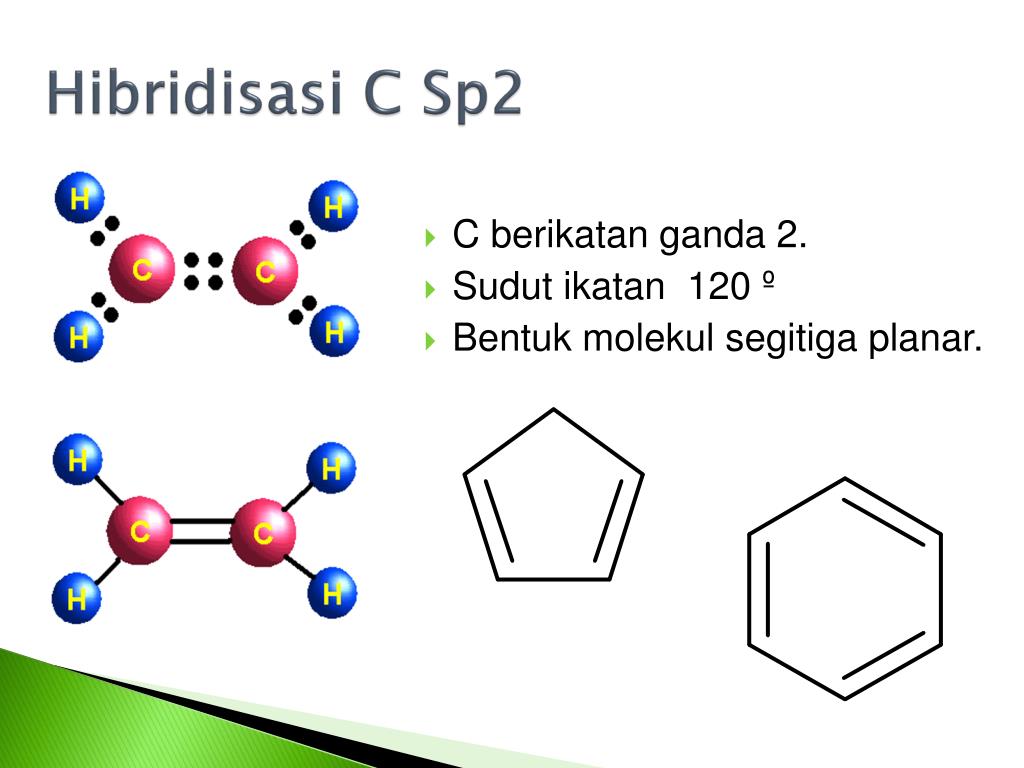
Perbandingan Jumlah Atom Karbon Dengan Hibridisasi Sp Dan Sp3 Adalah Lengkap
Here you will find curriculum-based, online educational resources for Chemistry for all grades. Subscribe and get access to thousands of top quality interact.