
LENGKAP ‼️ Cara Mudah Menentukan Pasangan Asam Basa Konjugasi TeoriAsamBasa AsamBasaKonjugasi
Menurut teori Brønsted-Lowry, HCN adalah asam Brønsted-Lowry karena mendonorkan proton (H+) sehingga menjadi ion CN− sedangkan H2O adalah basa Brønsted-Lowry karena menerima proton sehingga membentuk ion H3O+. Menurut teori Lewis, H2O adalah basa Lewis karena mendonorkan pasangan elektron kepada ion H+ yang berasal dari molekul HCN.

Draw The Lewis Structure For H3o+. What Is The Hybridization Of The O Atom Drawing Easy
Step 4: Substitute Coefficients and Verify Result. Count the number of atoms of each element on each side of the equation and verify that all elements and electrons (if there are charges/ions) are balanced. 3 CH3COOH + 6 CH3OH = 4 CH3COOHCH3 + 4 H2O. Reactants. Products.

Teori Asam Basa
Teori Brønsted-Lowry adalah teori reaksi asam-basa yang diajukan secara terpisah oleh Johannes Nicolaus Brønsted dan Thomas Martin Lowry pada tahun 1923. Konsep dasar teori ini adalah bahwa ketika suatu asam dan basa bereaksi satu sama lain, asam akan membentuk basa konjugatnya, dan basa membentuk asam konjugatnya melalui pertukaran proton (kation hidrogen, atau H +).

H3O+, l'ion hydronium définition et explications
The base we choose for exponentiation depends on the base of the logarithm. In this case that is 10 (An unlabeled logarithm is assumed to have a base of 10). So exponentiating an equation by 10 which includes a logarithm of base 10 undoes the logarithm. This allows us to solve for the [H3O+] and makes it equal to a power of 10. Hope that helps.

Pasangan spesi yang bersifat basa pada reaksi HCl + H2O ↔ H3O+ + Cl adalah YouTube
Asam Bronsted Lowry. Menurut Bronsted Lowry ,Asam adalah spesies yang menyumbangkan proton (H +) dan basa adalah spesies yang menerima proton. contoh asam: HNO3 (aq) + H2O <-> NO3- (aq) + H3O + (aq) Keq = jumlah yang sangat besar. Dalam contoh ini, HNO3 adalah asam dan H2O bertindak sebagai basa. NO3- disebut basa konjugasi dari asam HNO3, dan.
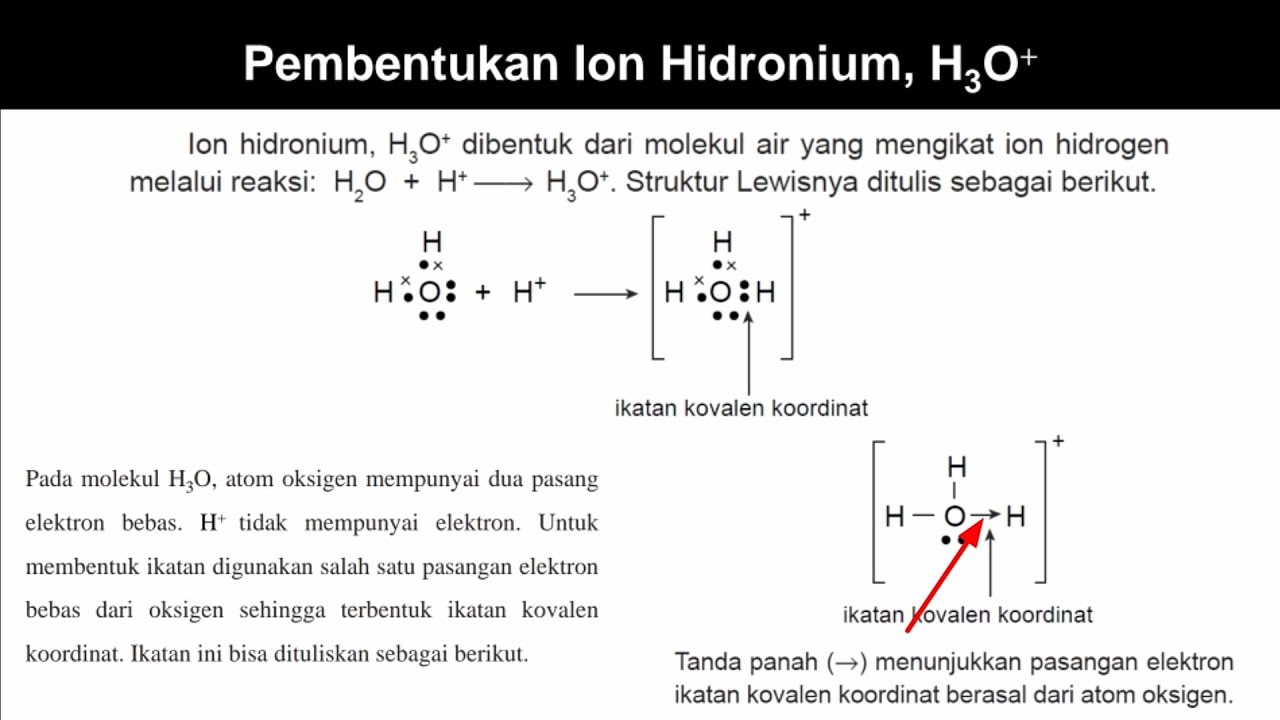
Bagaimana Ikatan Kovalen Koordinasi H3O+ (Hidronium) Terbentuk ? YouTube
Referensi. Dalam kimia, hidronium merupakan nama umum bagi kation berair H3O+, jenis ion oksonium yang dihasilkan melalui protonasi air. Ion ini merupakan ion positif yang hadir ketika suatu asam Arrhenius terlarut dalam air, karena molekul asam Arrhenius dalam larutan melepaskan sebuah proton (suatu ion hidrogen positif, H +) terhadap molekul.
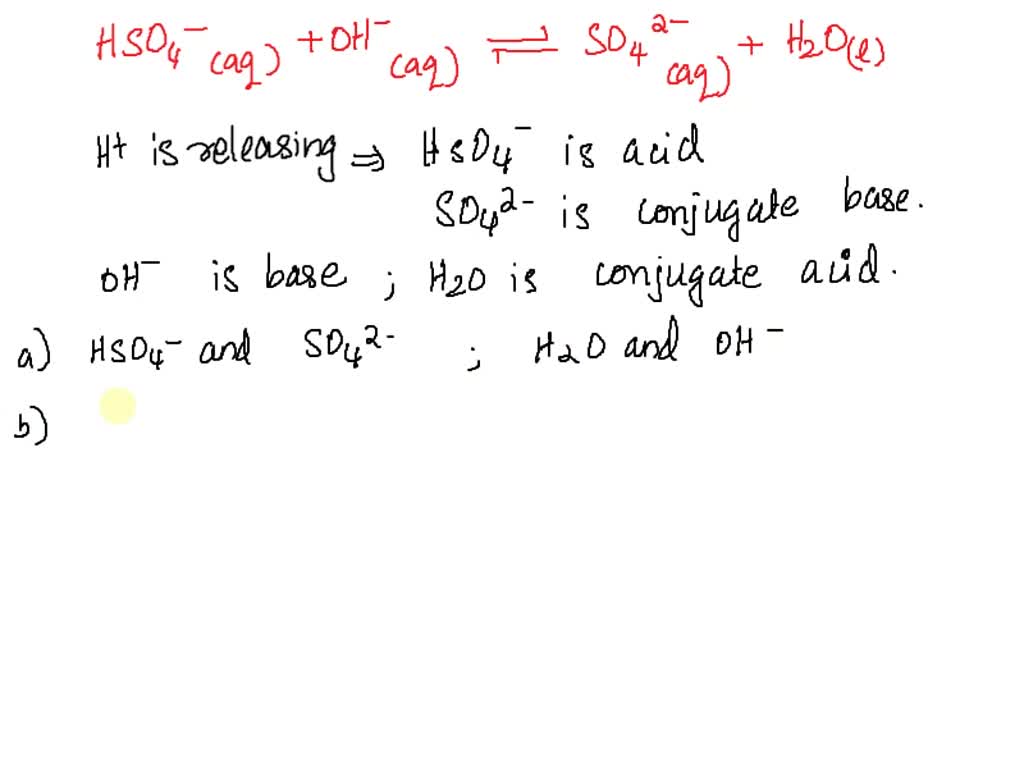
SOLVED pasangan asam basa konjugasi dari reaksi hso4(aq) + h2o(l) = h3o+(aq) + so4 2(aq) adalah
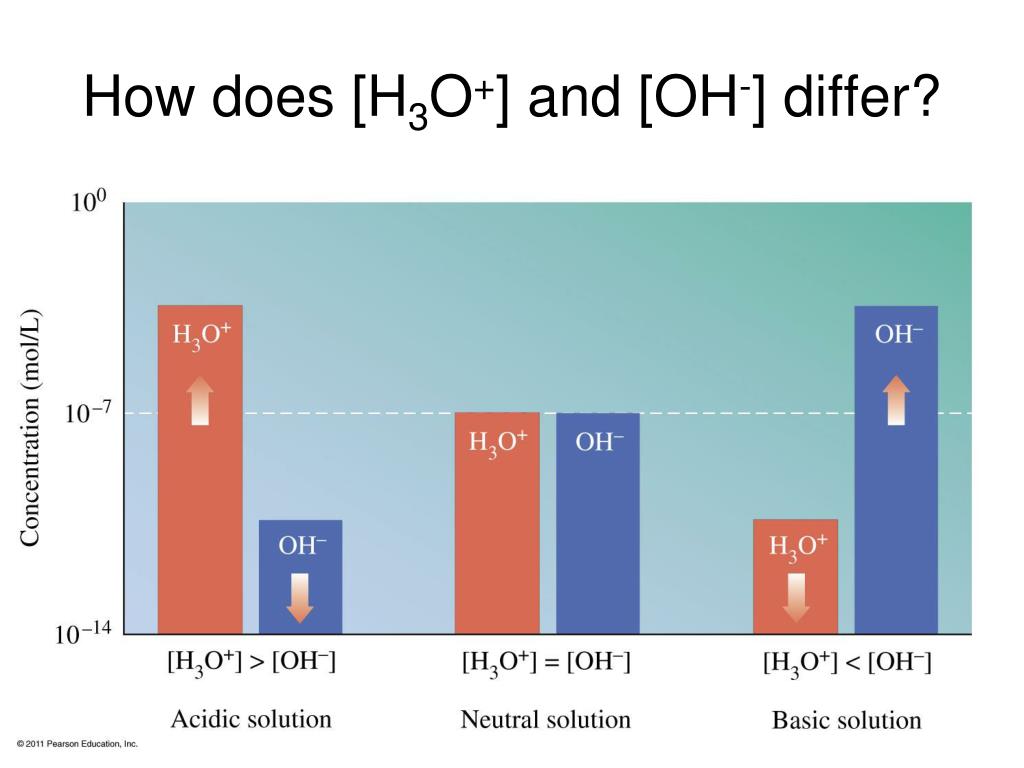
Dalam mempelajari reaksi asam basa dalam air, kuantitas yang penting adalah konsentrasi ion hidrogen. Tetapan kesetimbangan autoionisasi air yang dinyatakan sebagai H+ atau H3O + dan OH-dinyatakan sebagai : Karena fraksi air yang mengion sangat kecil, konsentrasi air [H2O] dapat dikatakan tidak berubah , karena itu : Kc [H2O] = Kw = [H +] [OH-]
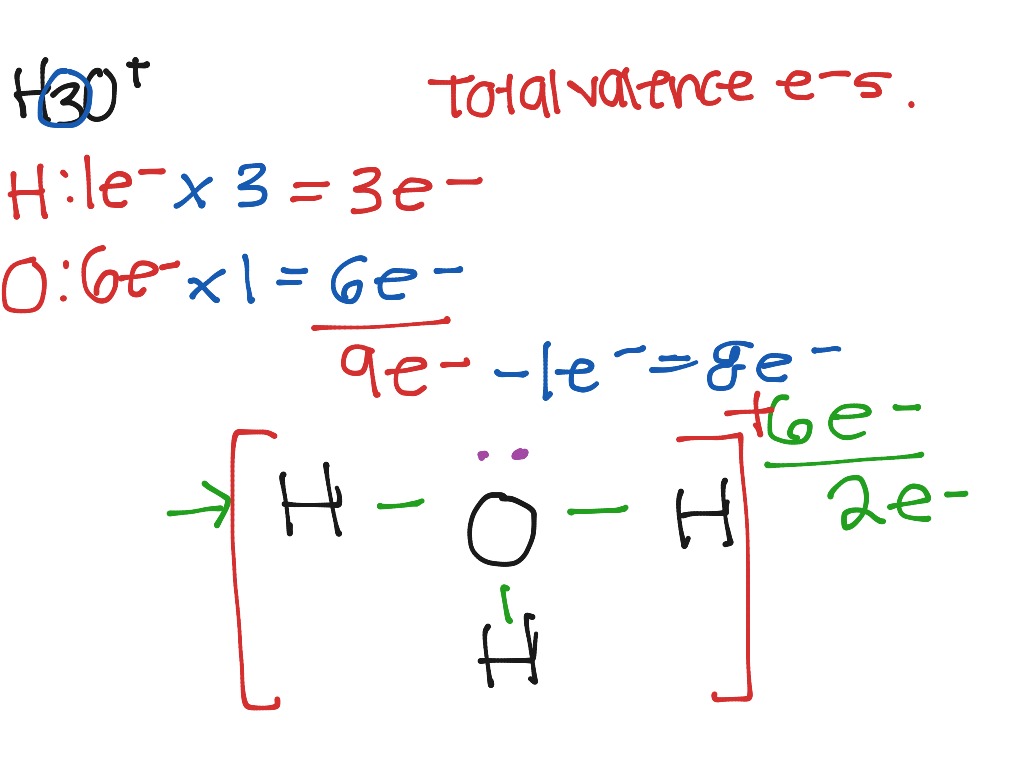
Lewis Dot Structure for H3O^+ Science ShowMe
Reaksi kimia untuk lebih jelasnya adalah seperti ini: H2O + H+ ⇌ H3O+ H20 atau air sendiri bisa berperan sebagai basa, atau juga berperan sebagai asam sehingga disebut bersifat amfoterik. Asam konjugasi maksudnya adalah ion yang diperoleh ketika basa menerima proton (H+). Sedangkan basa konjugasi adalah ion yang diperoleh setelah asam.

electron dot structure of H3O Brainly.in
This problem has been solved! You'll get a detailed solution from a subject matter expert that helps you learn core concepts. Question: HBr (aq) + H2O (l) → H3O+ (aq) + Br (aq) Label each of the following based on the above reaction: A. HBr: B.H20 Select) conjugate acid acid conjugate base base SCIO C. H30*: Rr. Select)

H3O+ Lewis Structure Lewis Dot Structure for H3O+ Hydronium ion Lewis Structure YouTube
Reaksi NH4 ke NH3. Asam Basa Konjugat - Konjugasi Asam Basa - Rumus, Konjugat, Contoh Soal dan Jawaban. Dapat dikatakan bahwa molekul air adalah asam konjugat ion hidroksida setelah hidroksida mendapat proton hidrogen yang diberikan oleh amonium.Di sisi lain, amonia adalah basa konjugat untuk amonium asam setelah amonium telah menyerahkan ion hidrogen untuk menghasilkan molekul air.
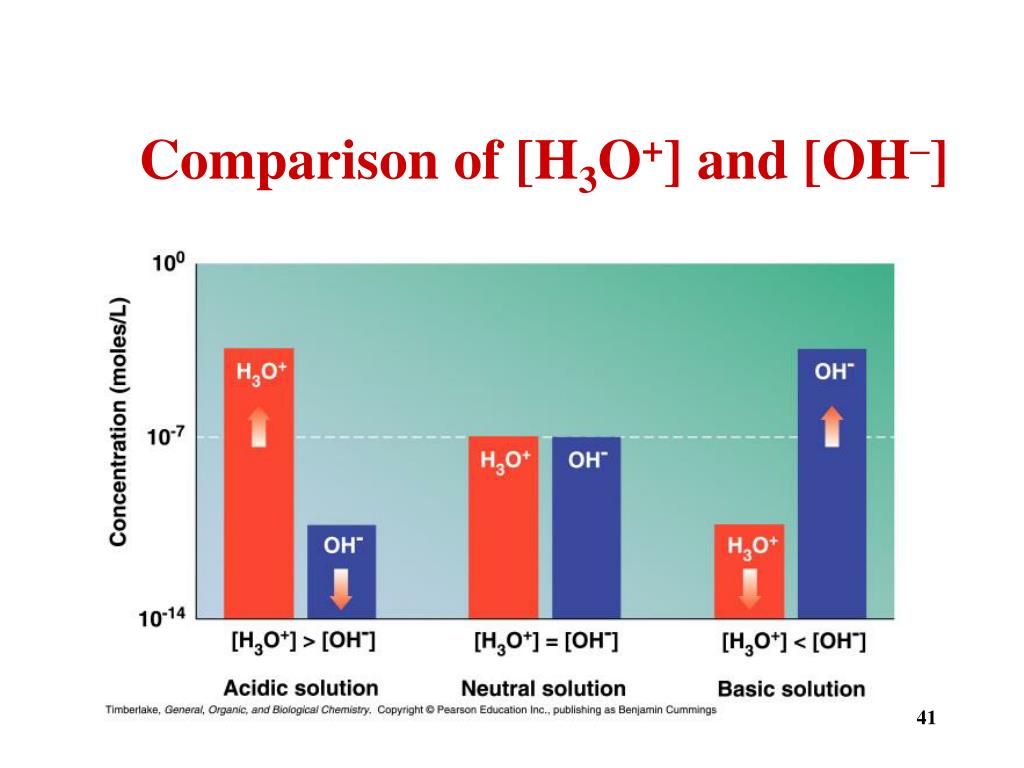
PPT Chapter 10 Acids and Bases PowerPoint Presentation, free download ID4509587
Dapat disimpulkan, bahwa teori Arrhenius ini menyatakan bahwa senyawa asam merupakan senyawa yang dapat melepaskan ion H+ atau ion hydronium H3O+ apabila dilarutkan dalam air. Sedangkan senyawa basa adalah senyawa yang melepaskan ion OH- jika dilarutkan dalam air.

H3O+ Lewis Structure (Hydronium Ion) YouTube
We are given the pKa for butyric acid and asked to calculate the Kb and the pKb for its conjugate base, the butyrate ion. Because the pKa value cited is for a temperature of 25°C, we can use Equation 16.6.16: pKa + pKb = pK w = 14.00. Substituting the pKa and solving for the pKb, 4.83 + pKb = 14.00.
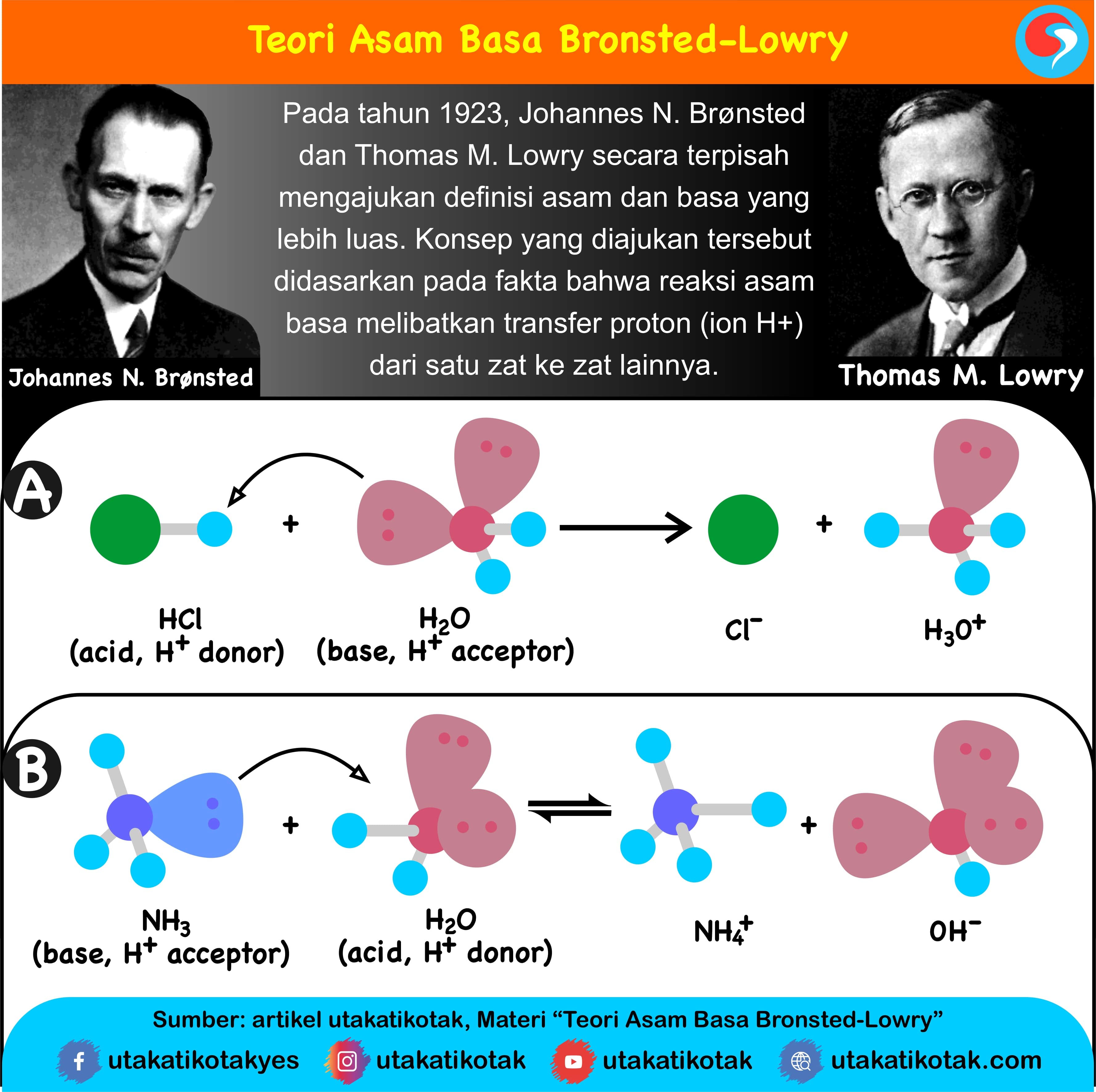
Teori Asam dan Basa Menurut BronstedLowry
a. HCl dan Cl- merupakan pasangan asam-basa konjugasi. HCl adalah asam konjugasi dari Cl-dan Cl- adalah basa konjugasi dari HCl. b. H2O dan H3O+ merupakan pasangan asam-basa konjugasi. H2O adalah basa konjugasi dari H3O+ dan H3O+ adalah asam konjugasi dari H2O. Berikut ini contoh pasangan asam-basa konjugasi pada beberapa reaksi. a.
PPT Acids, Bases, and Salts PowerPoint Presentation, free download ID3063628
Air H3O adalah air yang diperkaya dengan hidrogen molekuler tinggi, yang dapat memberikan manfaat kesehatan dan hidrasi optimal bagi tubuh manusia. Hidrogen telah dikenal luas memiliki sifat antioksidan yang kuat, dan dengan mengkonsumsi air H3O, Anda dapat mendapatkan akses ke manfaat ini dengan lebih efektif..

PPT Acids And Bases PowerPoint Presentation, free download ID1994745
Step 4: Substitute Coefficients and Verify Result. Count the number of atoms of each element on each side of the equation and verify that all elements and electrons (if there are charges/ions) are balanced. Since there is an equal number of each element in the reactants and products of B (OH)3 + 2H2O = B (OH)4 {-} + H3O {+}, the equation is.

A stepbystep explanation of how to draw the H3O+ Lewis Structure. YouTube
Reaction. The hydronium ion is an important factor when dealing with chemical reactions that occur in aqueous solutions. Its concentration relative to hydroxide is a direct measure of the pH of a solution. It can be formed when an acid is present in water or simply in pure water. It's chemical formula is H 3O +.