
PENYETARAAN REDOKS DENGAN CARA BILOKS UNTUK REAKSI ION (Part 1) YouTube
Reaksi oksidasi adalah proses kimia di mana suatu zat kehilangan elektron atau menambahkan oksigen. Ini adalah salah satu jenis reaksi redoks (oksidasi reduksi), yang melibatkan transfer elektron antara zat-zat kimia. Untuk memahami lebih lanjut, mari kita bahas unsur-unsur kunci yang terlibat dalam reaksi oksidasi.

Reaksi Redoks dan Elektrokimia Kimia Kelas 12 • Part 10 Reaksi Sel Elektrolisis YouTube
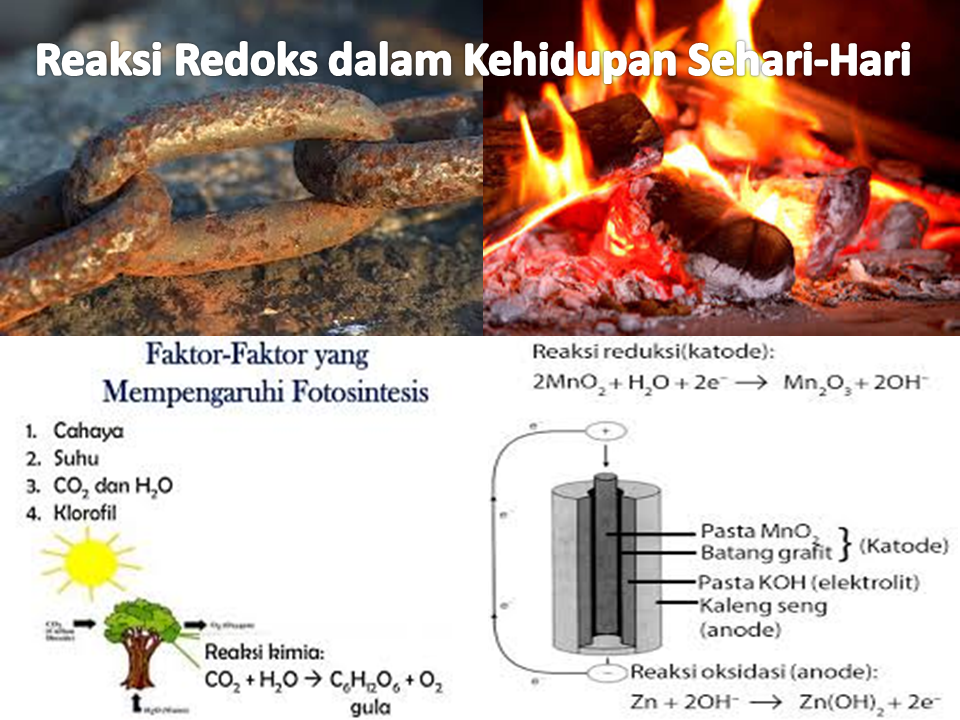
Penerapan Reaksi Redoks dalam Kehidupan Sehari-Hari. Di awal artikel, gue sempet mention beberapa contoh, lalu bagaimana nih penerapan reaksi redoks dalam kehidupan sehari sehari. Nah, supaya elo gampang mengingat, gue udah buat daftar contohnya berikut ini: Pembakaran. Tahu nggak sih, oksigen yang ada di atmosfer bumi itu mengalami penurunan.
.png)
Reaksi Redoks Pengertian, Ciri, Konsep, dan Menentukan BIlangan Oksidasi
Materi ini bertujuan untuk memahami bagaimana konsep dasar dari reaksi reduksi dan oksidasi (redoks). Dimulai dari pengertian redoks berdasarkan oksigen, ele.

Reaksi Redoks
REAKSI OKSIDASI DAN REDUKSI. Gambar. 8 Reaksi oksidasi pada pelapisan logam. Sumber: Ensiklopedi Sains & Kehidupan. Pada pelajaran kedelapan ini akan dipelajari tentang definisi reaksi. oksidasi dan reduksi serta lumpur aktif sebagai aplikasi dari konsep redoks. Reaksi Oksidasi dan Reduksi SMA Jilid 1 131. Bab 8 Reaksi Oksidasi dan Reduksi
1. A. Reaksi Redoks dan Tata Nama Senyawa Kimia Berbasis TIK
Konsep Reaksi Redoks berdasarkan Perpindahan Elektron. Berdasarkan perpindahan (transfer) elektron, reaksi reduksi adalah reaksi penangkapan elektron, sedangkan reaksi oksidasi adalah reaksi pelepasan elektron. Bisa kamu perhatikan gambar di atas ya, pada reaksi reduksi, elektronnya berada di ruas sebelah kiri reaksi, sebagai reaktan. Sementara.

BAHAN PELAJARAN MAPEL KIMIA BAB 2 REAKSI REDOKS DAN ELEKTROKIMIA
Permulaan Reaksi Redoks Kimia dalam Kehidupan Sehari-hari. Pada intinya, Reaksi Kimia bisa terjadi di manapun di sekitar kita, bukan hanya di laboratorium. Materi berinteraksi untuk membentuk produk baru melalui proses yang disebut reaksi kimia atau perubahan kimiawi. Setiap kali kita memasak atau sedang bersih-bersih, itu juga merupakan kimia.

KONSEP DASAR REAKSI REDOKS YouTube
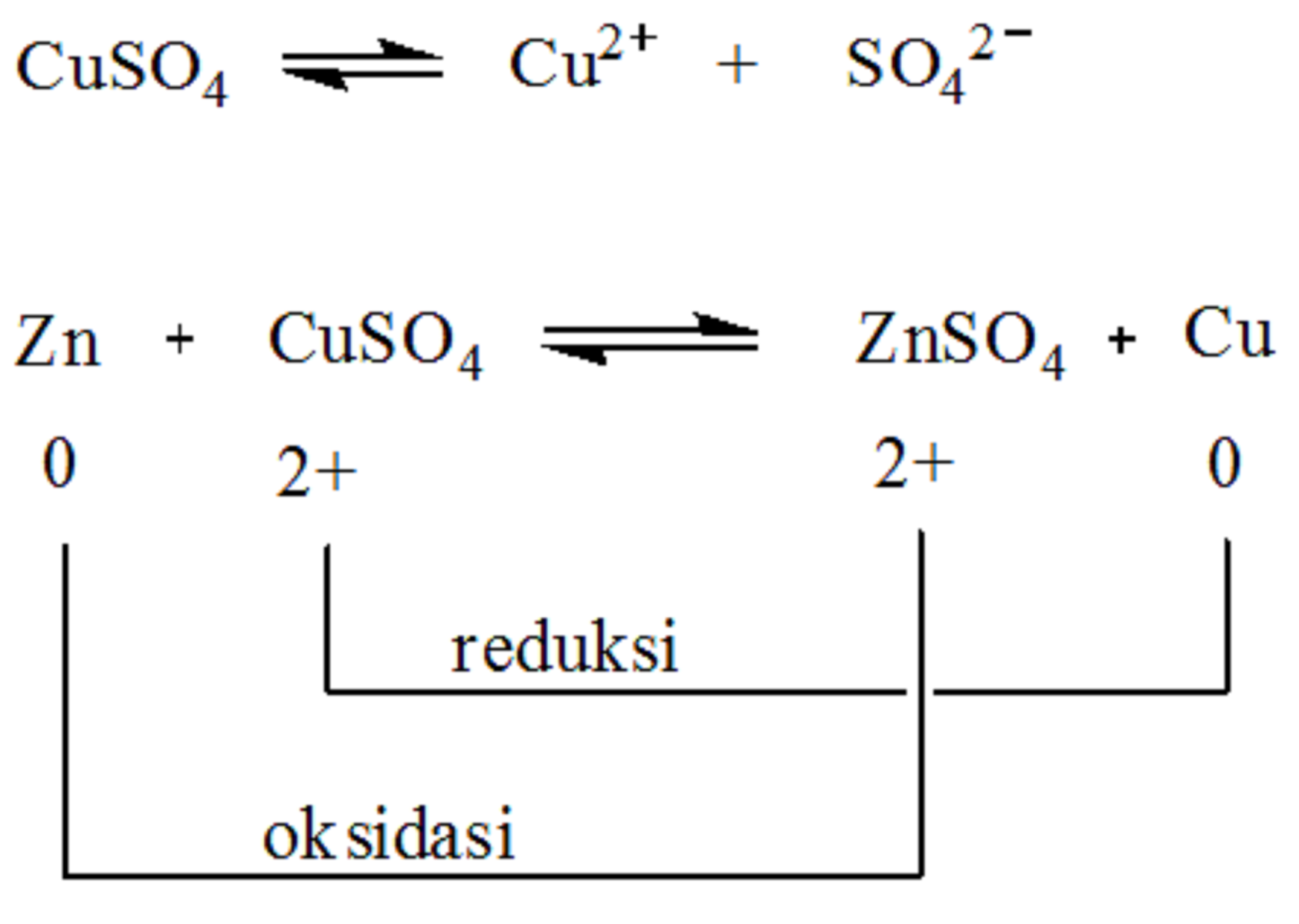
Pada reaksi reduksi di atas, terjadi penurunan biloks yaitu dari +2 ke 0. Secara umum, oksigen (O) mempunyai biloks -2 (kecuali pada senyawa H 2 O 2), sehingga jika melihat pada persamaan reaksi reduksi di atas nilainya adalah -1.Selanjutnya, senyawa CuO mempunyai nilai yang netral, maka biloks total Cu dan O adalah nol. Nah, karena biloks O = -2, maka agar total biloks CuO = 0, biloks Cu.

Reaksi redoks
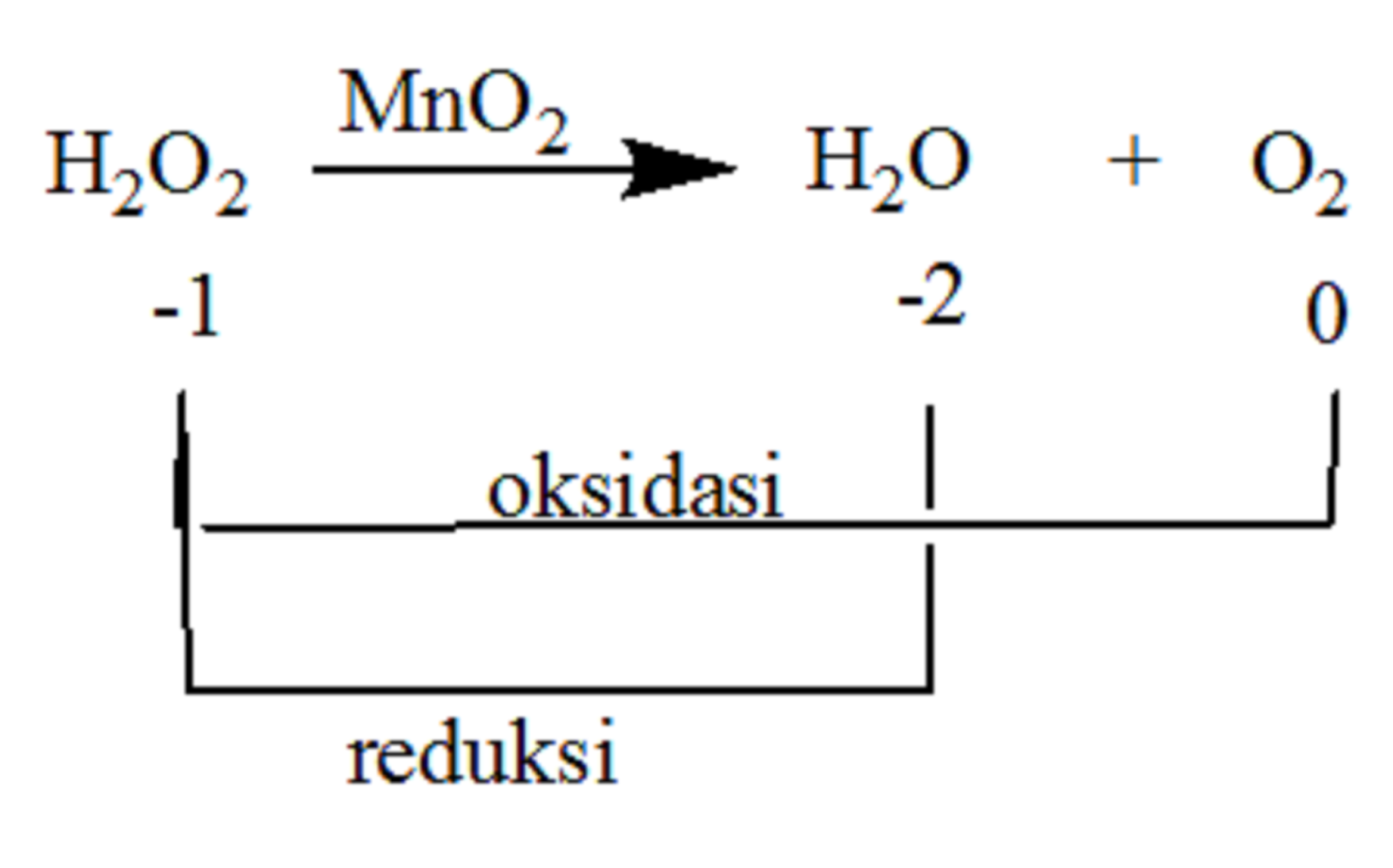
Berdasarkan penangkapan atau pelepasan oksigen. Oksidasi: reaksi yang melibatkan penangkapan atom oksigen. Contoh: C+ O2 → CO2. Atom C (karbon) mengalami oksidasi karena dalam reaksi atom karbon mengikat atom oksigen menjadi CO2. Reduksi: reaksi yang melibatkan pelepasan atom oksigen. Contoh: H2O2 → H2O + O2.
PERCOBAAN VIII REAKSI REDOKS (Kimia Dasar II) Blog Najih
Pengertian Reaksi Redoks. Reaksi redoks adalah jenis reaksi kimia di mana terjadi pertukaran elektron antara atom atau molekul yang terlibat. Istilah "redoks" sendiri berasal dari singkatan "reduksi-oksidasi.". Reaksi redoks sangat penting dalam kimia dan berbagai aspek kehidupan sehari-hari.
PPT Reaksi Redoks PowerPoint Presentation, free download ID7018645
Contoh Reaksi Redoks. Salah satu contoh reaksi redoks yaitu antara hidrogen dan fluorin: H2 + F2 a 2 HF. Anda bisa menuliskan semua reaksi tersebut sebagai 2 (dua) reaksi setengah: Reaksi oksidasi: H2 a 2H+ + 2e-Reaksi reduksi: F2 + 2e- a 2F-Penganalisaan tiap-tiap reaksi setengah akan menjadikan keseluruhan proses kimia tampak lebih jelas lagu.

Reaksi Redoks YouTube
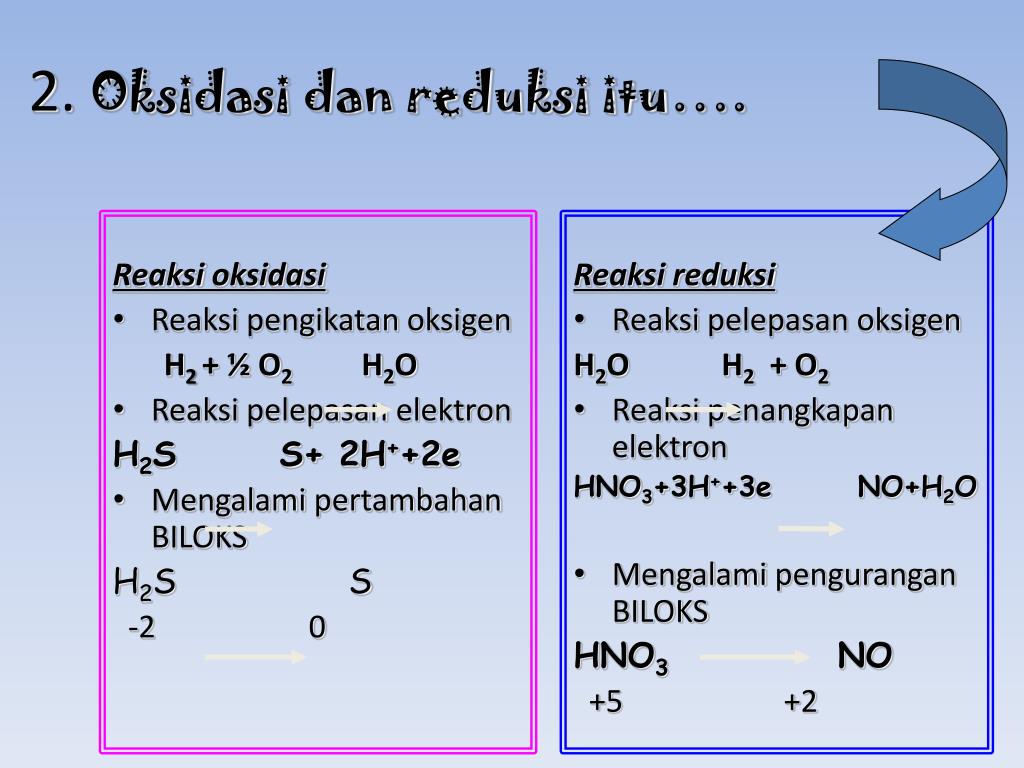
Pemahaman Akhir. Reaksi redoks merupakan reaksi yang terdiri dari reduksi (penerimaan elektron) dan oksidasi (penyisihan elektron). Konsep reaksi redoks dapat dilihat dari berbagai sudut pandang, seperti berdasarkan pengikatan dan pelepasan oksigen, pengikatan dan pelepasan elektron, atau penambahan dan penurunan bilangan oksidasi.

Mempelajari Konsep Reaksi Redoks (ReduksiOksidasi) Kimia Kelas 10
Reaksi redoks adalah reaksikimia yang menyebabkan adanya perubahan bilangan oksidasi pada suatu unsur, maupun molekul. Selain ditandai dengan perubahan bilangan oksidasi, Reaksi ini juga ditandai dengan penambahan atau pengurangan oksigen dalam suatu molekul. Reaksi redoks terjadi akibat adanya reaksi reduksi dan oksidasi. Reaksi Reduksi

Reaksi Redoks dan Elektrokimia Kimia Kelas 12 • Part 7 Sel Volta YouTube
REDOKS DAN ELEKTROKIMIA 3 Gambar 2. menunjukkan terjadinya reaksi oksidasi yaitu reaksi Fe (s) menjadi Fe 2+(aq) dan Fe 2+(aq) menjadi Fe 3+(aq). Reak - si tersebut diikuti dengan reaksi reduksi yaitu reaksi O 2 (g) + 4H+(aq) + 4e-→ 2H 2 O(l). Dengan demikian, dapat disimpulkan bahwa reaksi oksidasi dan reduksi akan berlangsung secara bersamaan.
PERCOBAAN VIII REAKSI REDOKS Kimia Dasar II Najih Web Id 30240 Hot Sex Picture
Reaksi redoks merupakan kependekan dari reaksi reduksi oksidasi. Bilangan oksidasi (biloks) suatu unsur adalah bilangan bulat yang digunakan untuk memudahkan perhitungan perpindahan elektron dari satu atom, molekul, atau ion ke atom, molekul atau ion. 12 Gambar 4.3.1 Hasil titrasi KMnO4 dengan asam oksalat Reaksi yang terjadi antara asam.

Reaksi Kimia Di Bawah Ini Yang Merupakan Reaksi Redoks Adalah Terbaru
Konsep Reaksi Redoks - Contoh, Cara Menentukan Biloks dan Tatanama - Materi dasar redoks dipelajari pada kelas 10 SMA semester 2 dimana akan dilanjutkan juga nantinya pada kelas 12 lebih mendalam tentang penyetaraan reaksi redoks. Reaksi redoks adalah reaksi yang melibatkan reaksi reduksi dan reaksi oksidasi.

Reaksi redoks
Konsep Reaksi Redoks Berdasarkan Keterlibatan Atom Oksigen Dalam konsep ini, proses Oksidasi berarti reaksi unsur yang mengikat oksigen. Adapun contohnya adalah di bawah ini. a. Contoh 1: proses berkaratnya logam dan besi akibat unsur besi mengikat oksigen baik dari udara maupun dari air. Reaksinya adalah: 4 Fe (s) + 3 O2(g) → 2 Fe2O3(s)