
SEL ELEKTROKIMIA (PART 1) SEL VOLTA DAN SEL ELEKTROLISIS KIMIA DASAR KIMIA SMA KELAS XII
LAPORAN PRAKTIKUM SEL VOLTA. Dalam kehidupan sehari-hari sangat sering terjadi reaksi kimia di sekeliling kita, namun hal itu jarang diketahui oleh setiap orang. Mulai dari pemakaian batrai sampai kepada hal yang sangat sering kita jumpai yaitu pemurnian logam dan emas. Menggunakan batrai ataupun memurnikan logam tak lepas dari reaksi kimia.

Presentasi Kimia Dasar II Baterai Sel Volta YouTube
Sel Volta: Pengertian, Contoh dan Prinsip Kerjanya. Kholida Qothrunnada - detikEdu. Kamis, 21 Okt 2021 14:48 WIB. Prinsip kerja sel volta (Foto: shutterstock) Jakarta -. Sel volta disebut juga dengan sel galvani. Penamaan keduanya tersebut, diambil dari nama penemunya yaitu seorang ilmuan bernama Alessandro Guiseppe Volta. dan Luigi Galvani.

Soal Dan Pembahasan Sel Volta Ruang Ilmu
Sel volta adalah materi yang akan kita pelajari, bersama dengan pengertian sel volta, rangkaian sel volta, dan masih banyak lagi. Yuk, simak pembahasannya!. elo bisa melihat kalau prinsip dasar sel volta ini dapat dilihat secara langsung pada baterai yang kita gunakan sehari-hari, yaitu pada keberadaan anoda dan katoda.

Sel Volta Simple konsep & Contoh Soal YouTube
Dedicated to the god of healing Wong Tai Sin, this iconic temple is a feast for the senses, with bright red pillars, bronze zodiac statues, jade-coloured roofs with intricate latticework and dragon adornments, and the scent of incense thick in the air. "I have been coming here to wish for good luck for at least a decade," says 65-year-old.
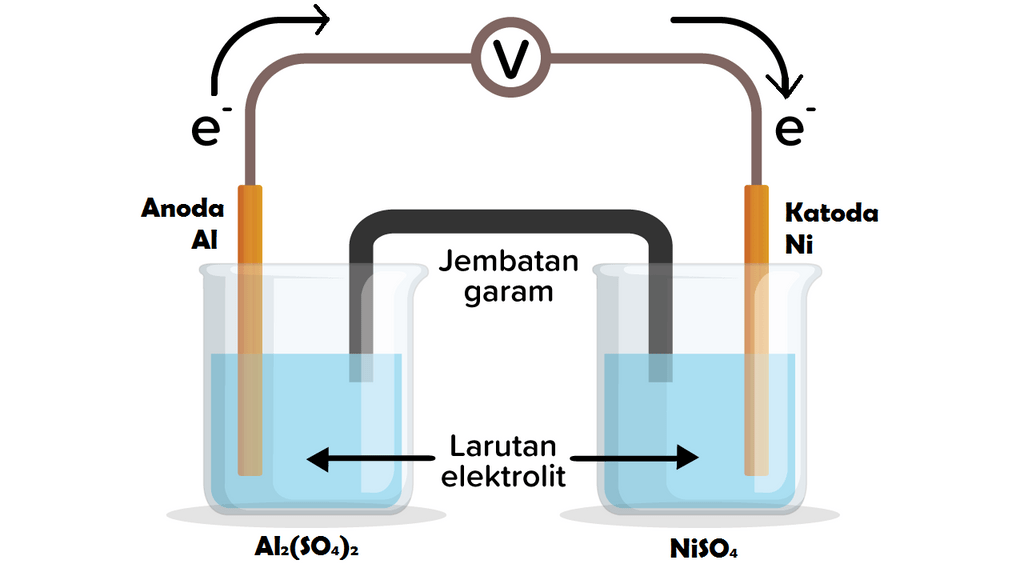
Sebuah sel volta terdiri dari elektrode Ni dalam l...
Sel volta terdiri atas dua elektroda yang terhubung dan dapat menghasilkan listrik, jembatan garam, dan juga larutan elektrolit tempat elektroda ditempatkan. Baca juga: Biografi Tokoh Dunia: Alessandro Volta, Fisikawan Italia Penemu Baterai. Prinsip Kerja Sel Volta. Jembatan garam adalah dinding berpori yang memisahkan katoda dan anoda sel volta.

Perhatikan sel Volta berikut! Notasi sel yang tepat untuk...
Penjelasan Tentang Sel Galvani (Sel Volta) dan Kegunaannya Sel galvani adalah sel di mana reaksi kimia antara dua konduktor berbeda yang terhubung melalui larutan elektrolit dan jembatan garam sehingga menghasilkan energi listrik. Sel galvani juga dapat didukung oleh reaksi reduksi oksidasi spontan. Pada dasarnya, energi listrik yang di hasilkan sel galvani dihasilkan oleh transfer elektron

(PDF) SEL VOLTA DAN ELEKTROLISIS chelsea simatupang Academia.edu
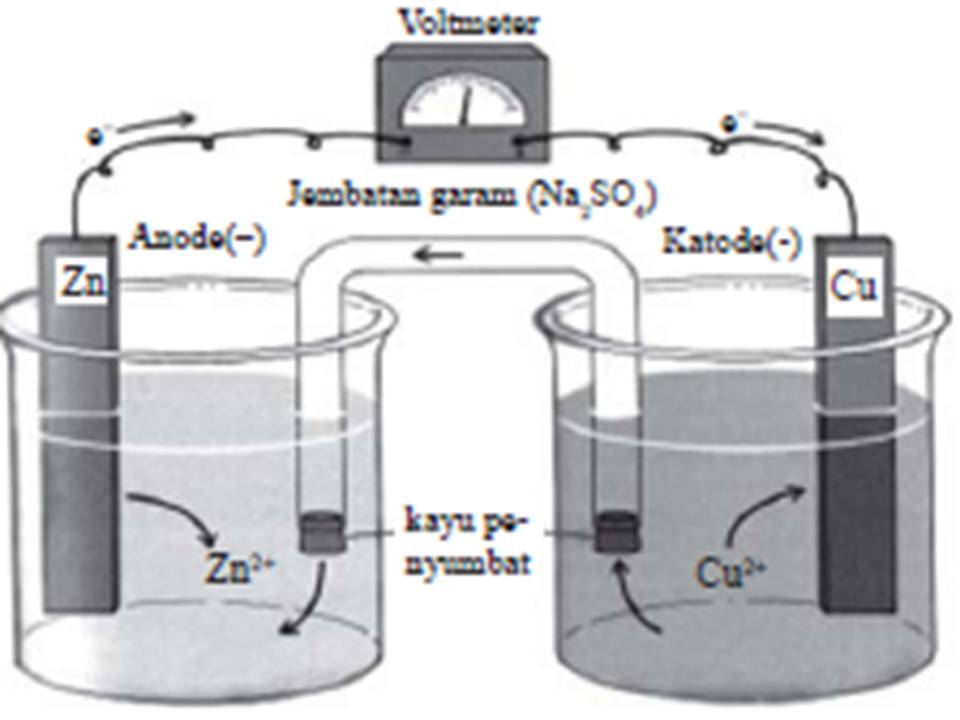
Contoh sel volta yaitu sel yang menggunakan logam Zn dan Cu. Ketika rangkaian ditutup kedua logam tersebut dapat bereaksi secara spontan dan mengalirkan listrik. Logam Zn teroksidasi menjadi Zn 2+ sedangkan pada sel Cu terjadi reduksi Cu 2+ menjadi Cu. Jadi selama pemakaian sel volta massa logam Zn akan berkurang sedangkan logam Cu menjadi.

SEL VOLTA (KIMIA SMA KELAS 12) YouTube
Scribd adalah situs bacaan dan penerbitan sosial terbesar di dunia.

peta konsep sel volta BAKRIE CHEMISTRY
Sel Volta: Pengertian, Prinsip, dan Kegunaannya. Menyajikan informasi terkini, terbaru dan terupdate mulai dari politik, bisnis, selebriti, lifestyle dan masih banyak lagi. Baterai adalah Jenis Sel Volta. Foto: Pixabay. Sebuah reaksi kimia dapat menghasilkan energi listrik yang berguna bagi manusia.

Sel volta kelas 12 YouTube
Rangkaian Sel Volta: Kedua larutan dihubungkan oleh jembatan garam yang berisi KCl. Elektron mengalir dari elektroda Zn (sebagai anoda) ke elektroda Cu (sebagai katoda) melalui kawat eksternal. Setengah sel yang satu terdiri dari logam seng (zinc) yang dicelupkan ke dalam larutan dan setengah sel yang lainnya terdiri atas logam tembaga (copper.

Sel Volta KIMIA KELAS 12 YouTube
LANDASAN TEORI SEL VOLTA. A. ELEKTROKIMIA. Elektrokimia adalah ilmu yang mempelajari aspek elektronik dari reaksi kimia. Elemen yang digunakan dalam reaksi elektrokimia dikarakterisasikan dengan banyaknya elektron yang dimiliki. (notechaca.blogspot.com) Reaksi elektrokimia dapat dibagi dalam dua kelas: yang menghasilkan arus listrik (proses.

Arti Mw Dalam Gelas Kimia √ Pengertian Sel Volta, Teori, Komponen, Cara Kerja, dan Contohnya
Dasar teori sel volta selanjutnya adalah hukum Faraday yang dikemukakan oleh Michael Faraday pada tahun 1833. Baca juga: Hukum Faraday I dan II tentang Elektrolisis. Dilansir dari Encyclopedia Britannica, menurut hukum Faraday zat yang dihasilkan pada elektroda berbanding lurus dengan jumlah muatan yang mengalir.
PRAKTIKUM SEL VOLTA DAN ELEKTROLISIS IGNAPBLOGZ
Terjun ke dalam dunia sains pada abad ke-19, teori sel volta menjadi perbincangan yang menggebu di kalangan ilmuwan. Ditemukan oleh Alessandro Volta pada tahun 1800, teori ini membahas tentang konsep dasar pembangkitan listrik menggunakan reaksi kimia di antara dua logam berbeda dalam larutan. Simak ulasan mendalam tentang teori sel volta, mekanisme kerjanya, dan aplikasi praktisnya dalam.

NOTASI SEL DAN POTENSIAL SEL (SEL VOLTA KIMIA SMA KELAS 12) YouTube
Reaksi redoks spontan dapat digunakan sebagai sumber listrik, alat yang dapat mengubah reaksi kimia menjadi energi listrik disebut sel Volta atau sel Galvani. Sel volta terdiri dari elektroda (katoda dan anoda) dan elektrolit. Elektron mengalir dari anoda menuju katoda. Potensial sel volta dapat ditentukan melalui eksperimen atau dihitung berdasarkan data potensial elektroda standar.

Detail Gambar Rangkaian Sel Volta Dan Penjelasannya Koleksi Nomer 6
Download Modul "Sel Volta" untuk Materi yang Lebih Lengkap dan Contoh Soal yang Lebih Banyak Di Sini. Pada gambar di atas, terlihat rangkaian sel volta dengan dua kompartemen. Masing-masing kompartemen merupakan setengah sel. Pada kompartemen kiri, dalam larutan ZnSO 4 terjadi setengah reaksi oksidasi Zn menjadi ion Zn 2+, sedangkan pada kompartemen kanan, dalam larutan CuSO 4 terjadi.

Materi Sel Volta Kimia Kelas 12 Bit CDN
Menguji apakah jeruk nipis merupakan sel volta yang mempunyai daya hantar listrik. II. Dasar Teori Sel volta atau sel Galvani adalah bagian dari sel elektrokimia yang didalamnya terjadi reaksi redoks spontan yang menghasilkan listrik. Dalam sel