
Materi Penurunan Titik Beku Beserta Contoh Soal Dan Pembahasan Reverasite
Untuk larutan elektrolit menggunakan rumus: Keterangan: ∆T f = Penurunan titik beku. K f = Tetapan penurunan titik beku molal. n = Jumlah mol zat terlarut. p = Massa pelarut. i = Faktor Van't Hoff. Dalam bidang thermodinamika konstanta titik beku ( K f ) lebih dikenal dengan istilah "Konstanta Kriokopik".

Contoh Soal Titik Beku Larutan (Sifat Koligatif Larutan Elektrolit) YouTube
Contoh soal sifat koligatif larutan kenaikan titik didih dan penurunan titik beku adalah sebagai berikut: Contoh Soal Sifat Koligatif Larutan Kenaikan Titik Didih. Soal No. 1. Natrium hidroksida 1,6 gram dilarutkan dalam 500 gram air. Hitung titik didih larutan tersebut! (K b air = 0,52 0 C/m, Ar Na = 23, Ar O = 16, Ar H = 1) Pembahasan: Diketahui:

Kumpulan Contoh Soal Penurunan Titik Beku Kimia Kelas 12 CoLearn halaman 17
Jawaban: Contoh penerapan sifat koligatif yang berkaitan dengan penurunan titik beku meliputi: Penggunaan garam dapur untuk mencairkan salju. Penambahan etilena glikol pada radiator mobil. Pembuatan es krim menggunakan campuran garam dapur. 3. Sebanyak 18 gr glukosa (Mr = 180) dilarutkan dalam 500 gram air.
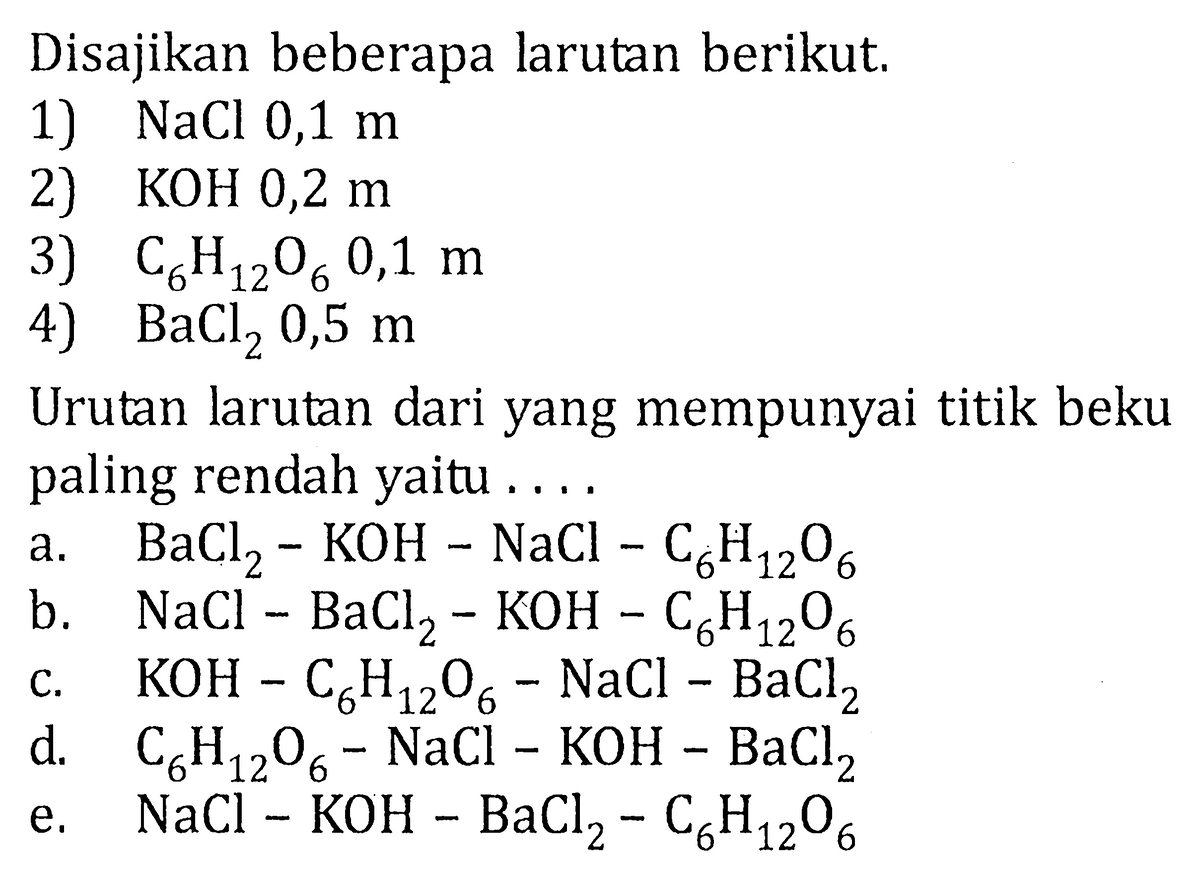
Kumpulan Contoh Soal Penurunan Titik Beku Kimia Kelas 12 CoLearn halaman 27
berikut KUMPULAN SOAL DAN PEMBAHASAN PENURUNAN TITIK BEKU (∆Tf) part 1. SOAL : Sebanyak 8 gram zat A dilarutkan kedalam 200 ml air. Jika diketahui tetapan penurunan titik beku air (Kf) air 1,86 /molal dan massa molar zat tersebut adalah 40 gr/mol , hitung titik beku larutan ! Dalam 200 gram air terlarut 10 gram urea CO (NH 2) 2.

Contoh Soal Kimia Tentang Penurunan Titik Beku Guru Luring
Sonora.ID- Berikut ini adalah ulasan tentang 10 Contoh Soal Titik Didih dan Titik Beku Lengkap Beserta Jawabannya. Titik didih dan titik beku adalah dua sifat fisik penting dari suatu zat yang berkaitan dengan fase zat tersebut, baik itu padat, cair, atau gas. Titik didih adalah suhu di mana zat berubah dari fase cair menjadi fase gas.

Contoh Soal Kimia Penurunan Titik Beku Soal Kelasmu
Ilustrasi gambar (pexels.com) Hukum Roult merupakan dasar dari sifat koligatif larutan. Keempat sifat itu ialah: 1.Penurunan tekanan uap. 2.Peningkatan titik didih. 3.Penurunan titik beku. 4.Gejala tekanan osmotik. Jadi gitu guys pembahasan mengenai Sifat Koligatif Larutan.

15 Contoh Soal Penurunan Titik Beku Rumus Jawaban Pembahasan Reverasite
Secara umum, penurunan titik beku dapat dijelaskan oleh Hukum Raoult dan hukum konsentrasi molal. Hukum Raoult menyatakan bahwa tekanan uap suatu pelarut ideal adalah produk dari fraksi mol pelarut dan tekanan uap pelarut murni. Dengan adanya zat terlarut (non-volatil), tekanan uap pelarut menurun, dan sebagai hasilnya, titik beku pelarut.

Cara Menghitung Tetapan Penurunan Titik Beku Larutan (Kf) (UN Kimia 2018 No. 24) YouTube
Contoh Soal Penurunan Titik Beku Soal 1. Sebanyak 8 gram zat A dilarutkan kedalam 200 ml air. Jika diketahui tetapan penurunan titik beku air (Kf) air 1,86 /molal dan massa molar zat tersebut.

Contoh Soal Penurunan Titik Beku Dan Pembahasan Reverasite Reverasite
Contoh soal dan pembahasan. Contoh soal 1. Sebanyak 2,4 gram urea (Mr = 60) dilarutkan dalam 50 gram air. Jika Kf air = 1,86 °C/m, tentukanlah titik beku larutan. Pembahasan. Pada soal ini urea sebagai zat terlarut dan air sebagai pelarut. Besaran yang diketahui sebagai berikut: gr = 2,4 gram. Mr = 60.

Materi Penurunan Titik Beku Beserta Contoh Soal Dan Pembahasan Reverasite
Contoh Soal Penurunan Titik Beku Larutan Elektrolit. Berikut ini adalah contoh soal penurunan titik beku larutan elektrolit: Sebuah larutan CaCl2 memiliki konsentrasi molal sebesar 0,5 mol/kg. Faktor vant Hoff (i) untuk CaCl2 adalah 3. Hitunglah penurunan titik beku larutan tersebut jika konstanta kriometri Kf = 1,86 °C/m.

Contoh Soal Kimia Sifat Koligatif Larutan Penurunan Titik Beku YouTube
Penurunan titik beku adalah selisih antara titik beku pelarut dengan titik beku larutan. Penurunan titik beku ini termasuk salah satu sifat koligatif larutan. Dalam perhitungan kimia, penurunan titik beku disimbolkan dengan ΔT f (f berasal dari kata freeze) atau ΔT b . Peristiwa penurunan titik beku ini sering diterapkan pada negara-negara.
Contoh Soal Penurunan Titik Beku Larutan Elektrolit Contoh Soal Terbaru Rezfoods Resep
Video Contoh Soal Penurunan Titik Beku Kelas 12. 01:10. Penurunan titik beku molal ialah penurunan titik beku yan. Penurunan Titik Beku; Sifat Koligatif Larutan;. Cari soal Matematika, Fisika, Kimia dan tonton video pembahasan biar ngerti materinya. Matematika, Fisika dan Kimia;

Kumpulan Contoh Soal Penurunan Titik Beku Kimia Kelas 12 CoLearn halaman 31
1. Titik Beku (Tf) Jadi begini , proses pembekuan itu terjadi ketika suatu zat telah mencapai titik beku. Titik beku ( Tf) akan tercapai apabila temperatur saat tekanan uap zat padat, sama dengan tekanan uap zat cair. Jika kalian mengetahui bahwa titik beku air sebesar 0ºC, itu artinya tekanan uap air dalam bentuk cair pada temperatur 0ºC.

Kumpulan Contoh Soal Penurunan Titik Beku Kimia Kelas 12 CoLearn halaman 2
Nah, disini saya akan membahas mengenai penuruan titik beku dalam kehidupan sehari-hari. Yuk simak artikel ini sampai selesai! Penurunan titik beku adalah penurunan titik beku pelarut akibat penambahan zat terlarut yang tidak mudah menguap. Penurunan titik beku dalam kehidupan sehari-hari yaitu : 1. Antibeku Dalam Tubuh Hewan

Penurunan Titik Beku Larutan Elektrolit Reverasite
Dikutip dari buku Belajar Kimia Secara Menarik untuk SMA/MA Kelas XII yang ditulis oleh Das Salirawati, dkk (2007: 16), berikut adalah 4 contoh soal penurunan titik beku dan pembahasannya: 1. Tentukan titik beku larutan 0,025 mol suatu senyawa dalam 250 gram air, jika Kf air = 1,86º C/m! Jawaban: m = n/p = 0,025 mol/0,25 kg = 0,1 m. Delta Tf = m .

Penurunan Titik Beku Larutan Definisi Dan Penyebabnya Reverasite
∆T f = penurunan titik beku (o C) T f = titik beku larutan (o C) T f = titik beku pelarut murni (o C) m = molalitas K f = tetapan penurunan titik beku molal (o C.kg/mol) i = faktor Van't Hoff. Contoh Soal. 1. Sebanyak 0,300 g urea, CO(NH 2) 2, dilarutkan ke dalam 10,0 g air. Dengan menganggap sifat larutan ideal, hitunglah titik beku larutan!