
32++ Contoh Soal Senyawa Asam Basa Contoh Soal Terbaru
Teori Asam Basa Lewis: Definisi - Reaksi - Keunggulan. Di tahun 1923, G.N. Lewis yang merupakan seorang ahli kimia berasal dari Amerika Serikat memperkenalkan teori asam dan basa yang tidak melibatkan transfer proton namun melibatkan penyerahan dan juga penerimaan pasangan elektron bebas dimana ada perbedaan sifat asam dan basa.

XI.6.q. Teori Asam Basa Lewis (Teori) YouTube
Asam konjugasi adalah basa yang memperoleh ion hidrogen, sedangkan basa konjugasi adalah yang tersisa setelah asam memberikan proton dalam sebuah reaksi kimia. Kedua hal tersebut disebut pasangan asam basa konjugasi. Teori Asam Basa Lewis. Asam basa Lewis menjelaskan terkait struktur dan ikatannya.
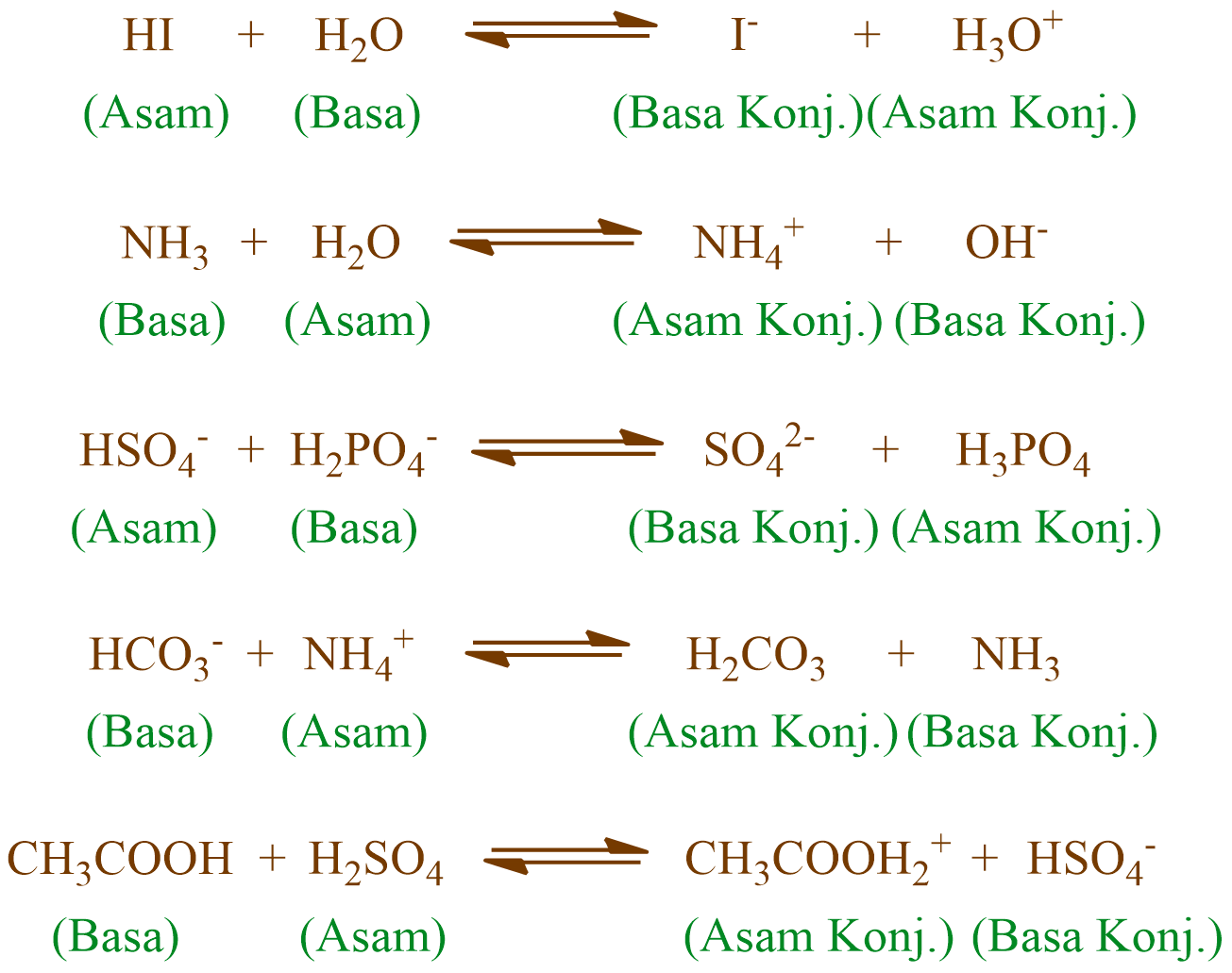
Chocogreentea Keterbatasan Teori AsamBasa Bronsted Lowry
Contoh reaksi asam basa Lewis adalah reaksi antara Na 2 O dan SO 3. Na 2 O + SO 3 → Na 2 SO 4. Baca Juga: Pengertian Larutan dan Klasifikasinya - Kimia Kelas 11. Contoh Soal dan Pembahasan Reaksi Asam Basa. Untuk menguji sejauh mana pemahaman mengenai materi reaksi asam basa, gue ada beberapa contoh soal dan pembahasan yang bisa dijadikan.

Konsep Mudah Belajar Teori Asam Basa LewisKimia SMA YouTube
Contoh Reaksi Asam-Basa Lewis. Sementara teori Brønsted tidak dapat menjelaskan pembentukan ion kompleks dengan ion logam pusat, teori asam-basa Lewis melihat logam sebagai Asam Lewis dan ligan senyawa koordinasi sebagai Basa Lewis. Al 3+ + 6H 2 O [Al(H 2 O) 6] 3+

Peran Sentral Konsep AsamBasa dalam Reaksi Kimia Organik
Contoh Soal. 1. Tentukan manakah asam dan basa didalam reaksi asam basa berikut dengan cara memberikan alasan berdasarkan teori asam basa Brønsted-Lowry, Arrhenius, atau Lewis. Ni 2+ (aq) + 4CN - (aq) ⇌ [Ni(CN) 4] 2-(aq) Jawab: Teori Arrhenius serta teori Brønsted-Lowry tidak bisa menjelaskan reaksi diatas.

LENGKAP ‼️ Cara Mudah Menentukan Pasangan Asam Basa Konjugasi TeoriAsamBasa AsamBasaKonjugasi
Menurut Lewis, asam merupakan akseptor pasangan elektron dan basa merupakan pendonor pasangan elektron. Teori ini juga diklaim memiliki kelebihan dalam mengidentifikasi reaksi asam-basa yang berada dalam benda padat, gas, dan medium pelarut lain (bukan air biasa), serta tidak melibatkan transfer proton (teori Bronsted-Lowry).

27+ Contoh Soal Asam Basa Lewis Ike Hodge
Kelebihan teori asam basa Lewis yaitu dapat menjelaskan reaksi-reaksi asam-basa lain dalam fase padat, gas, dan medium pelarut selain air yang tidak melibatkan transfer proton.. 3−, [Al(H2O)6]3+, dan [Cu(NH3)4]2+, dan sebagian reaksi dalam kimia organik. Contoh Soal dan Pembahasan. Tentukan manakah asam dan basa dalam reaksi asam-basa.
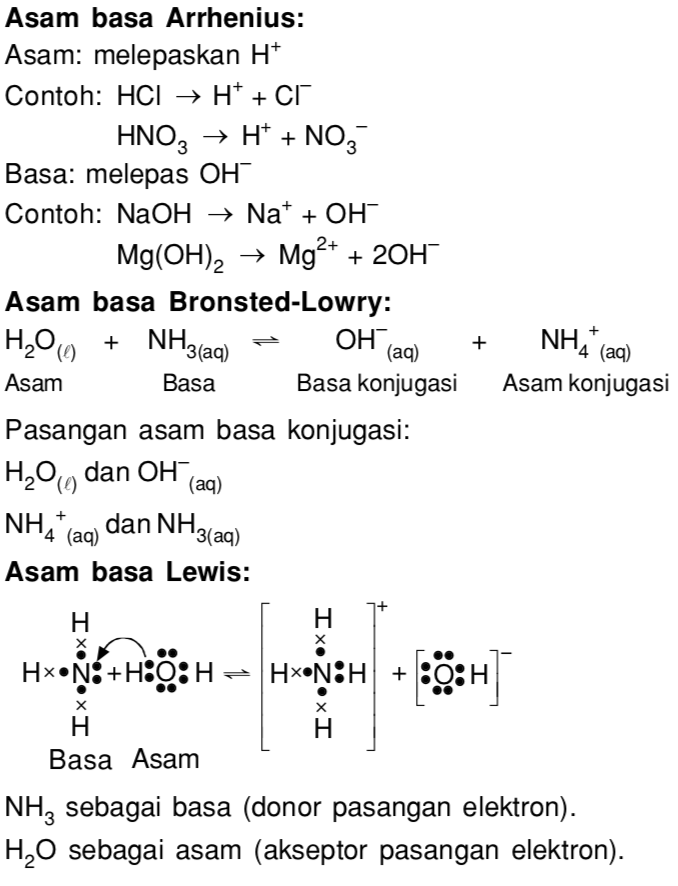
Contoh Soal Dan Jawaban Asam Basa Konjugasi Jawaban Buku
Berdasarkan contoh reaksi asam basa ini, Lewis menyatakan bahwa: Contoh lainnya adalah reaksi antara Na 2O dan SO 3 yang menghasilkan Na 2SO 4 tanpa terbentuk air seperti reaksi di bawah ini: Basa lewis dari reaksi di atas adalah ion oksida sedangkan sulfur trioksida adalah asam Lewis. Reaksi di atas menggambarkan keterbatasan teori

LENGKAP ‼️ Teori Asam Basa Lewis Latihan Soal dan Pembahasan YouTube
Kelebihan teori asam basa Lewis adalah: Dapat mengklasifikasikan asam dan basa dalam berbagai pelarut (selain air) dan juga tanpa pelarut. Dapat menjelaskan reaksi asam-basa tanpa transfer proton. Dapat menjelaskan sifat asam asa zat yang memiliki elektron bebas. Memperluas definisi asam basa, seperti pada pembuatan ion kompleks.

Asam Basa Teori, Contoh, dan Sifat Asam Basa InformasainsEdu
Berdasarkan definisi Lewis, asam yang berperan sebagai spesi penerima pasangan elektron tidak hanya H +. Senyawa yang memiliki orbital kosong pada kulit valensi seperti BF 3 juga dapat berperan sebagai asam. Sebagai contoh, reaksi antara BF 3 dan NH 3 merupakan reaksi asam-basa, di mana BF 3 sebagai asam Lewis dan NH 3 sebagai basa Lewis.
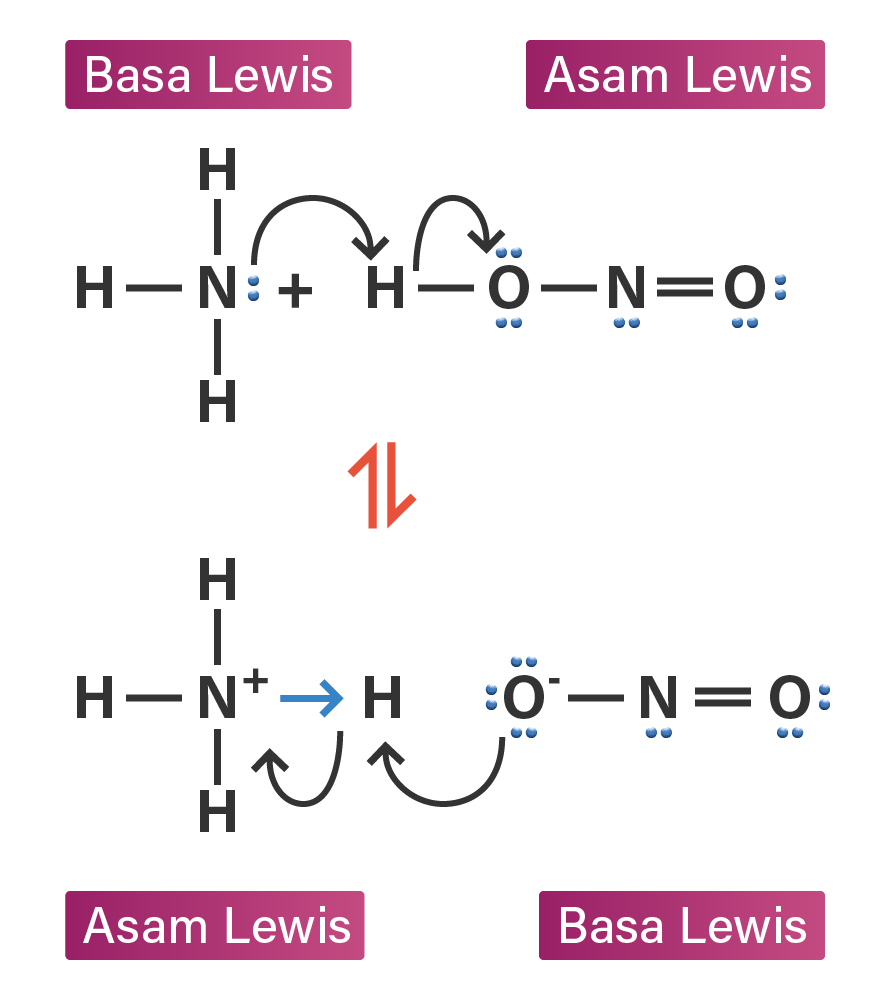
tuliskan pasangan asam basa lewis dari reaksi beri...
Kelemahan dari teori Brønsted-Lowry yaitu teori Brønsted-Lowry tidak dapat menjelaskan reaksi asam-basa yang tidak melibatkan transfer proton (H +).. Namun, spesi yang berperan sebagai asam Lewis tidak selalu menyediakan orbitasl kosong. Contoh asam lewis yaitu: H + B 2 H 6; BF 3; AlF 3; Fe 2+ Cu 2+ Zn 2+ 2. Contoh Basa Lewis.
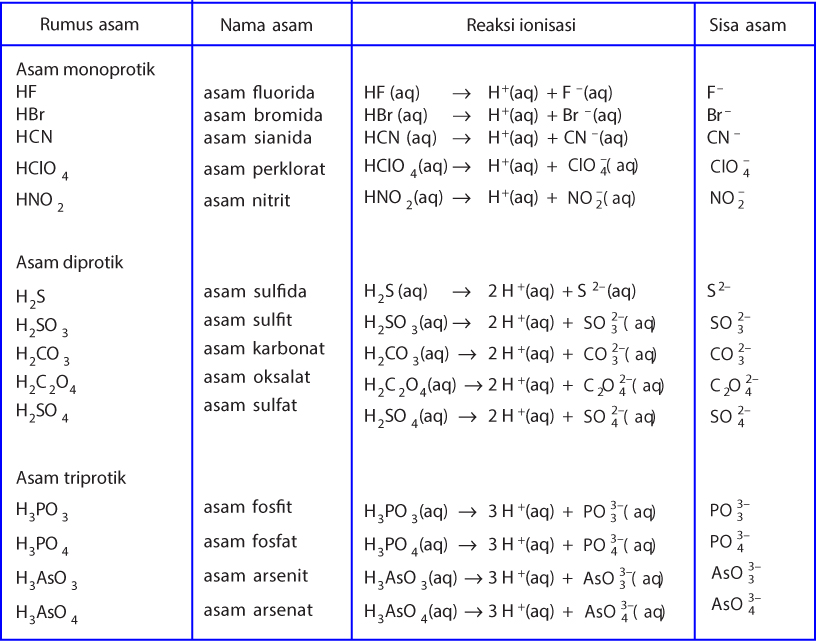
Teori Asam Dan Basa Menurut Arrhenius, BronstedLowry, dan Lewis
Basa = penerima H+. Reaksi kimia yang bisa dijadikan contoh berdasarkan teori Bronsted-Lowry misalnya pada asam klorida (HCL) dan air (H2O) berikut ini: HCl + H2O ⇌ H3O+ + Cl-. Penjelasannya seperti mengutip pada emodul Kemdikbud: HCL bersifat asam karena itu ia mendonorkan ion H+ nya kepada H20. H20 bersifat basa karena ia menerima donor H+.
PPT ASAM DAN BASA PowerPoint Presentation, free download ID4714427
Kekurangan Teori Asam Basa Lewis. Walaupun memiliki beberapa kelebihan, teori asam basa Lewis juga mempunyai kekurangan yang perlu diketahui. Teori asam dan basa Lewis ini cukup sulit untuk menggambarkan reaksi asam-basa, seperti reaksi antara ion Fe3+ dan ion CN-. Sebab keduanya tidak melibatkan ion H+ atau ion OH-.

Teori Asam Basa
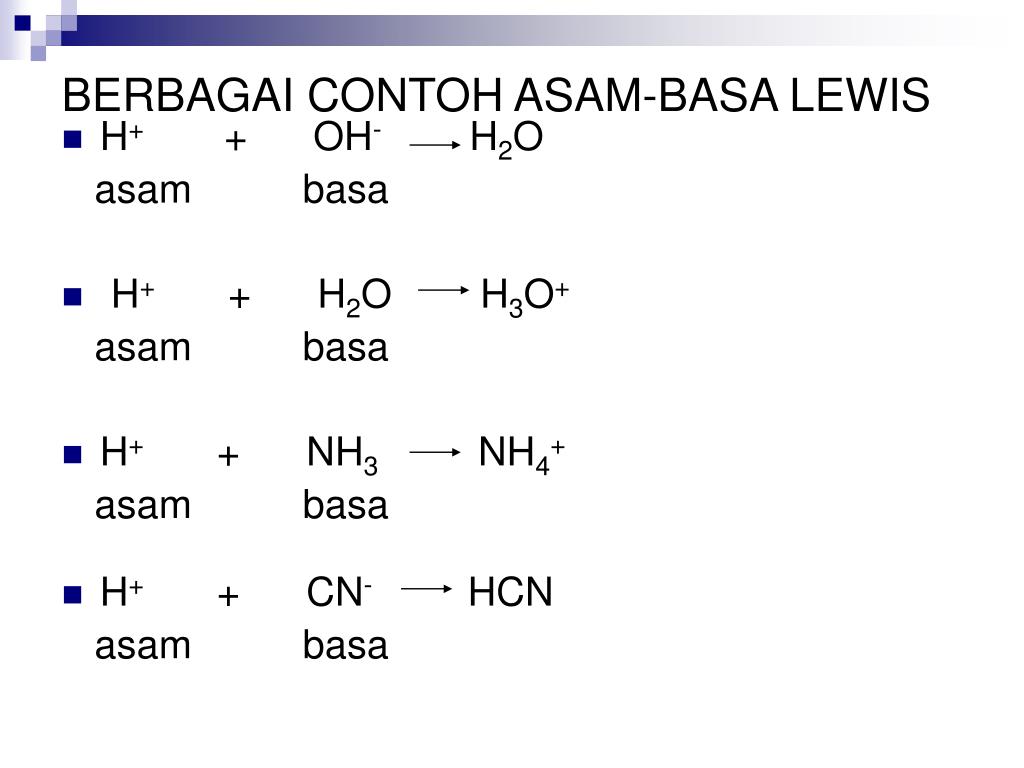
Contoh Teori Asam dan Basa Menurut Lewis pada Gambar diatas telah menunjukan bahwa Ion H+ (Proton) ialah Asam Lewis karena mampu menerima Pasangan Elektron, sedang NH3 merupakan Basa Lewis.. Newton Lewis lebih luas dan lengkap jika sepanjang yang dibahas didalamnya ialah Senyawa tanpa Proton, namun jika Reaksi Asam Basa yang melibatkan.

studying chemistry belajar kimia Teori Asam Basa Lewis
Sedangkan basa menurut Newton Lewis merupakan zat yang mampu memberikan pasangan pada electron. Dalam pandangan teori asam basa Lewis, basa memiliki pasangan yang elektronnya bebas, contohnya adalah seperti NH3, Cl-, maupuan ROH. Lebih lanjut, Lewis berpandangan bahwa reaksi dari asam dan basa adalah reaksi dari serah terima pasangan elektron.

Contoh Soal Asam Basa Lewis Asam Basa Pengertian Teori Reaksi Indikatornya Lengkap Contoh
Konsepkan mudah belajar teori asam basa lewis . dimana asam adalah penerima pasangan elektron sedangkan basa adalah pemberi pasangan elektron. Kimia SMA