Sifat Koligatif Larutan (Molalitas, Fraksi Mol, Penurunan Tekanan Uap, Titik Didih, Titik Beku
Contoh Soal Molalitas Larutan. Diketahui natrium hidroksida (NaOH) sebnayak 10 gram dengan massa molekul relatif 40 dilarutkan ke dalam air sebanyak 2 kg. Tentukan molalitas larutan NaOH. Pembahasan. m = n / P. n = 10 / 40 mol. n = 0,25 mol. m = 0,25 / 2 molal. m = 0,125 molal.

Perbedaan Molaritas Dan Molalitas Riset
Jawaban: m = n / P. m = 0,36 / 2. m = 0,18. Apabila Grameds hendak memahami rumus normalitas, molaritas, molalitas dengan lebih baik, pastikan untuk memahami pengertian, rumus dan contoh soalnya. Selain itu, latihlah pengetahuan rumus ini dengan menjawab beberapa contoh soal berdasarkan rumus tersebut. Apabila masih merasa kesulitan, Grameds.

Molalitas Pengertian, Satuan, Rumus, dan Contoh Soal Menghitungnya
Molalitas - Pengertian, Rumus, dan Contoh Soal. Molalitas suatu larutan bisa diuji dengan menambahkan beberapa zat pelarut. Pada waktu membuat sirup, kamu tentu melarutkan sirup ke dalam air, semakin banyak sirup yang dilarutkan semakin manis minuman yang terjadi. Sirup disebut zat terlarut (solute) dan air disebut zat pelarut (solvent).

Fraksi mol dan molalitas (m) Soal dan Pembahasan KIMIA KELAS 12 YouTube
Memahami Rumus Molaritas dan Molalitas Serta Pembahasan Soal. Molaritas adalah jumlah mol suatu zat yang bisa larut dalam setiap liter larutan. Molaritas termasuk satuan konsentrasi dalam Sistem Internasional (SI). Satuan molaritas yaitu mol/L atau molL-1. Artinya 1 mol zat terlarut apapun dalam 1 L pelarut memiliki konsentrasi 1,0 mol/L.
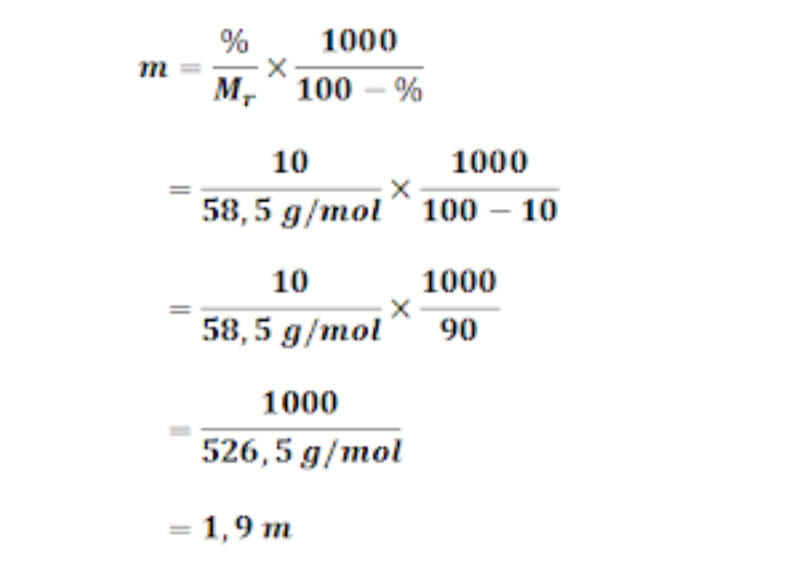
Cara Menghitung dan Contoh Soal Fraksi Mol dan Jawabannya Rumus dan Pembahasan Fraksi Mol
Contoh soal 1. Tentukan molaritas larutan yang dibuat dengan melarutkan: 0,8 mol NaCl dalam 250 mL air; 0,5 mol KOH dalam 1000 mL air; Pembahasan. Untuk menjawab soal ini ubah satuan volume menjadi liter. 250 mL = 0,25 L dan 1000 mL = 1 L, Jawaban soal 1: M = n. V = 0,8 mol. 0,25 L = 3,2 mol/L Jawaban soal 2 M =

Rumus Molalitas dan Contoh Soal dan Pembahasannya!
Contoh Soal dan Pembahasan Molalitas. Soal Sifat Koligatif Larutan. Sebelumnya Mafia Online sudah membahas materi tentang Molalitas yang juga sudah disertai dengan beberapa contoh soal. Postingan ini Mafia Online hanya membahas tentang contoh soal molalitas. Semoga dengan soal-soal ini Anda bisa memahami konsep dan cara menghitung molalitas.

Perbedaan Molaritas Dan Molalitas Riset
Postingan ini membahas contoh soal molalitas dan fraksi mol yang disertai pembahasannya atau penyelesaiannya. Molalitas adalah jumlah mol zat terlarut didalam setiap 1 kg atau 1000 gram pelarut. Sedangkan fraksi mol menyatakan satuan konsentrasi yang semua komponen larutannya dinyatakan berdasarkan mol. Rumus molalitas Rumus molalitas sebagai berikut: m = jumlah mol zat terlarut jumlah kg

Contoh Soal Molaritas Youtube Riset
Ingat, rumus molaritas pencampuran adalah: Maka, konsentrasi larutan setelah dicampurkan adalah: M campuran = (100 x 0,1) + (150 x 0,2) / (100 + 150) = 40 / 250. = 0,16 M. Quipperian, itu dia pembahasan mengenai rumus molaritas beserta contoh soal dan pembahasannya. Agar semakin paham dan mahir dalam menggunakan rumus molaritas, cobalah untuk.

Cara mudah mencari molaritas atau konsentrasi larutan soal kimia SMA YouTube
Contoh Soal Rumus Molaritas dan Molalitas. Biar kalian lebih paham lagi mengenai rumus Molaritas dan Molalitas serta perbedaannya, gua bakal kasih salah satu contoh soal… Berapa besar Massa glukosa (C 6 H 12 O 6) yang terdapat dalam 500 mL larutan glukosa 0,1 M? (Ar C = 12, H = 1, dan O = 16) A. 1.8 g B. 3.6 g

Molalitas dari 100 mL larutan H2SO4 5 M adalah (Mr H2SO4
Contoh Soal dan Pembahasan. Di atas kita sudah mengenal tentang molaritas dan molalitas, mulai dari pengertian hingga rumusnya. Supaya elo makin paham dengan materi rumus molaritas dan molalitas, gue sudah menyediakan contoh soal dan pembahasannya nih. Elo siapkan alat tulisnya juga ya untuk ikut mengerjakan! Contoh Soal 1

Contoh Soal Molalitas dan Fraksi Mol larutan LABORATORIUM SMK
Pengertian Molalitas — ciri, kelebihan, rumus, contoh, perbedaan. Molalitas: Satuan pengukuran Sistem Satuan Internasional untuk menyatakan konsentrasi suatu larutan, simbolnya adalah m. Molalitas adalah rasio jumlah mol setiap zat terlarut per kilogram pelarut (m). Satuan kilogram digunakan pada skala industri, namun, untuk percobaan yang.

Menghitung Molalitas Larutan Jika Diketahui Molaritas dan Kerapatan Larutannya YouTube
Molalitas: Pengertian, Rumus, Satuan dan Contoh Soalnya. Ketika Sedulur mempelajari ilmu kimia, salah satu materi atau topik yang biasanya muncul adalah molalitas. Ia merupakan sebuah ukuran konsentrasi atas suatu zat yang terlarut dalam suatu larutan kimia. Nama lain dari ukuran konsentrasi zat tersebut adalah konsentrasi molal.

Contoh Soal Molalitas Homecare24
Contoh Soal Molalitas dilansir buku 'Praktis Belajar Kimia' karya Iman Rahayu. 1. Sebanyak 30 gram urea (Mr = 60 g/mol) dilarutkan ke dalam 100 gram air. Hitunglah molalitas larutan. Cara mengerjakan contoh soal molalitas: Mol urea = massa urea = 30 g = 0,5 mol. Mr urea 60 g/mol. Massa pelarut = 100 g = 100 = 0,1 kg. 1.000.

Detail Contoh Soal Molaritas Dan Molalitas Koleksi Nomer 11
Perhitungan Molalitas - Materi Kimia berikut tentang Perhitungan Molalitas. Dalam perhitungan molaritas, kuantitas larutan didasarkan pada volume.. Perhatikanlah contoh soal penentuan molalitas berikut. Contoh Perhitungan Molalitas. Sebanyak 30 g urea (M r = 60 g/mol) dilarutkan ke dalam 100 g air. Hitunglah molalitas larutan.

contoh soal Molaritas, Molalitas, dan Fraksi Mol Kimia XII IPA SMA Negeri 1 Tanjung Palas
Satuan molalitas. Molalitas adalah besaran turunan yang memiliki satuan. Dilansir dari ChemistryGod, satuan standar molalitas adalah mol per kilogram (mol/kg) atau kerap disebut sebagai molal. Molal biasanya dilambangkan dengan huruf "m". Misalnya, molalitas suatu larutan adalah 12 mol/kg, maka dapat dinyatakan sebagai 12 molal atau 12 m.

Contoh Soal Molaritas Molalitas Dan Fraksi Mol Pusat Soal
Contoh perhitungan molalitas larutan. Misalnya 10 gram natrium hidroksida (NaOH) dilarutkan dalam 2 kg air. Massa molekul relatif NaOH yaitu 40. Molalitas larutan bisa dihitung dengan cara : Jumlah mol NaOH, n = gram/Mr = 10/40 = 0,25 mol Molalitas larutan, m = n/P = 0,25/2 = 0,125 molal