
Contoh Soal Hukum Hess
Hukum-hukum yang terkait dengan termokimia adalah hukum Hess yang dikemukaan oleh German Henry Hess pada tahun 1849.. Baca juga: Perubahan Entalpi pada Reaksi Kimia Hukum Hess. Dilansir dari bbc.co.uk, hukum hess menjelaskan bahwa setiap reaksi kimia memiliki perubahan total entalpi yang tetap dan tidak tergantung pada tahapan atau jalur reaksinya.. Maka perubahan entalpi hanya bergantung pada.
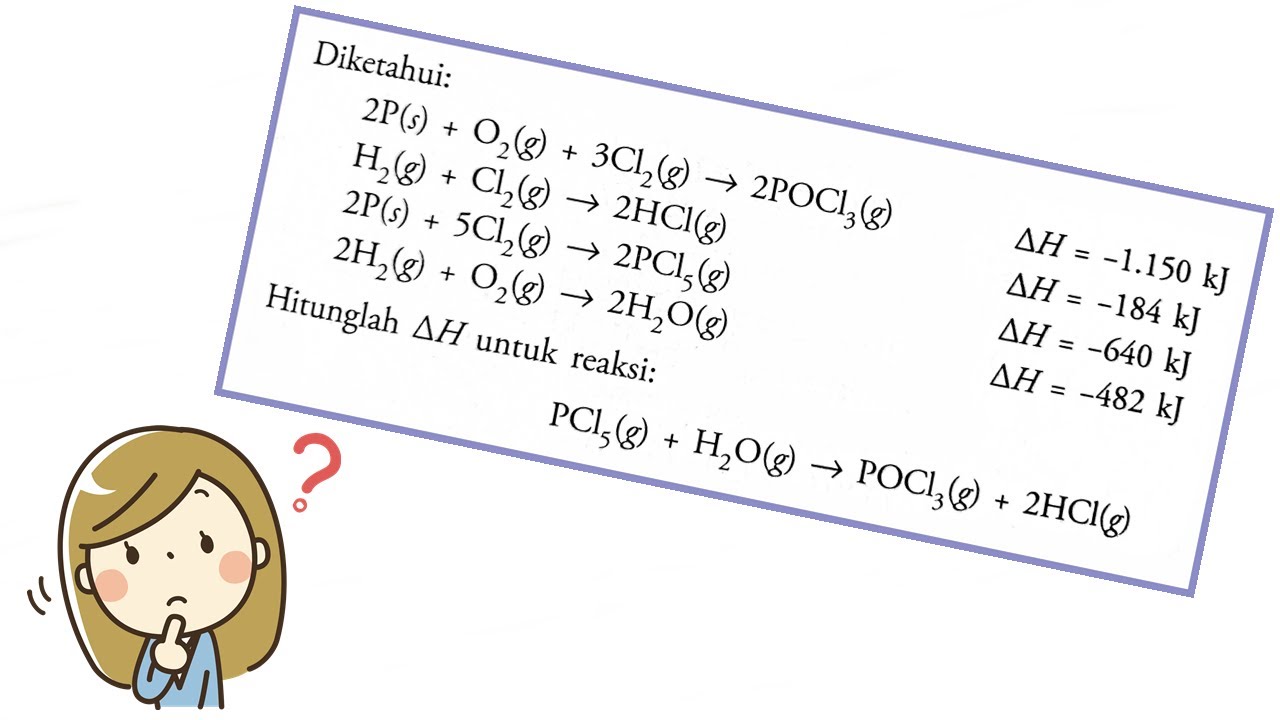
Pembahasan Soal Termokimia Hukum Hess dengan Susun Reaksi (1) YouTube
Video penjelasan Hukum Hess dan cara menentukan entalpi reaksi menggunakan Hukum Hess beserta contoh soal.Kimia Kelas 11#hukumhess

Contoh Soal Hukum Hess YouTube
Menelaah Rumus Hukum OHM dan Contoh Soalnya. Terdapat 3 cara untuk mencari ∆Hreaksi menggunakan Hukum Hess sebagai berikut. 1. Cara Diagram. Sesuai dengan Hukum Hess, yang diperhatikan adalah awal dan akhir diagram. Dari diagram diketahui bahwa reaksi 1/2N₂ (g)+O₂ (g) sebesar -90,25 kj dan NO₂ (g) sebesar -57,05 kj.
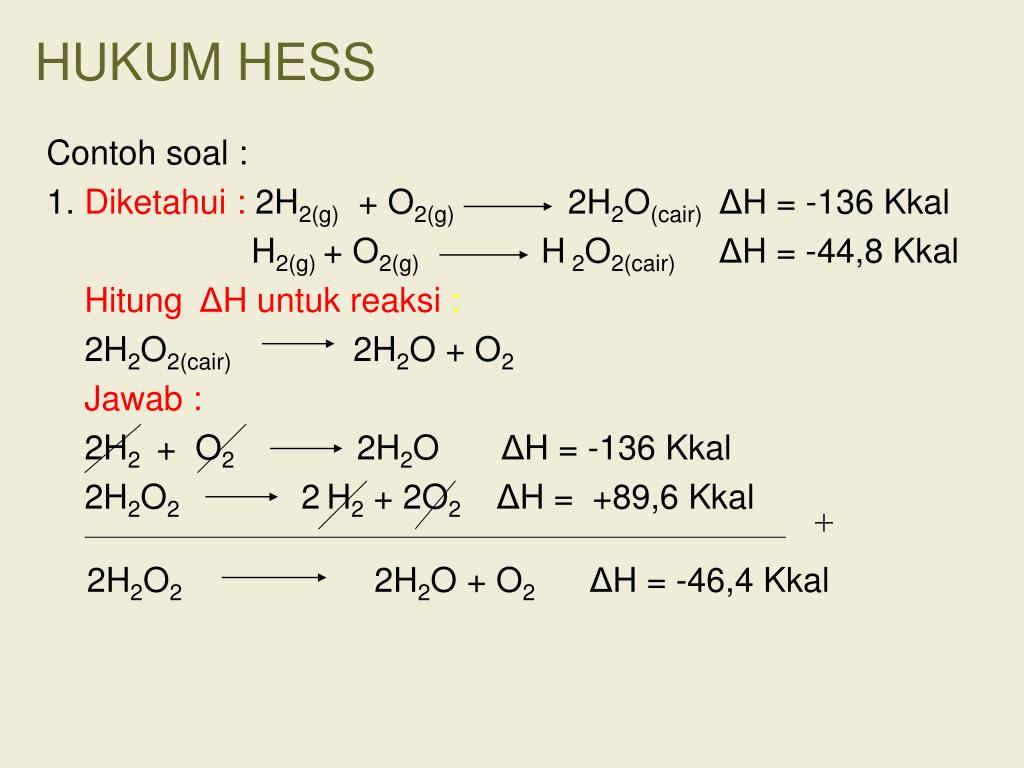
Soal Dan Pembahasan Hukum Hess
Contoh Soal Hukum Hess dan Penyelesaian. Hukum Hess berbunyi "perubahan entalpi suatu reaksi hanya tergantung pada keadaan awal (zat-zat pereaksi) dan keadaan akhir (zat-zat hasil reaksi) dari suatu reaksi kimia dan tidak bergantung pada jalannya reaksi. Secara matematis, Hukum Hess dirumuskan sebagai berikut, ∆H reaksi = ∆H 1 + ∆H 2.

KELAS 11 IPA LATIHAN SOAL HUKUM HESS
Video ini berisi penjelasan lengkap, contoh-contoh soal dan pembahasan tentang cara menghitung perubahan entalpi dengan menggunakan hukum Hess.Semoga video i.

Contoh Soal Hukum Hess Bentuk Bagan YouTube
Contoh soal hukum Hess nomor 6. Diagram tahap reaksi pembentukan gas SO 3 adalah sebagai berikut. Contoh soal hukum Hess nomor 6. Berdasarkan diagram tersebut, harga ΔH 2 adalah. A. 790,4 kj B. 593,8 kj C. 250,6 kj D. -250,6 kj E. -593,8 kj. Pembahasan. Menurut hukum Hess, pada gambar diatas berlaku: ΔH 3 = ΔH 1 + ΔH 2; ΔH 2 = ΔH 3.

Contoh Soal Hukum Hess dengan menggunakan data delta Hf (di akhir ada cara cepatnya) YouTube
Hukum Hess menyatakan bahwa perubahan entalpi keseluruhan dari suatu proses hanya tergantung pada keadaan awal dan akhir reaksi, dan tidak tergantung kepada rute atau langkah-langkah diantaranya. Dengan mengetahui ΔH f (perubahan entalpi pembentukan) dari reaktan dan produknya, dapat diramalkan perubahan entalpi reaksi apapun, dengan rumus.

Contoh Hukum Hess
Perhatikan contoh berikut. Dalam penerapan hukum Hess, kadangkala persamaan termokimia yang tersedia perlu dimanipulasi terlebih dahulu. Berikut aturan dalam memanipulasi persamaan termokimia: Ketika persamaan reaksi dibalik (reaktan menjadi produk, produk menjadi reaktan), tanda nilai ΔH juga harus dibalik (dari positif menjadi negatif, dan.

Contoh Soal Hukum Hess Dan Penyelesaiannya Gudang Materi Online
Contoh Hukum Hess. Pada diagram di atas, jelas bahwa jika C ( s) + 2H 2 ( g) + O 2 ( g) direaksikan menjadi CO 2 ( g) + 2H 2 ( g) mempunyai perubahan entalpi sebesar -393,5 kJ. Walaupun terdapat reaksi dua langkah, tetap saja perubahan entalpi akan selalu konstan (-483,6 kJ + 90,1 kJ = -393,5 kJ). Hukum Hess menyatakan bahwa perubahan entalpi.

Hukum Hess KIMIA KELAS 11 YouTube
Contoh Soal Terkait Hukum Hess dan Pembahasannya. Berikut ini adalah beberapa contoh soal yang menerapkan aturan Hess: Soal 1. Hitung perubahan entalpi standar untuk reaksi. CO₂ (g) + H₂ (g) → CO (g) + H₂O (g) Mengingat bahwa ΔH untuk senyawa CO₂ (g), CO (g) dan H₂O (g) masing-masing sebesar -393,5 kJ/mol, -110,5 kJ/mol, dan 241,8.

Pembahasan Soal Termokimia Hukum Hess (3) (Cara Menentukan ΔHf CH4 & Diagram Tingkat Energinya
Berikut adalah contoh soal hukum Hess dalam kimia: Diberikan reaksi: 2H2 (g) + O2 (g) → 2H2O (g) ΔH1 = -484 kJ/mol H2 (g) + 1/2O2 (g) → H2O (l) ΔH2 = -286 kJ/mol Hitung ΔH untuk reaksi: H2 (g) + 1/2O2 (g) → H2O (g) Jawaban: Untuk menghitung ΔH reaksi ini, kita harus menggunakan hukum Hess. Kita dapat memecah reaksi yang diinginkan.

Gunakan hukum Hess untuk menghitung perubahan entalpi rea...
Hukum Hess adalah hukum yang digunakan untuk menentukan besarnya perubahan entalpi suatu reaksi. Dalam hukum Hess, nilai perubahan entalpi dinyatakan sebagai fungsi keadaan (∆ H).Menurut hukum ini, karena perubahan entalpi merupakan fungsi keadaan maka perubahan reaksi kimia akan bernilai sama meskipun langkah-langkah yang diperlukan untuk menghasilkan hasil reaksi berbeda.
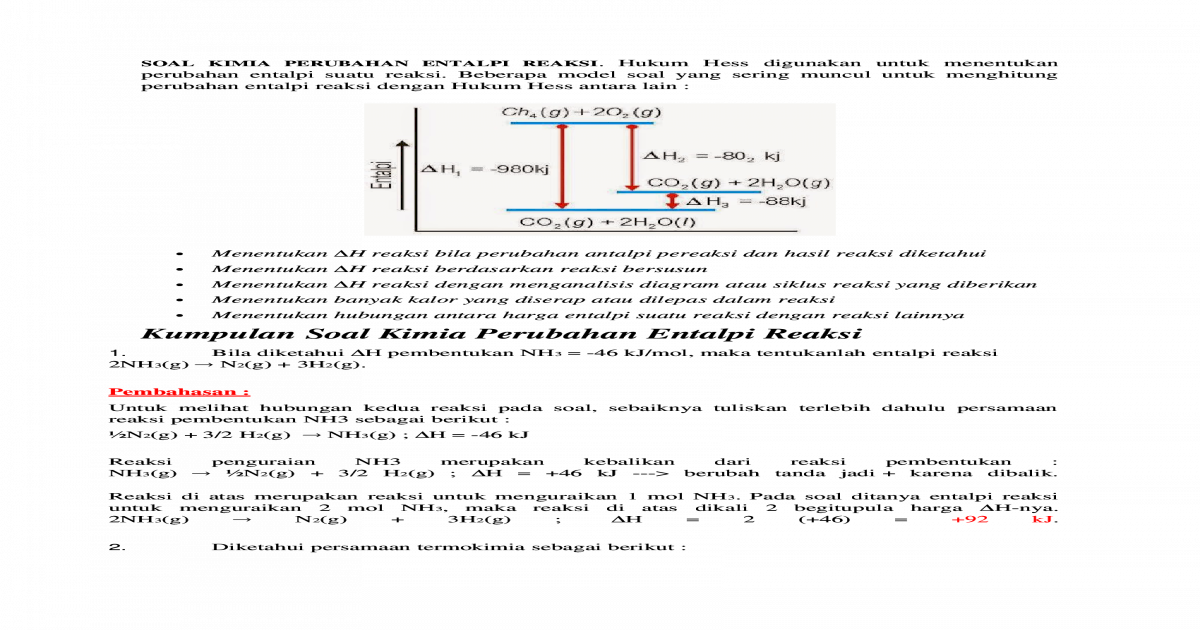
Contoh Soal Hukum Hess LEMBAR EDU
Latihan Soal Hukum Hess (Sukar) Penguraian 3,6 gram besi (II) oksida dibutuhkan energi 13,6 kJ. Penguraian 4 gram besi (III) oksida dibutuhkan energi 20,605 kJ. Pembentukan 9,28 gram Fe3O4 dilepaskan energi 44,736 kJ. Berdasarkan data di atas berapakah ΔH reaksi dari Fe3O4(s) → FeO(s)+ Fe2O3(s) adalah. .

Contoh Soal Dan Jawaban Menentukan Entalpi Berdasarkan Hukum Hess
ΔH 1 = ΔH 2 + ΔH 3. x = y + z. Menurut Hukum Hess : ΔH 1 = ΔH 2 + ΔH 3 atau x = y + z. Perubahan yang terjadi dari N 2 g) dan O 2 g) menjadi NO (g) disertai dengan adanya perubahan entalpi (ΔH 1) sebesar +33,85 kJ/mol, walau pun reaksi telah ditetapkan dalam satu tahap atau pun dua tahap, ΔH 1 = ΔH 2 + ΔH 3.

Soal Hukum Hess LEMBAR EDU
Contoh Soal dan Pembahasan Hukum Hess. Tentukah ΔH dari diagram di bawah ini: Perhatikan gambar di atas bahwa jika C (s) + 2H 2 (g) + O 2 (g) direaksikan menjadi CO 2 (g) + 2H 2 (g) mempunyai perubahan entalpi sebesar -393,5 kJ. Meskipun terdapat reaksi dua langkah, tetap saja perubahan entalpi akan selalu konstan :

Contoh Soal Hukum Hess Bentuk Reaksi YouTube
Contoh Soal Hukum Hess. Pada diagram di atas, jelas bahwa jika C (s) + 2H2 (g) + O2 (g) direaksikan menjadi CO2 (g) + 2H2 (g) mempunyai perubahan entalpi sebesar -393,5 kJ. Walaupun terdapat reaksi dua langkah, tetap saja perubahan entalpi akan selalu konstan (-483,6 kJ + 90,1 kJ = -393,5 kJ). Demikian penjelasan materi kimia mengenai Hukum.