
Cara Menghitung Ph Larutan Asam Basa Garam Beserta Contoh Soal Dan Rezfoods Resep Masakan
Sebagai informasi tambahan, garam dari asam lemah dan basa lemah atau terjadinya reaksi garam yang terhidrolisis sempurna, bergantung pada nilai Ka dan Kb.. Adapun contoh garam yang tidak terhidrolisis adalah garam yang berasal dari asam kuat dan basa kuat. Pelarutan garam ini tidak akan mengubah jumlah [H+] dan [OH-] dalam air, sehingga.

PPT BAB 2 ASAM, BASA DAN GARAM PowerPoint Presentation, free download ID5075424
Garam dari asam kuat dan basa lemah, garam ini bersifat asam (pH <7). Contohnya adalah Zn(ClO 4) 2, NH 4 Cl, AlCl 3, Fe(NO 3) 2. Garam dari basa kuat dan asam lemah, garam ini bersifat basa (pH >7). Contohnya adalah Na 2 SO 3, KCN, Na 2 CO 3, (CH 3 COO) 2 Ca. Garam dari asam lemah dan basa lemah, sifat asam/basa bergantung pada nilai Ka dan Kb dari

sifat bahan asam dan basa Ava
Pengertian Asam, Basa, Garam, Ciri, Sifat, Indikator, Gambar dan Contoh : Asam adalah senyawa kimia yang bila dilarutkan dalam air akan menghasilkan larutan dengan pH lebih kecil dari 7.Basa adalah senyawa kimia yang menyerap ion hidronium ketika dilarutkan dalam air. Basa memiliki pH lebih besar dari 7. Garam atau "Natrium Klorida" (Nacl) adalah senyawa ionik yang terdiri dari ion positif.

Perhitungan pH Garam dari Asam lemah dan Basa Lemah
Oleh karena itu, larutan garam dari asam lemah dan basa kuat akan meningkatkan konsentrasi OH − dalam air sehingga larutannya bersifat basa (pH > 7).. Garam dari asam lemah dan basa lemah. Garam seperti CH 3 COONH 4 yang dapat terbentuk dari reaksi asam lemah (CH 3 COOH) dan basa lemah (NH 3) akan mengalami hidrolisis kation dan anionnya. pH larutan garam demikian bergantung pada kekuatan.
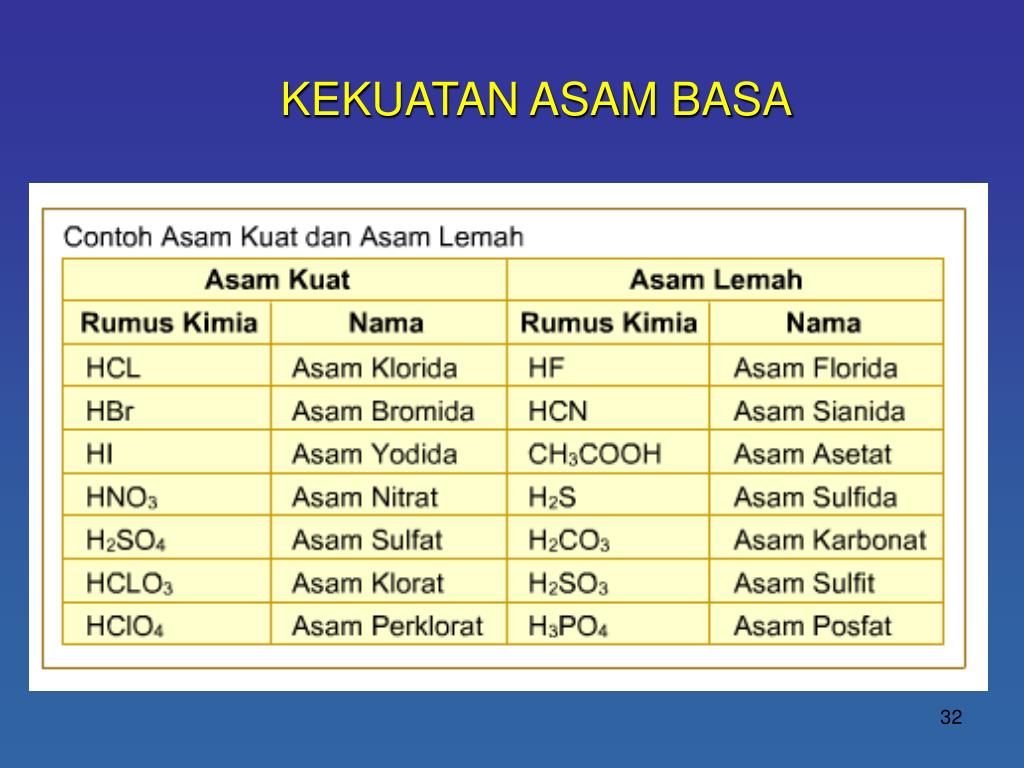
Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah Berbagai Contoh
2. Reaksi antara asam kuat dan basa lemah. Reaksi asam dan basa juga bisa terjadi pada larutan dengan asam kuat dan larutan dengan basa lemah. Contoh: HBr (aq) + NH 3(aq) → NH 4 Br (aq) Dari contoh di atas, dapat diketahui bahwa HBr adalah asam kuat, sedangkan NH3 adalah basa lemah. Hasil reaksi antara asam kuat dan basa lemah ini dapat.

PERHITUNGAN pH ASAM LEMAH DAN BASA LEMAH YouTube
Oleh karena itu garam dapat terbentuk dari 4 reaksi hidrolisis kimia sebagai berikut: Garam yang berasal dari asam lemah dan basa kuat bersifat netral dan memiliki pH = 7, yang artinya tidak terjadi hidrolisis. Garam dari asam kuat dan basa lemah, di mana garam ini akan memiliki pH < 7 alias bersifat asam. Garam dari asam lemah dan basa kuat.

Mengenal Asam Basa Sifat, Cara Membedakan, dan Klasifikasinya Kimia Kelas 11
2. Asam Lemah dan Basa Lemah. Asam lemah merupakan senyawa yang sedikit terurai pada waktu dilarutkan didalam air. Contohnya: H 3 PO 4, H 2 SO 3, HNO 2, CH 3 COOH. Basa lemah merupakan senyawa yang cuma sedikit terurai pada waktu dilarutkan kedalam air. Contohnya: NaHCO 3, NH 4 OH. Lalu berdasarkan bentuk ionnya, asam basa diklasifikasikan menjadi:
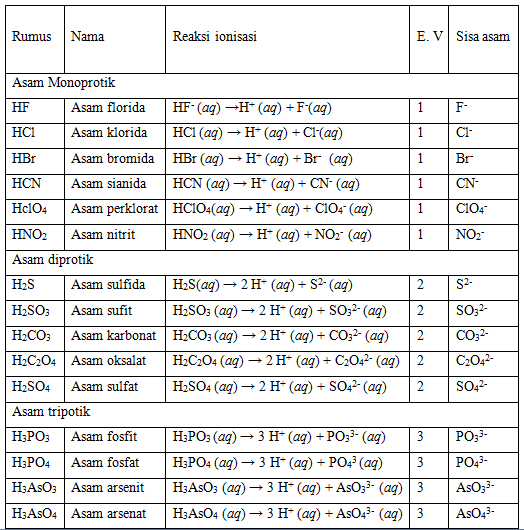
Teori Asam Basa Dan Garam Fisika Dan Matematika kulturaupice
Contoh dari senyawa garam jenis ini adalah NH4Cl yang merupakan garam yang terbentuk dari asam kuat HCl dan basa lemah NH4OH. Asam Lemah - Basa Lemah. Ketika asam lemah dan basa lemah bereaksi, maka garam yang terbentuk akan mengalami hidrolisis total yang artinya seluruh senyawa garam dapat terurai dengan air.

Contoh Asam Lemah Dan Basa Lemah Brain
Garam asam adalah garam yang berasal dari asam kuat dan basa lemah bersifat, contoh garam asam adalah NH 4 Cl. Garam basa yang berasal dari asam lemah dan basa kuat bersifat basa. Contoh garam basa adalah CH 3 COONa. Contoh asam kuat adalah HCl, HNO 3 ,H2SO 4. Adapun KOH, NaOH, Ca (OH) 2 termasuk basa kuat.

Rangkuman Materi Asam, Basa, Garam
Garam dari asam lemah dan basa kuat jika di hidrolisis akan menghasilkan larutan basa. Misalnya garam natrium flurida (NaF) yang terbentuk dari asam lemah flurida (HF) dan basa kuat natrium hidroksida (NaOH).. Pengertian, Manfaat, dan Contoh dari Sikap Tenggang Rasa. Skola. 04/03/2024, 22:30 WIB. Cause and Effect: Karakteristik, Fungsi, dan.

Hidrolisis Garam Pengertian, Macam, Dan Rumus, Beserta Contoh Soalnya Secara Lengkap
Oksida asam + basa → garam + H2O. Contoh: SO3 + 2NaOH → Na2SO4 + H2O. Yap, dalam menentukan reaksi oksida ini memang agak ribet ya, guys. Karena kita harus tahu dulu oksida tersebut termasuk zat apa.. Reaksi bisa terjadi antara senyawa asam kuat-basa kuat dan asam lemah-basa lemah. Hasil dari reaksinya berupa garam dan H2O.

Hidrolisis Garam Pengertian Macam Rumus Dan Contoh Soal Sexiz Pix
Contoh hidrolisis amonium klorida (NH4Cl) yang terbentuk dari asam kuat dan basa lemah yaitu asam klorida (HCl) dan amonia (NH3). Amonia akan mengalami ionisasi terurai menjadi ion NH4+ dan Cl-. Perlu diingat bahwa ion Cl- dari asam kuat HCl tidak akan terhidrolisis oleh air, maka hanya ion NH4+ yang akan bereaksi dengan air dan meningkatkan.

Contoh Soal Hidrolisis Asam Lemah Dan Basa Lemah
Pembahasan : Hidrolisis yang berasal dari asam lemah dan basa lemah merupakan hidrolisis total, sebab kedua ion garam mengalami reaksi hidrolisis dengan air. Dari soal diatas penyusun dari garam NH 4 CN adalah NH 4 OH ( basa lemah ) dan HCN ( asam lemah ) Dan akan terjadi hidrolisis total. Maka NH 4 CN akan terionisasi menjadi NH 4+ dan CN - .
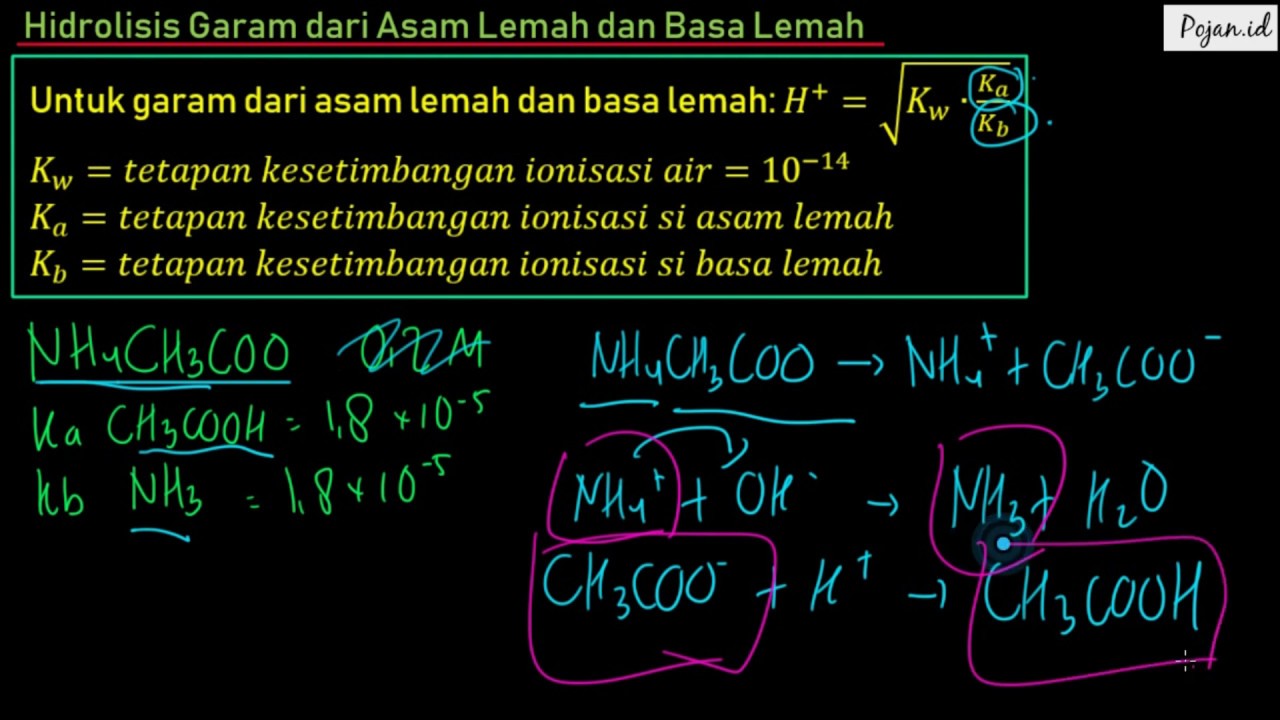
Hidrolisis Garam dari Asam Lemah dan Basa Lemah Materi Hidrolisis Garam Kimia SMA Pojan.id
Asam + basa → garam + air. HCl + KOH → KCl + H2O. Garam dapur (NaCl) diperoleh dari air laut yang mengalami penguapan dan kristalisasi. Untuk menjadikannya garam beryodium, harus diproses iodisasi (garam kalium/KI). Sifat-sifat atau ciri-ciri garam: Larut dalam air. Contohnya : KNO3, NH4Cl, Na2SO4. Sukar larut dalam air.

Detail Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah Koleksi Nomer 21
Berikut kami sajikan contoh asam kuat, asam lemah, basa kuat, basa lemah beserta rumus dan reaksi Ionisasinya. 7 Contoh asam kuat beserta rumus dan reaksi Ionisasinya. 1. Asam Klorida (HCl) Reaksi ionisasi: HCl → H+ + Cl- 2. Asam Nitrat (HNO3) Reaksi ionisasi : HNO3 → H+ + NO3- 3. Asam Sulfat (H2SO4) Reaksi ionisasi:

Contoh Asam Lemah Dan Basa Lemah Brain
Contoh asam lemah yaitu H 3 PO 4, H 2 SO 3, HNO 2, dan CH 3 COOH. Basa lemah adalah senyawa basa yang sulit melepaskan ion OH - dalam air dan mengalami disosiasi sebagian dalam larutannya. Contoh basa lemah yaitu NaHCO 3 dan NH 4 OH. Itu tadi pembahasan kita tentang asam basa, mulai dari sifat atau cirinya, cara membedekan, hingga.