PPT ASAM BASA PowerPoint Presentation, free download ID5640840
Reaksi NH4 ke NH3. Asam Basa Konjugat - Konjugasi Asam Basa - Rumus, Konjugat, Contoh Soal dan Jawaban. Dapat dikatakan bahwa molekul air adalah asam konjugat ion hidroksida setelah hidroksida mendapat proton hidrogen yang diberikan oleh amonium.Di sisi lain, amonia adalah basa konjugat untuk amonium asam setelah amonium telah menyerahkan ion hidrogen untuk menghasilkan molekul air.

lon HCO3^ bersifat asam maupun basa. Reaksi berikut yang...
Co3 memiliki banyak kegunaan di dalam industri, seperti dalam pembuatan semen dan kaca. Namun, co3 juga memiliki kekurangan yang perlu dipertimbangkan. Dalam artikel ini, akan dibahas secara detail mengenai kelebihan dan kekurangan co3 sebagai asam atau basa. Kelebihan Co3 Sebagai Asam atau Basa. 1. Stabil di dalam lingkungan kimia
PPT ASAM DAN BASA PowerPoint Presentation, free download ID1244635
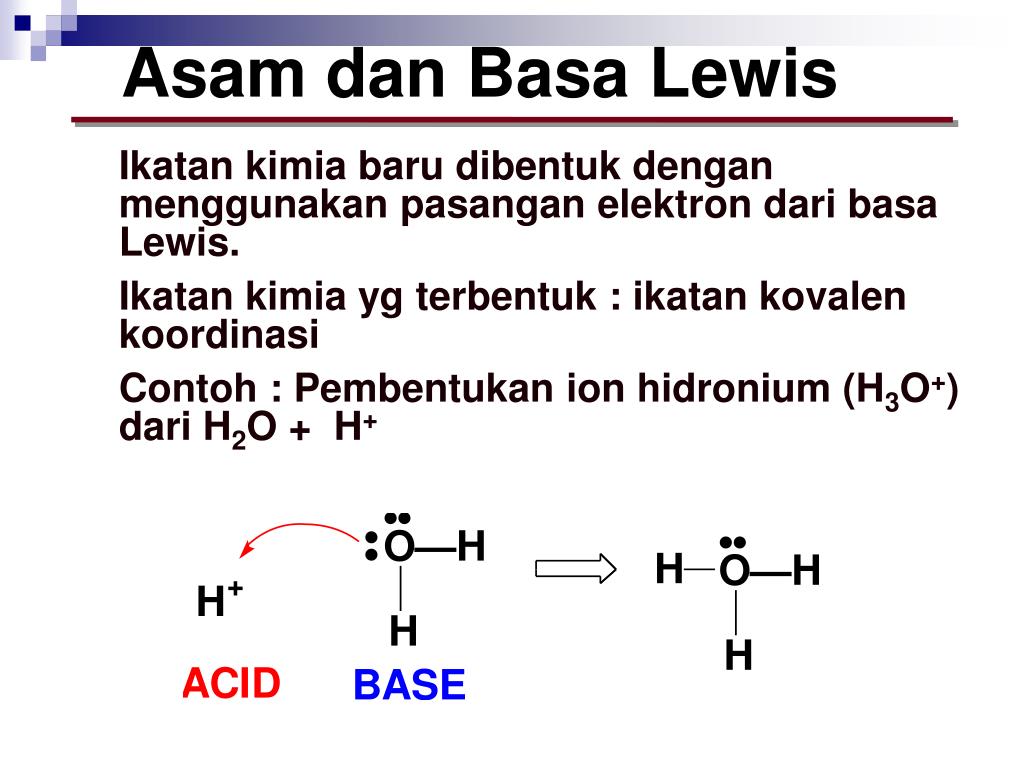
Ion HCO3− bersifat asam maupun basa, sehingga disebut sebagai amfoter. Secara umum, Bronsted-Lowry mendefinisikan asam dan basa sebagai berikut. Asam adalah pemberi/donor proton ( H+) Basa adalah penerima/akseptor proton ( H+) Reaksi yang menunjukkan bahwa HCO3− bersifat basa adalah. Pada reaksi ini, H2O memberi 1 proton ( H+) ke HCO3−.

Mengenal Asam Basa Sifat, Cara Membedakan, dan Klasifikasinya Kimia Kelas 11
Skala pH berkisar dari 0 hingga 14, di mana 0 menunjukkan larutan sangat asam, 7 adalah netral, dan 14 sangat basa. Ketika CO2 terlarut dalam air, ia bereaksi dengan air untuk membentuk asam karbonat. Asam karbonat memiliki efek menurunkan pH air, sehingga membuatnya lebih asam. Ini berarti bahwa kadar CO2 yang tinggi dapat membuat lingkungan.

Asam Basa Teori, Contoh, dan Sifat Asam Basa InformasainsEdu
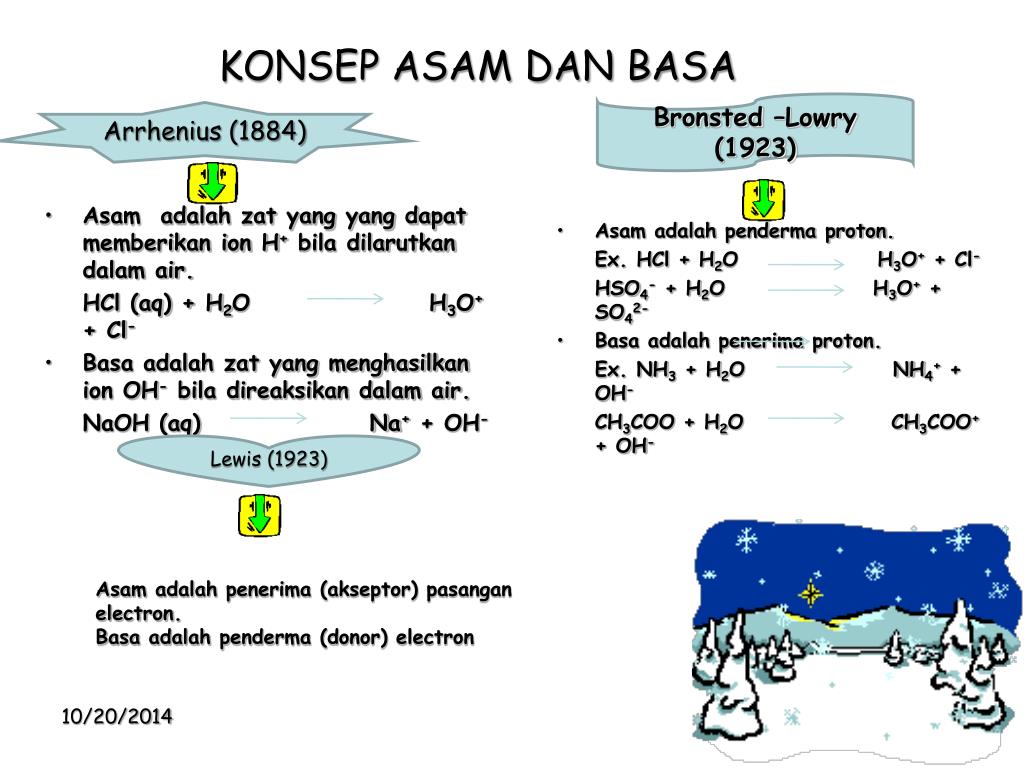
Pembahasan. Menurut Arrhenius, definisi dari asam dan basa, yaitu asam adalah senyawa yang jika dilarutkan dalam air melepaskan ion , sedangkan basa adalah senyawa yang jika dilarutkan dalam air melepaskan ion . Sedangkan garam merupakan zat hasil reaksi antara asam dan basa atau dengan kata lain garam terbentuk dari reaksi kation basa dengan.

Mengenal Asam Basa Sifat, Cara Membedakan, dan Klasifikasinya Kimia Kelas 11
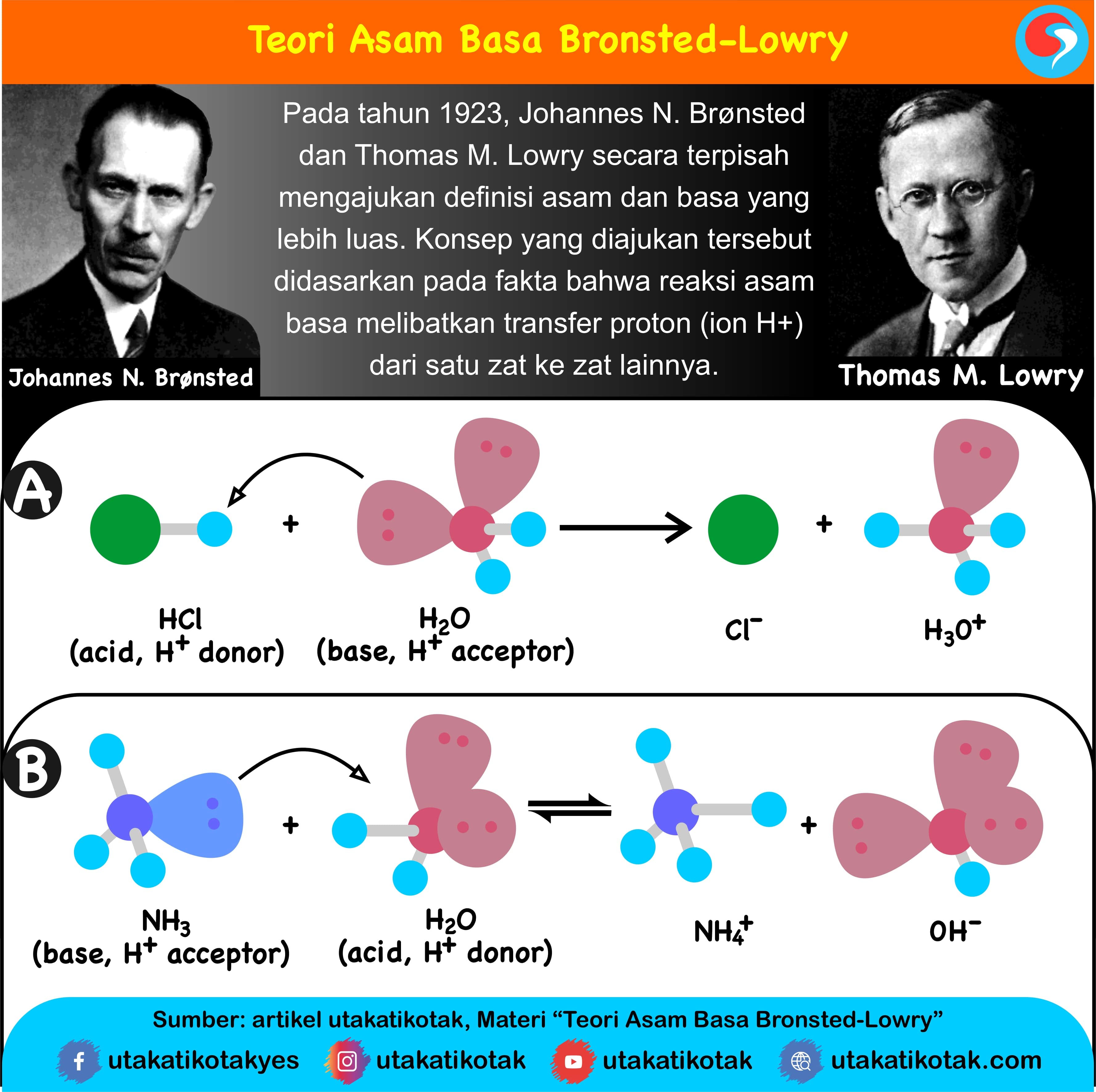
Basa = penerima H+. Reaksi kimia yang bisa dijadikan contoh berdasarkan teori Bronsted-Lowry misalnya pada asam klorida (HCL) dan air (H2O) berikut ini: HCl + H2O ⇌ H3O+ + Cl-. Penjelasannya seperti mengutip pada emodul Kemdikbud: HCL bersifat asam karena itu ia mendonorkan ion H+ nya kepada H20. H20 bersifat basa karena ia menerima donor H+.

PPT Konsep asam basa PowerPoint Presentation, free download ID6283281
Bikarbonat ( HCO− 3) bersifat alkalis, dan merupakan komponen vital pada sistem pendaparan pH [3] tubuh manusia (mempertahankan homeostatis asam-basa ). Sebanyak 70-75% CO2 dalam tubuh dikonversi menjadi asam karbonat ( H2CO3 ), yang dapat diubah dengan cepat menjadi bikarbonat. Dengan asam karbonat sebagai spesies intermediat pusat.

LENGKAP ‼️ Cara Mudah Menentukan Pasangan Asam Basa Konjugasi TeoriAsamBasa AsamBasaKonjugasi
Cara Membedakan Asam dan Basa. Senyawa asam dapat dengan mudah ditemukan pada buah-buahan, seperti jeruk dan lemon. Selain itu, bisa juga ditemukan pada bahan makanan, seperti cuka. Bahkan, senyawa asam juga banyak digunakan sebagai bahan pengawet makanan lho, misalnya asam benzoat yang dimanfaatkan sebagai pengawet jus buah dan selai.

Menentukan Asam Basa Konjugat BronstedLowry YouTube
Asam dan basa dapat bereaksi menghasilkan air serta senyawa ionic garam. Reaksi itu disebut reaksi netralisasi. Asam dan basa merupakan dua jenis larutan yang kerap digunakan dalam kehidupan sehari-hari manusia. Asam dan basa ada yang memiliki sifat kuat dan juga lemah. Berikut daftar nama asam kuat, asam lemah, basa kuat, dan juga basa lemah:
Teori Asam dan Basa Menurut BronstedLowry
Jenis Ikatan Kimia dan Sifat Elektrolit Suatu Zat. Lengkapi persamaan reaksi ionisasi asam basa berikut!a. CH3COOH b. H2CO3 c. HNO3 d. NH4OH e. Ca (OH)2. Jenis Ikatan Kimia dan Sifat Elektrolit Suatu Zat. Larutan Elektrolit dan Larutan Non-Elektrolit. Kimia Fisik dan Analisis.
Chocogreentea Keterbatasan Teori AsamBasa Bronsted Lowry
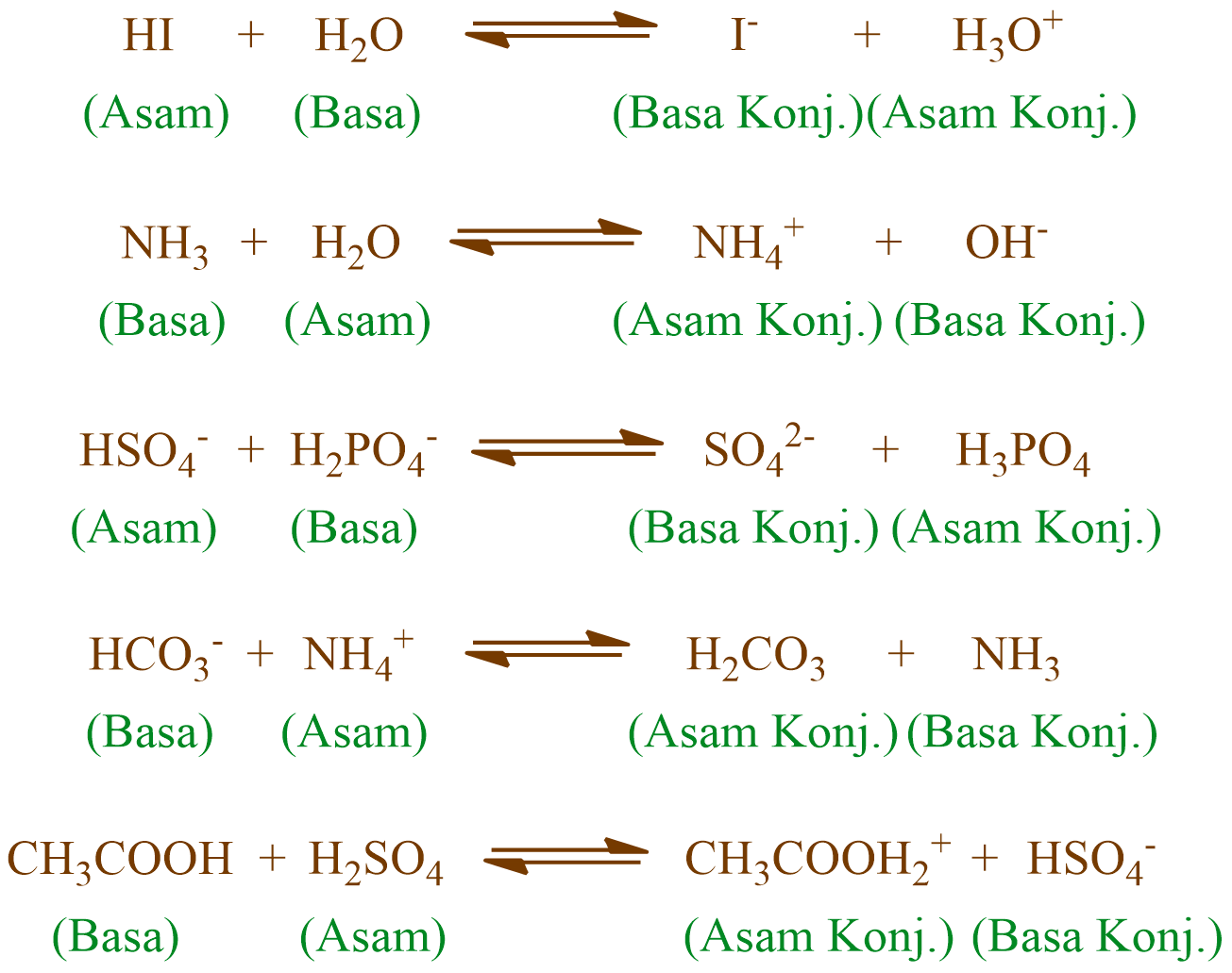
Selain itu dikenal juga istilah pasangan asam basa konjugasi pada teori Bronsted-Lowry dimana: 1. Spesi yang memiliki kemiripan, namun salah satu spesinya memiliki jumlah H (muatan proton) lebih banyak adalah asam Bronsted-Lowry dan pasangannya disebut basa konjugasi. 2.

Asam Basa Teori, Contoh, dan Sifat Asam Basa InformasainsEdu
Pasangan garam yang bersifat basa ditunjukkan oleh nomor 1 dan 4. Jawaban (B). Dilansir dari buku Bahas Total Matematika, Fisika, Biologi, Kimia, Ekonomi, Geografi, Sosiologi SMA IPA Kelas XI (2011) oleh Budhi Setyono, garam K2CO3 atau kalium karbonat terbentuk dari asam lemah H2CO3 dan basa kuat KOH, sehingga memiliki pH > 7 atau bersifat basa.
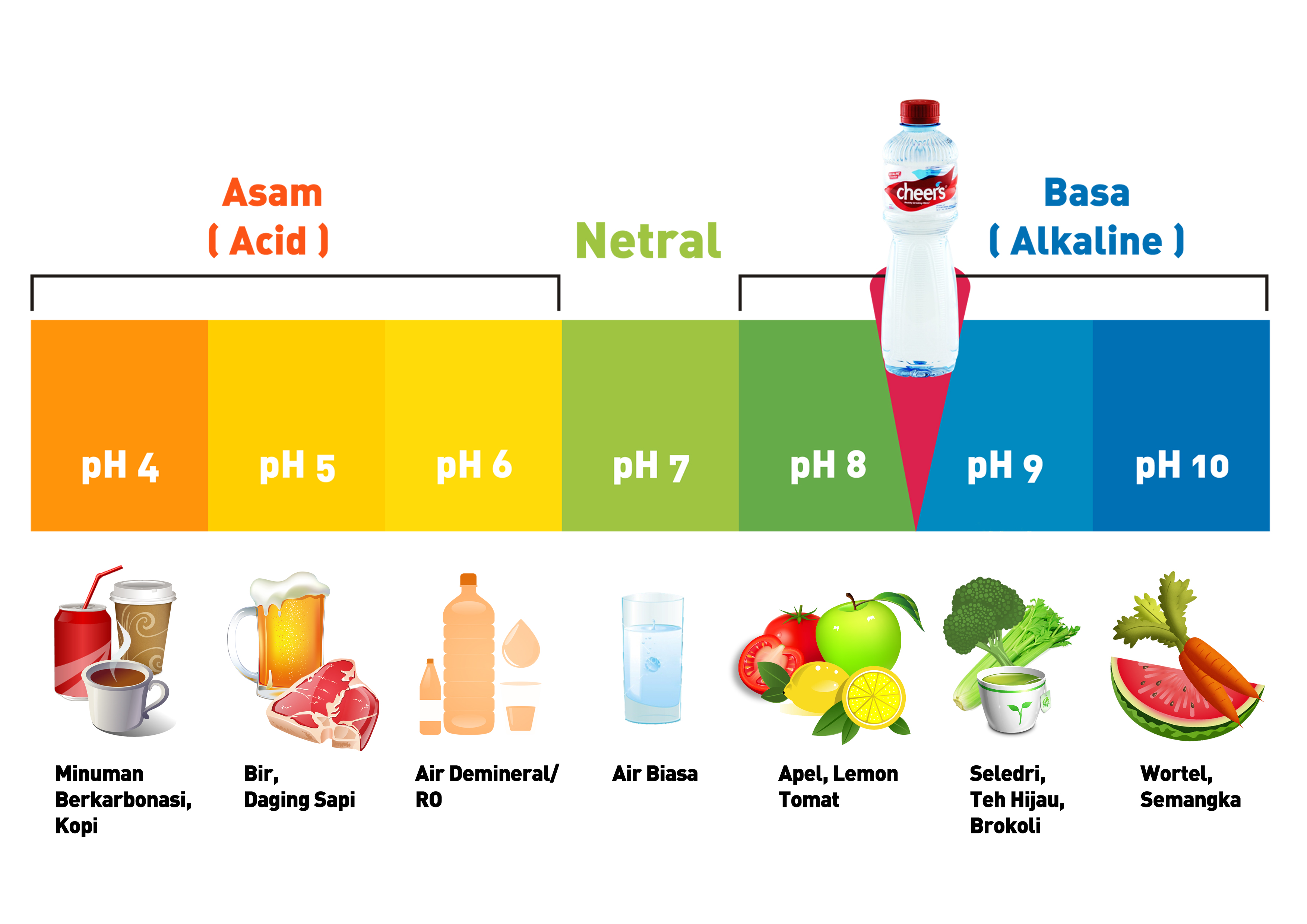
Indikator Asam Basa
Baca juga: Daftar Nama Asam-Basa Kuat dan Asam-Basa Lemah. Sifat kalsium karbonat. Garam kalsium dan ion karbonat membentuk kalsium karbonat yang tidak larut dalam air. Dilansir dari National Library of Medicine, kalsium karbonat dapat berupa bubuk putih yang tidak berbau atau kristal yang tidak berwarna dengan rasa berkapur atau hambar.

Contoh Asam Basa Menurut Bronsted Lowry Berbagai Contoh Riset
Umumnya, indikator asam basa akan berubah warna apabila dikenai senyawa asam atau basa. Ada banyak jenis indikator asam basa yang bisa dijumpai, mulai dari buatan dan alami. Berikut jenis-jenis indikator asam basa: Kertas lakmus merah dan kertas lakmus biru. Indikator asam basa alami, misalnya kol ungu, kulit manggis, bunga sepatu, dan lainnya.

Pengertian Asam dan Basa Serta Penggunaannya
Rumus Kimia Asam Karbonat. Rumus kimia asam karbonat yaitu H 2 CO 3 yang merupakan termasuk ke dalam golongan senyawa organik atau yang lebih dikenal sebagai asam karbonat organik. Asam karbonat organik juga merupakan senyawa yang telah menyusun gugus fungsi asam karbonat. Dimana saat CO 2 atau karbon dioksida larut kedalam air atau O 2 maka.

Pasangan basa konjugasi dari (HCO)_(3)^() adalah.a...
Natrium karbonat (juga dikenal sebagai soda cuci dan soda abu ), Na 2 CO 3, adalah garam natrium dari asam karbonat yang mudah larut dalam air. Natrium karbonat murni berwarna putih, bubuk tanpa warna yang menyerap embun dari udara, punya rasa alkalin/pahit, dan membentuk larutan alkali yang kuat.