
Cara mudah menentukan rumus molekul senyawa kimia SMA YouTube
Mengetahui massa molekul sangat diperlukan untuk mengubah gram menjadi mol. Kalikan jumlah atom dari masing-masing unsur yang terdapat di dalam senyawa dengan berat atom unsur tersebut. Jumlahkan total berat dari masing-masing unsur dalam senyawa. Misalnya, (NH 4) 2 S memiliki berat molekul (2 x 14,01) + (8 x 1,01) + (1 x 32,07) = 68,17 g/mol.

Cara Mencari Rumus Molekul Unsur dan Senyawa Kimia Kelas 10 Belajar Gratis di Rumah Kapan
Dengan kata lain, ada 1,67 sextillion molekul air dalam setetes air . Sekarang, jumlah atom dalam tetesan air adalah 3x jumlah molekul: atom dalam setetes air = 3 atom/molekul x 1,67 x 10 21 molekul. atom dalam setetes air = 5,01 x 10 21 atom. Atau, ada sekitar 5 sextillion atom dalam setetes air . Satu pertanyaan menarik adalah apakah jumlah.

Contoh Soal Menghitung Jumlah Atom Dikdasmen
1. Rumus Molekul Unsur Rumus molekul unsur adalah rumus yang menyatakan gabungan atom-atom yang sama jenis unsurnya lalu membentuk sebuah molekul. Nah, molekul unsur dibagi lagi menjadi dua berdasar dari jumlah atom yang bergabung. Ada molekul diatomik dan molekul poliatomik. a. Molekul Diatomik

Cara Menentukan Bentuk Molekul Bentuk Molekul Berdasarkan Jumlah Pasangan Elektron YouTube
Pembahasan Untuk mengetahui jumlah molekul suatu unsur, digunakan hubungan mol dengan bilangan avogadro dan jumlah partikel. langkah pertama, menghitung jumlah mol dengan konsep hubungan mol dengan massa zat: Langkah kedua, menghitung jumlah partikel dengan konsep hubungan mol dengan bilangan avogadro dan jumlah partikel:

Stoikiometri (Soal 45 Konsep Mol (Menghitung Jumlah molekul hasil reaksi)) YouTube
Perhitungan bisa meliputi jumlah mol, suhu, massa atom relatif, dan masih banyak variabel lainnya. Kali ini, Quipper Blog akan membahas salah satu variabel yang telah disebutkan sebelumnya, yaitu konsep mol. Penasaran dengan konsep mol? Ayo lanjutkan membacamu! Daftar Isi Sembunyikan Konsep Persamaan Reaksi Penyetaraan Persamaan Reaksi
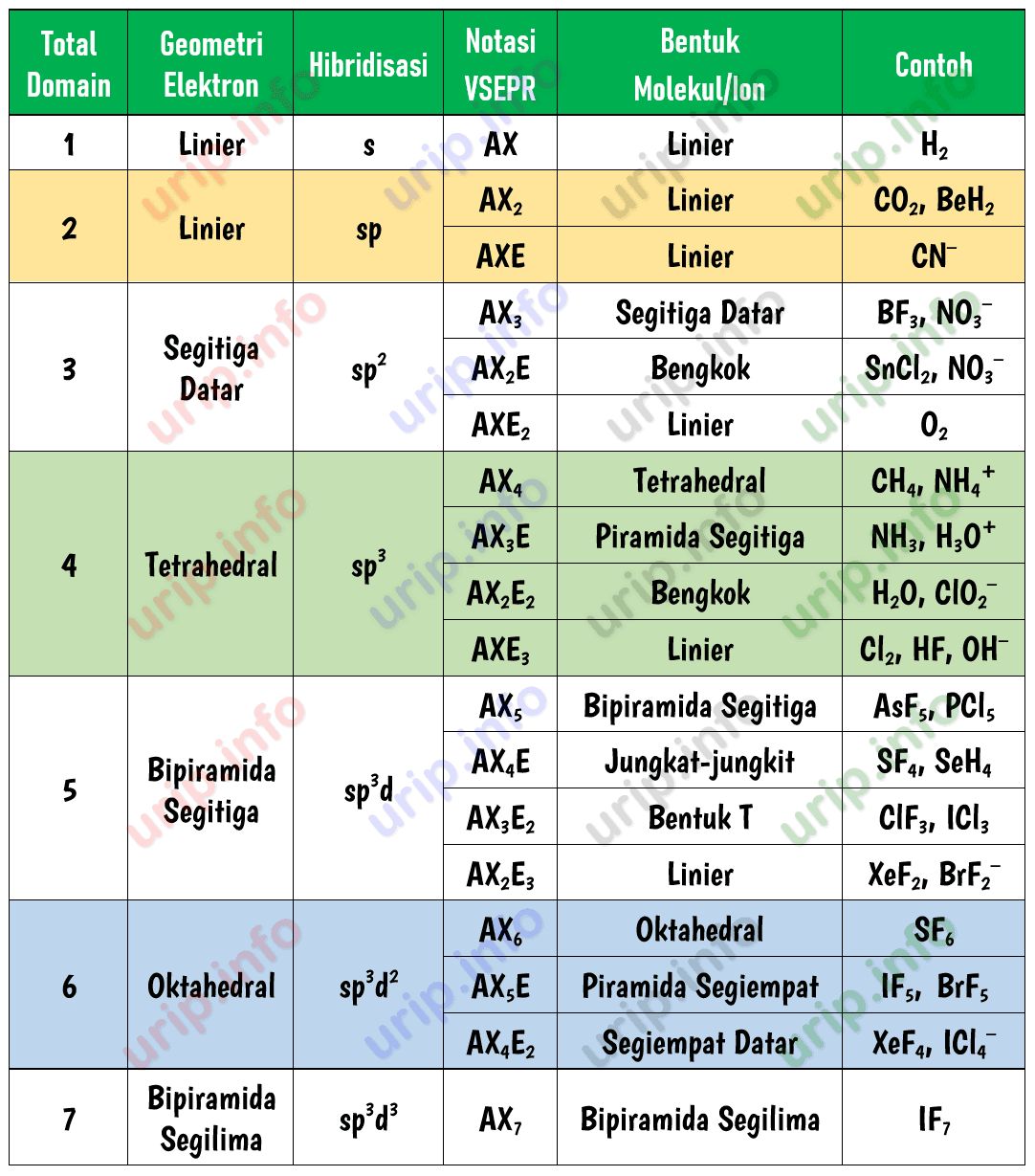
Cara Praktis Menghitung Jumlah Pasangan Elektron Bebas Atom Pusat dalam Molekul atau Ion
Jawab: a) Gas O2 adalah unsur diatomik dengan partikel berupa molekul unsur. b) Banyaknya mol O2 yang mengandung 1,505 × 1023 partikel dapat kita hitung dengan menggunakan rumus berikut. Jumlah partikel = mol × N. mol = Jumlah partikel/N. mol = 1,505 × 1023/6,02 × 1023. mol =1,505/6,02. mol = 0,25 mol.

Menghitung Jumlah mol jika diketahui Massa Molar Zat dan Massa Molekul Relatif YouTube
Rumus molekul merupakan rumus yang jumlah atomnya kelipatan dari rumus empiris. Namun demikian, ada beberapa senyawa yang memiliki rumus molekul dan empiris sama.. Jika nilai n sudah diketahui, Quipperian bisa mencari rumus molekulnya seperti cara berikut. Jadi, rumus molekul senyawa tersebut adalah C 5 H 10 O 5. Melengkapi Persamaan Reaksi.

Cara Menghitung Jumlah Atom Dalam Suatu Senyawa Hal Images
mol = Massa unsur dibagi Massa atom relatif (Ar) Tentukan perbandingan mol diantara unsur-unsur yang paling sederhana. Dengan begitu, bisa didapatkan rumus empiris Tentukan rumus molekul dengan cara mencari faktor pengali n. Adapun rumus yang digunakan ialah sebagai berikut (Rumus Empiris)n = Mr

cara menghitung jumlah atom dalam rumus kimia menghitung jumlah atom kimia kelas 10 SMA
Cara mencari rumus molekul unsur bisa dilakukan dengan mengidentifikasi simbol senyawa dan nomor atom. Dikutip dari Byjus, simbol senyawa dinyatakan sebagai huruf yang tertera di depan rumus. Sementara, angka di belakangnya diidentifikasi sebagai nomor jumlah atom yang membentuk molekul. Berikut contoh cara mencari rumus molekul unsur:

Jumlah molekul 30 gram senyawa dengan rumus empiris (CH2...
Menghitung mol dari gram dan sebaliknya bekerja dengan cara yang sama. Ini didasarkan pada massa setiap mol dari jenis atom atau molekul tertentu. Selanjutnya, kita akan melihat berbagai cara untuk menghitung mol dari massa suatu zat, serta menghitung massa suatu zat dari jumlah molnya. Salah satu dari ketiga cara melakukan perhitungan ini.

Cara Mencari Rumus Molekul Unsur dan Senyawa Kimia Kelas 10 Belajar Gratis di Rumah Kapan
Contoh soal: gram terlarut * (1/massa molar terlarut) = 3,4 g * (1 mol / 158 g) = 0,0215 mol. 5. Bagilah jumlah mol dengan banyaknya liter. Karena kamu sudah memiliki jumlah mol, kamu bisa membaginya dengan banyaknya liter larutan untuk mencari molaritas. Contoh soal: molaritas = mol terlarut / liter larutan = 0,0215 mol / 5,2 L = 0,004134615. 6.

Cara Mencari Rumus Molekul Unsur dan Senyawa Kimia Kelas 10 Belajar Gratis di Rumah Kapan
1. Hitung jumlah atom untuk setiap elemen yang ada dalam molekul. Pertama-tama, daftarkan setiap elemen yang ada dalam molekul. Anda bisa memakai simbol kimia atau menuliskan nama elemen tersebut. Kemudian, hitung atom sesuai formula molekuler dan tuliskan di sebelah nama atau simbol elemen.

Latihan soal UN jumlah molekul kimia SMA YouTube
Cara menghitung jumlah molekul. 2024. 1. Dapatkan Formula Kimia ; 2. Dapatkan Berat Atom dari Setiap Elemen ; 3. Hitung Berat Atom dari Senyawa ; 4. Hitung Jumlah Tahi Lalat. 6.022 x 10 ^ 23, untuk menghitung jumlah molekul dalam sampel Anda. Dalam contoh ini, jumlah molekul Na2SO4 adalah 0, 141 x 6, 022 x 10 ^ 23, atau 8, 491 x 10 ^ 22.

hitung jumlah atom dalam molekul (part 2) YouTube
Mr = n x (Ar C + 2 Ar H + Ar O) 60 = n x (12 + 2 + 16) 60 = n x 30 n = 2 dengan n = 2, rumus molekul senyawa tersebut adalah: 2 x (CH 2 O) = C 2 H 4 O 2 Jadi, rumus molekul senyawa adalah C2H4O2. Berdasarkan rumus molekul dan sifat-sifat senyawa diketahui bahwa senyawa tersebut adalah asam asetat.

Cara Menghitung Jumlah Atom Dalam Rumus Kimia Gini Caranya Hot My XXX Hot Girl
Volume (STP) = mol x 22,4L Namun, apabila tidak dalam kondisi standar hipotesis avogadro ini dapat dituliskan dalam bentuk persamaan: PV = nRT Dengan P : Tekanan (atm) V : Volume (L)
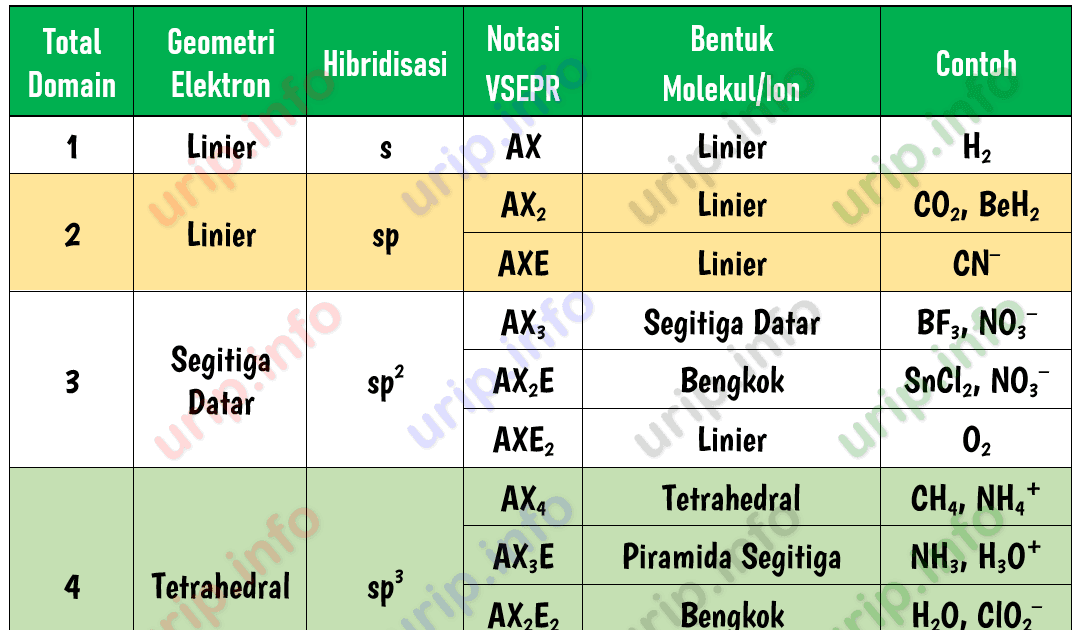
Cara Praktis Menghitung Jumlah Pasangan Elektron Bebas Atom Pusat dalam Molekul atau Ion
Cara Menghitung Berat Molekul Senyawa Kimia. Jagad Kimia Tuesday, November 27, 2018. Berat molekul ( BM ) atau molekul relative ( Mr ) adalah berat suatu molekul dalam satuan massa atom. Berat molekul dapat dihitung dengan cara menjumlahkan berat seluruh atom yang menyusunnya. Berat atom (BA) atau atom relative (Ar) adalah berat suatu atom.