
Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah
Kita ambil contoh reaksi asam HNO3 dan basa Ca(OH)2. 2HNO3 + Ca(OH)2 → Ca(NO)2 + 2H2O. Untuk menghasilkan reaksi di atas, maka dibuat penyetaraan antara reaktan dan produknya. Reaksi Oksida Asam dan Oksida Basa. Selain itu, ada juga nih yang namanya oksida asam dan oksida basa. Oksida asam umumnya unsur non logam yang berikatan dengan oksigen.

Cara Menghitung pH dan pOH Asam Kuat dan Basa Kuat YouTube
Perbedaannya, asam kuat adalah asam yang mudah terurai. Sedangkan asam lemah merupakan asam yang terion sebagian atau sulit terurai. Sekarang kita simak macam-macam contoh asam kuat dan asam lemah, yuk! Baca Juga: Sifat Zat dan Hubungannya dengan Partikel Penyusunnya: Sifat Fisika, IPA Kelas 9 SMP. Contoh Asam Kuat. 1. Asam klorida (HCl) 2.
Daftar Asam Basa Kuat Dan Lemah
Baca juga Cara Menentukan Derajat Keasaman dan Kebasaan (pH dan pOH) Zat. Memahami Kekuatan Asam dan Basa Zat. Pada dasarnya, cara mengetahui kekuatan asam dan basa bisa dilakukan dengan melihat ion yang ada dalam sebuah larutan. Sekedar informasi, ion adalah sekelompok atom atau atom yang bermuatan listrik.

Cara Mengitung pH Larutan Asam Kuat, Asam Lemah, Basa Kuat, Basa Lemah YouTube
Tabel Nilai Ka Umum untuk Asam Lemah. K a adalah tetapan kesetimbangan untuk reaksi disosiasi asam lemah . Asam lemah adalah asam yang hanya terdisosiasi sebagian dalam air atau larutan berair. Nilai K a digunakan untuk menghitung pH asam lemah . Nilai pKa digunakan untuk memilih buffer saat dibutuhkan. Memilih asam atau basa di mana pKa.

Detail Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah Koleksi Nomer 34
Di artikel Kimia kelas 11 ini, kita akan belajar mengenai macam-macam indikator asam basa dan cara menggunakannya. Yuk, baca sampai habis! Teman-teman, di artikel sebelumnya, kamu sudah mengenal apa itu zat asam-basa dan cara membedakannya, ya. Senyawa asam akan mengandung ion H +. Contohnya buah-buahan kaya vitamin C, cuka, minuman bersoda, dsb.

Cara Menghitung PH Larutan Asam Kuat Dan Asam Lemah Panduan Kimia + Riset
Cara Membedakan Asam dan Basa. Senyawa asam dapat dengan mudah ditemukan pada buah-buahan, seperti jeruk dan lemon. Selain itu, bisa juga ditemukan pada bahan makanan, seperti cuka. Bahkan, senyawa asam juga banyak digunakan sebagai bahan pengawet makanan lho, misalnya asam benzoat yang dimanfaatkan sebagai pengawet jus buah dan selai.

daftar nama asam basa kuat dan lemah.docx
Dengan cara ini diharapkan Anda bisa membedakan mana saja golongan zat asam yang termasuk asam kuat dan mana saja golongan asam yang termasuk asam lemah. Baca juga : Beo Jantan. Cara membedakan asam kuat dan asam lemah ini bisa dilakukan dengan 4 cara yang sangat mudah. Adapun keempat cara tersebut yaitu:

Menentukan pH Larutan Asam Kuat dan Asam Lemah KIMIA KELAS 11 YouTube
Asam kuat. Asam kuat terdisosiasi sempurna dalam air, membentuk H + dan anion. Ada enam asam kuat. Yang lain dianggap asam lemah. Anda harus memasukkan asam kuat ke memori: Jika asam 100 persen terdisosiasi dalam larutan 1,0 M atau kurang, itu disebut kuat.

MENGHITUNG / MENENTUKAN pH ASAM KUAT DAN ASAM LEMAH YouTube
Pada video ini, kita bahas tentang tips dan trik cara menghafal dan membedakan asam kuat, asam lemah, basa kuat, basa lemah dengan cepat, mudah, dan seru. Ti.
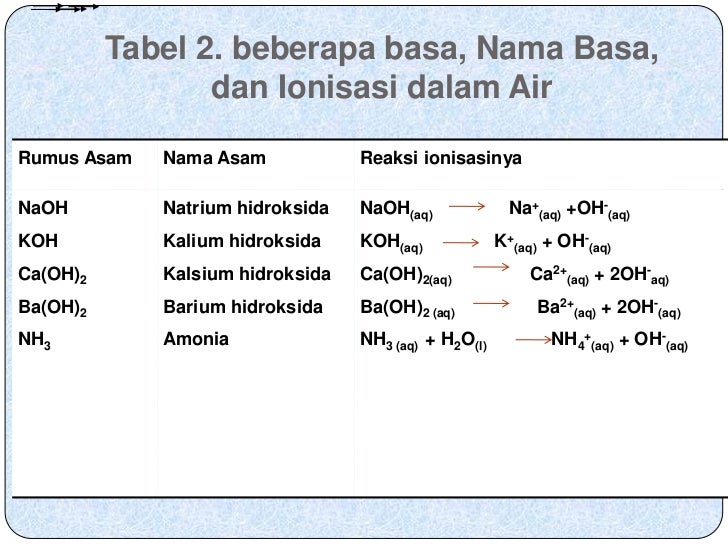
Contoh Asam Basa Kuat Dan Lemah Serta Reaksi Ionisasinya Berbagai Contoh
Asam basa diklasifikasikan menjadi dua bagian yaitu asam kuat & basa kuat dan asam lemah & basa lemah. Berikut penjelasannya berikut ini. 1. Asam kuat dan Basa kuat. Asam kuat merupakan asam yang jika dilarutkan dalam air mudah melepaskan ion H+, larutan tersebut akan mengalami disosiasi total dalam larutan. Contoh asam kuat yaitu HCl, HNO3, H.

Trik Super Kilat Membedakan Asam kuat / Asam lemah & Basa kuat / Basa lemah YouTube
Cara cepat membedakan senyawa yang termasuk asam kuat atau asam lemah dan senyawa yang termasuk basa kuat atau basa lemah.Cara atau trik dalam video ini dibu.

Cara mudah menentukan pH Asam yang paling lemah kimia SMA YouTube
Kalau pada suhu 25℃, pH < 7 bersifat asam, pH = 7 bersifat netral, dan pH > 7 bersifat basa. Derajat keasaman dan kebasaan suatu larutan. (dok. Flickr/boellstiftung) Semakin kecil nilainya, maka larutan tersebut akan semakin asam. Misalnya antara larutan dengan pH 3 dan 1, akan lebih kuat konsentrasi asam dengan pH 1 daripada 3.

PERHITUNGAN pH ASAM LEMAH DAN BASA LEMAH YouTube
1. Asam Kuat - Kekuatan Asam Kuat dan Asam Lemah. Asam kuat yaitu senyawa asam yang dalam larutannya terion seluruhnya menjadi ion-ionnya. Reaksi ionisasi asam kuat merupakan reaksi berkesudahan. Secara umum, ionisasi asam kuat dirumuskan sebagai berikut. HA(aq) → H+(aq) + A-(aq) Dengan: x = valensi asam. M = konsentrasi asam.

🔴pH ASAM KUAT & pH ASAM LEMAH ‼️🟢PEMBAHASAN SOAL pH ASAM KUAT & pH ASAM LEMAH YouTube
4. Titrasi Basa Lemah oleh Asam Kuat. Titrasi basa lemah oleh asam kuat, artinya: Titran (larutan standar pada buret) → asam kuat ; Titrat (larutan sampel pada labu erlenmeyer) → basa lemah; Titrasi basa lemah oleh asam kuat akan menghasilkan kurva sebagai berikut. Baca Juga: Bagaimana Cara Menentukan Indikator Asam Basa? Rumus Titrasi Asam.

pH Campuran asam Lemah dan Asam KuatKimia SMA YouTube
Klasifikasi Asam dan Basa. Di atas sudah disebutkan bahwa larutan asam dan basa dibagi menjadi dua jenis, yaitu kuat dan lemah. Kira-kira apa maksudnya? Mari kita bahas satu-satu, ya! Asam Kuat dan Basa Kuat. Asam kuat, singkatnya, merupakan senyawa asam yang dapat dengan mudah melepaskan ion H+ di dalam air dan dalam larutannya terjadi.

20+ Contoh Soal Hidrolisis Asam Lemah Dan Basa Kuat Contoh Soal Terbaru
Oleh karena itu, larutan garam dari asam lemah dan basa kuat akan meningkatkan konsentrasi OH − dalam air sehingga larutannya bersifat basa (pH > 7).. Garam dari asam lemah dan basa lemah. Garam seperti CH 3 COONH 4 yang dapat terbentuk dari reaksi asam lemah (CH 3 COOH) dan basa lemah (NH 3) akan mengalami hidrolisis kation dan anionnya. pH larutan garam demikian bergantung pada kekuatan.