
Larutan 0,1 molal berikut yang memiliki titik beku terend...
Berikut ini larutan yang diharapkan mempunyai titik didih. Agar 500 gram air tidak membeku pada suhu -5,4 C (Kf = 1,. Berapakah titik didih dan titik beku larutan 0,152 gram g. Sebanyak 27,75 g zat elektrolit dicampurkan ke dalam 800. Sebanyak lima zat nonelektrolit yang masing-masing massan. Jika zat nonelektrolit dengan massa yang.

Data percobaan penurunan titik beku Larutan Konsentrasi
Soal UN Sifat Koligatif Larutan Tahun 2013. Bagan berikut ini adalah gambaran molekuler larutan dengan berbagai konsentrasi. Gambar yang menunjukkan titik didih larutan paling besar adalah nomor.. A. I. B. II. C. III. D. IV. Pembahasan: Ingat kembali rumus kenaikan titik didih larutan! ∆Tb = Kb . m. jika diturunkan, maka rumusnya menjadi.

Contoh Soal Perbandingan Penurunan Titik Beku (Sifat Koligatif Larutan Elektrolit) YouTube
Di antara larutan berikut yang memiliki titik beku paling rendah adalah. Na 2 CO 3 0,3 m. CH 3 COOH 0,5 m. Mg(NO 3) 2 0,2 m. CuSO 4 0,2 m. glukosa 0,8 m. 10. Multiple Choice. Edit. 2 minutes. 1 pt. Di antara larutan berikut, yang memiliki titik beku paling tinggi adalah. Na 2 CO 3 0,3 M. Mg(NO. Di antara kelima macam larutan di bawah.

Larutan berikut yang memiliki titik beku paling tinggi ad...
Persamaan Penurunan Titik beku. Penurunan titik beku dapat dihitung menggunakan persamaan Clausius-Clapeyron dan hukum Raoult. Dalam larutan ideal encer titik beku adalah: Titik beku larutan total = Titik beku larutan - ΔTf. dimana ΔTf = molalitas * Kf * i. K f = konstanta titik beku air (1,86 ° C kg / mol ) i = Faktor Van't Hoff.

Diantara Larutan Berikut Yang Memiliki Titik Beku Paling Tinggi Adalah alat musik khas
Halo friends di sini ada soal pada soal ini kita punya 5 larutan di mana lima macam larutan ini ditanyakan mana yang punya titik beku terendah jadi semakin tinggi penurunan titik beku atau disini Delta TF maka akan semakin rendah pula titik beku larutan nya atau TF larutan karena Delta TF itu nilainya sama dengan TF pelarut dikurangi dengan urutannya Nah jadi kita cari dari kelima larutan ini.

Rumus titik beku larutan
Pertanyaan serupa. Disajukan beberapa larutan berikut. NaCl 0 , 1 m KOH 0 , 2 m C 6 H 12 O 6 0 , 1 m BaCl 2 0 , 5 m Urutan larutan dari yang mempunyai titik beku paling rendah yaitu.

Penurunan Titik Beku Larutan Adalah Reverasite
Haikal Friends pada kali ini kita diminta untuk menentukan larutan yang mempunyai titik beku paling rendah dan diketahui molalitas larutannya sama yaitu 0,1 molal Delta t f = m * a f dikalikan dengan larutan sama dengan pelarut dikurangi Delta TF TF larutan paling rendah. Jika paling besar di sini diketahui m dan KF nya sama karena digunakan.
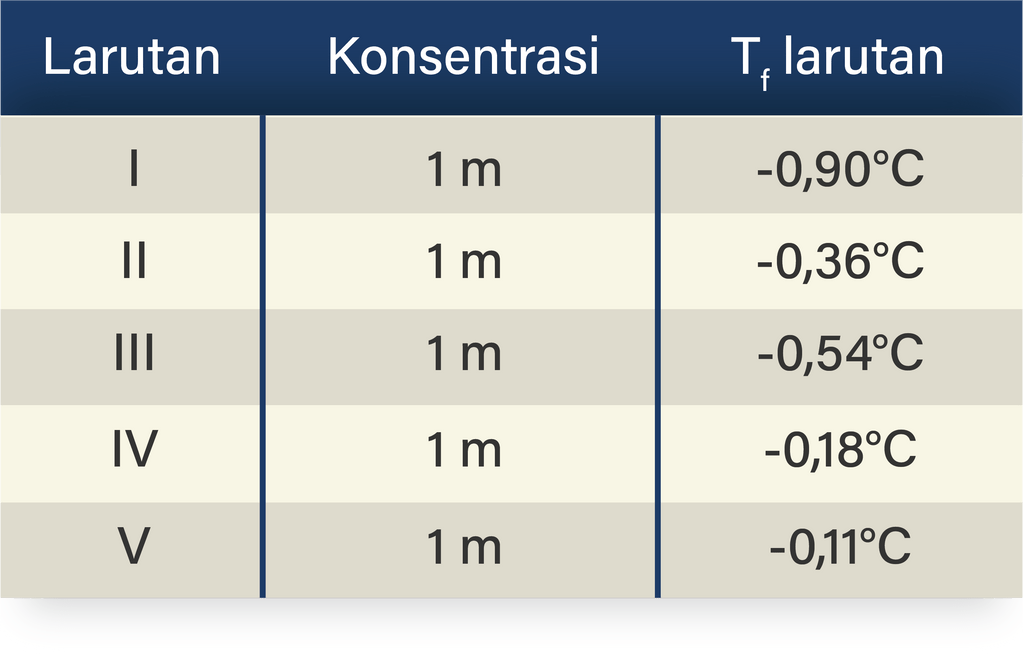
Berikut ini data titik beku beberapa larutan dalam...
Larutan yang memiliki titik beku paling rendah memiliki suhu yang lebih rendah dibandingkan dengan larutan lain yang memiliki efek penurunan titik beku yang kurang signifikan. Karena titik beku paling rendah lebih rendah, larutan semacam ini dapat digunakan dalam berbagai aplikasi industri, seperti pendinginan dan pengawetan.

Penurunan Titik Beku Larutan Definisi Dan Penyebabnya Reverasite
Dengan penambahan zat terlarut. Titik beku larutan akan lebih rendah dibandingkan titik beku pelarut. Hal ini dapat dijelaskan dengan diagram fasa. Jika titik beku pelarut (Tfo) dan titik beku larutan (TfL). Maka berlaku : Besar penurunan titik beku (∆Tf) adalah : Tfo air = 0oC.

Berikut data titik beku (Tf) beberapa larutan elektrolit
Di antara kelima larutan berikut ini yang mempunyai titik didih paling rendah adalah.A. C6H12O6 0,03 M B. Mg(NO3)2 0,02 M C. NaCl 0,02 M D. Al2(SO4)3 0,01 M E. KAl(SO4) 0,03 M. memiliki titik didih atau TB larutan yang paling rendah kita harus mencari larutan yang memiliki Delta TB yang paling kecil untuk rumus delta TB tadi ada Faktor.

Larutan berikut yang menyebabkan penurunan titik beku pal...
Sifat Koligatif Larutan; Penurunan Titik Beku; Larutan berikut yang mempunyai titik beku paling rendah adalah larutan A. asam sulfat 0,1 M D. sukrosa 0,1 M B. natrium asetat 0,1 M E. tembaga(I) sulfat 0,1 M C. barium nitrat 0,1 M. Penurunan Titik Beku; Sifat Koligatif Larutan; Kimia Fisik dan Analisis
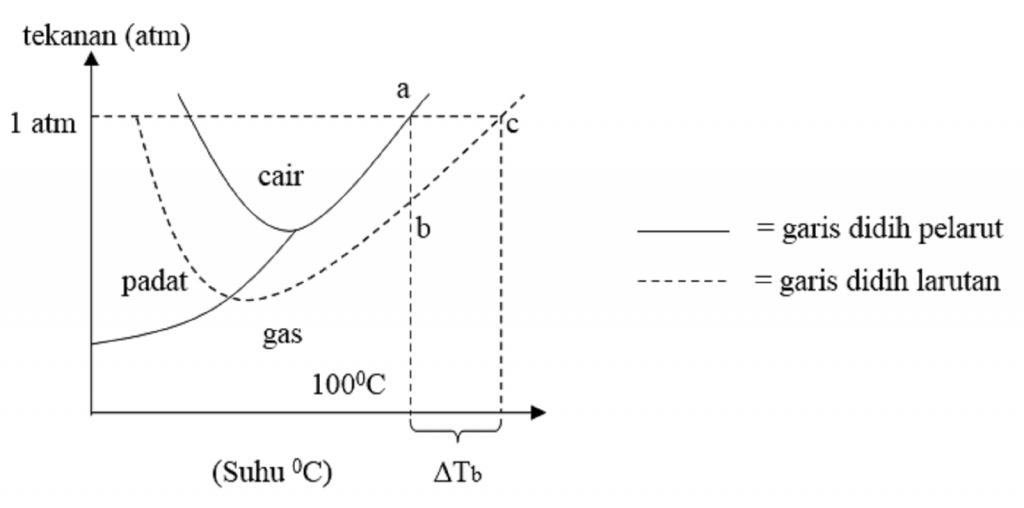
Membaca Grafik Titik Didih Dan Titik Beku Larutan Pelarut Sifat
Pada kosentrasi yang sama, larutan di bawah ini yang diprediksi mempunyai titik didih paling tinggi terdapat pada larutan.. A. C 6 H 12 O 6 . B. CO(NH 2) 2. C. Ba(OH) 2. D. NaCl. E. HCl. Soal nomor 8. Jika kenaikan titik didih 1 molal larutan urea 0,52ºC, pada konsentrasi yang sama kenaikan titik didih untuk larutan NaCl (α = 1) adalah.

Larutan berikut yang memiliki titik beku paling rendah ji...
Penurunan titik beku adalah selisih antara titik beku pelarut dengan titik beku larutan. Penurunan titik beku ini termasuk salah satu sifat koligatif larutan. Dalam perhitungan kimia, penurunan titik beku disimbolkan dengan ΔT f (f berasal dari kata freeze) atau ΔT b . Peristiwa penurunan titik beku ini sering diterapkan pada negara-negara.

Larutan yang memiliki titik beku paling rendah adalah.
Di sini ada soal mengenai titik beku ditanyakan adalah larutan yang memiliki titik beku paling rendah adalah kita harus tahu dulu untuk rumus dari penurunan titik beku atau Delta t f = k f dikali m dikali kemudian Delta TF sendiri mempunyai rumus PS pelarut dikurangi TF larutan = k f X M dikali nah pada rumus ini kita tahu bahwa TF ini berbanding terbalik dengan molalitas tapi karena di sini.

Di antara larutanlarutan berikut, larutan yang mempunyai...
17. Diantara larutan berikut ini pada konsentrasi yang sama, yang mempunyai titik didih paling tinggi adalah… A. Urea B. Natrium Klorida C. Asam Cuka D. Gula E. Kalsium Klorida 18. Kelarutan CaCl 2 dalam air pada suhu 0º C sekitar 5,4 molal. Jika K f = 1,86 ºC/m, maka penurunan titik beku larutan CaCl 2 0,54 molal adalah.. A. 1 º C B. 2 º.

Contoh Soal Titik Beku Larutan (Sifat Koligatif Larutan Elektrolit) YouTube
Jawaban terverifikasi. Diantara larutan berikut yang memiliki titik beku paling rendah adalah…. a. KAl (SO4)2 0,03 molal b. Al2 (SO4)3 0,01 molal c. NaCl 0,02 molal d. Mg (NO3)2 0,03 molal e.