
Kekhasan Atom Karbon Kimia YouTube
Elektron yang terletak pada petala terluar atom suatu unsur dipanggil elektron valens.. kumpulan karbon: 4 kumpulan nitrogen: 5 kumpulan oksigen: 6 halogen: 7 gas adi: 8** * Elektron valensi tidak berguna untuk logam peralihan. **Kecuali helium, kerana helium hanya mempunyai dua elektron valensi.
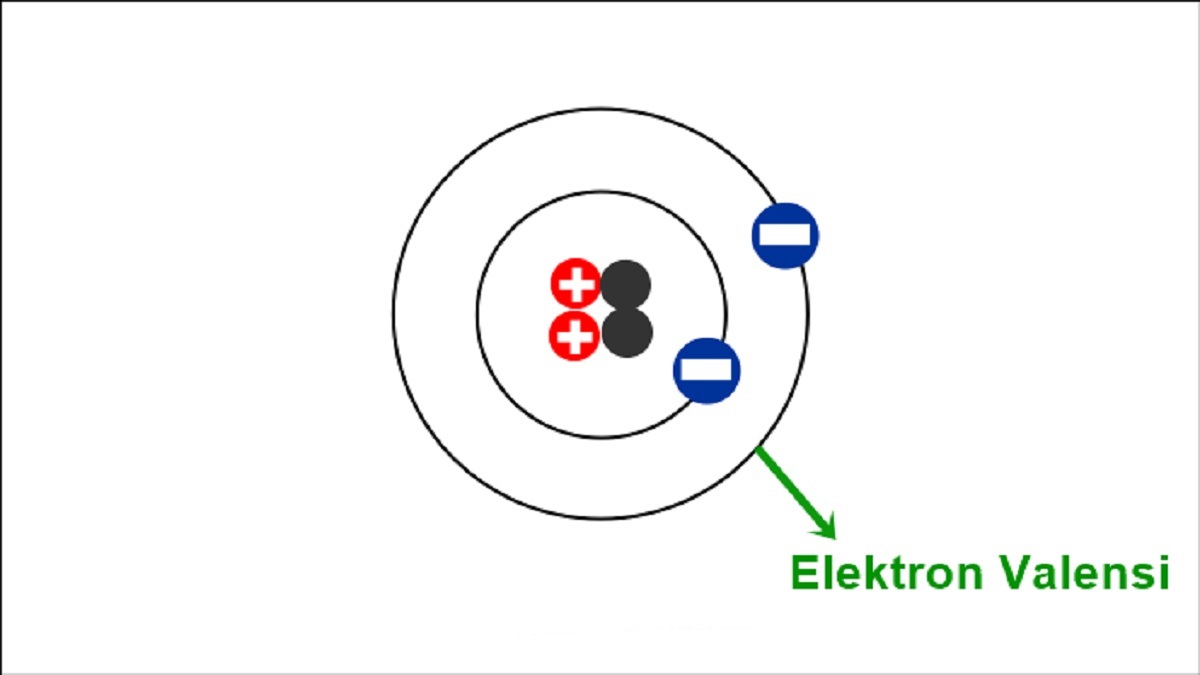
Pengertian Elektron Valensi, Karakteristik, Serta Penerapannya
Banyaknya jumlah elektron terluar (elektron valensi) dari suatu atom menentukan sifat-sifat kimia suatu unsur. Konfigurasi elektron dapat dituliskan dengan cara: 1. Berdasarkan Kulit. Berdasarkan kulit, dapat digunakan rumus konfigurasi elektron 2n2 2 n 2, di mana n menunjukkan kulit atom. Contoh: 11Na 11 N a: 2, 8, 1.

Konfigurasi Elektron Dan Elektron Valensi Special
3. Atom karbon dapat membentuk rantai karbon. Kehadiran 4 elektron valensi di atom karbon, nampaknya membawa sejuta manfaat bagi umat. Bagaimana tidak, dengan adanya 4 elektron valensi inilah atom karbon mampu membentuk ikatan kovalen dengan rantai karbon yang sangat panjang. Baik ikatan kovalen tunggal, rangkap 2, bahkan rangkap 3.

Konfigurasi Elektron Dalam Atom Kimia YouTube
Empat ikatan kovalen.Karbon memiliki empat elektron valensi sehingga valensinya adalah empat. Masing-masing atom hidrogen memiliki satu elektron valensi dan disebut univalen. Dalam ilmu kimia, elektron valensi atau elektron harkat adalah elektron pada kelopak terluar yang terhubung dengan suatu atom, dan dapat berpartisipasi dalam pembentukan ikatan kimia jika kelopak terluar belum penuh.

Susunan Elektron Bagi Atom SanaihasKelly
Elektron valensi. Elektron valensi adalah elektron yang berada pada kulit terluar. Pada konfigurasi elektron tersebut, elektron terakhir berada pada subkulit valensi 2s 2 2p 2. Maka, jumlah elektron valensinya adalah 2 + 2 = 4. Elektron valensi ini menjadi alasan dari kekhasan atom karbon, yaitu dapat membentuk rantai karbon dan dapat mengikat.
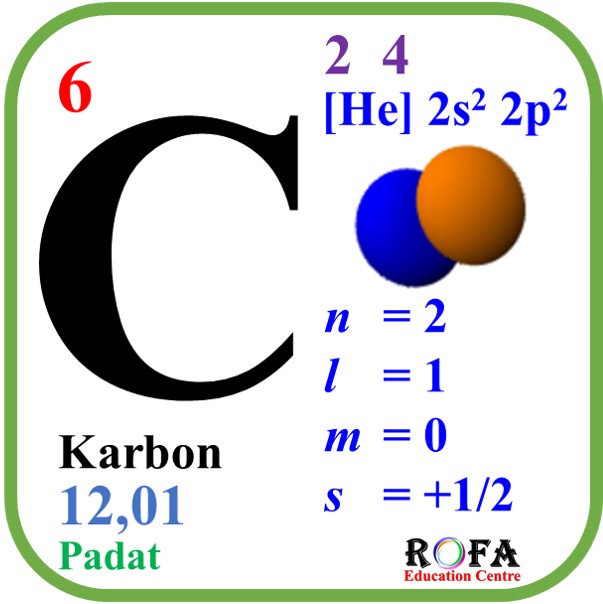
Keunikan Atom Karbon
Namun, atom dapat dipantau menggunakan mikroskop gaya atom. Ukuran atom sangat kecil, sedemikian kecilnya lebar satu helai rambut dapat menampung sekitar 1 juta atom karbon. Satu tetes air juga mengandung sekitar 2 × 10 21 atom oksigen. Intan satu karat dengan massa 2 × 10 -4 kg mengandung sekitar 10 22 atom karbon.
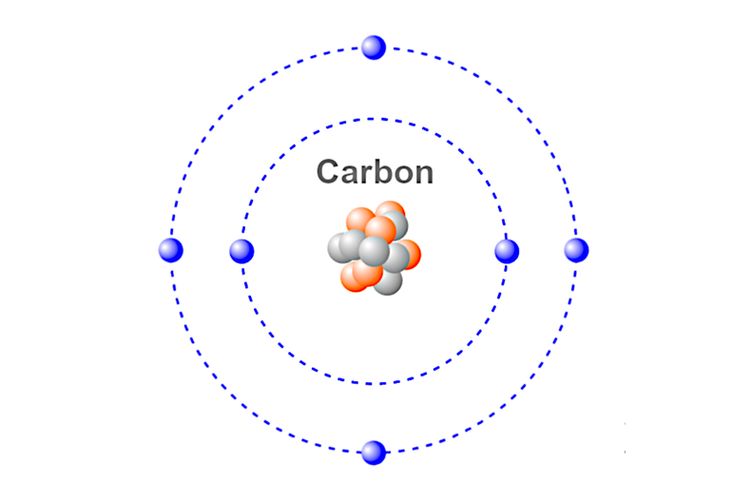
Foto Kekhasan Atom Karbon
Konfigurasi elektron atom 6 C: 2, 4. Jadi, atom C memiliki 4 elektron valensi, sedangkan atom H konfigurasinya hanya 1 saja, atau memiliki 1 elektron valensi. Ketika atom karbon (C) berikatan dengan atom hidrogen (H) makan setiap atom C mampu mengikat 4 atom H membentuk CH 4.
Kekhasan Atom Karbon Chemistry Quizizz
Elektron Valensi. Elektron valensi adalah elektron dalam atom yang berperan dalam pembentukan ikatan kimia. Pada unsur-unsur golongan utama (IA, IIA, IIIA, hingga VIIIA), elektron valensi adalah elektron yang berada pada kulit elektron terluar. Oleh karena itu, kulit elektron terluar sering disebut sebagai kulit valensi.

Penjelasan Struktur Atom Proton, Neutron, Elektron dengan Contoh Soal
Keempat elektron valensi atom karbon dapat membentuk rantai tersendiri. Sehingga akan dihasilkan banyak sekali kemungkinan terbentuknya senyawa-senyawa yang berbeda. Kemungkinan ini didasarkan pada jenis ikatan, jumlah ikatan, serta posisi atom karbon tersebut di dalam rantai karbon. 3. Karbon juga dapat membentuk rantai lurus, bercabang.
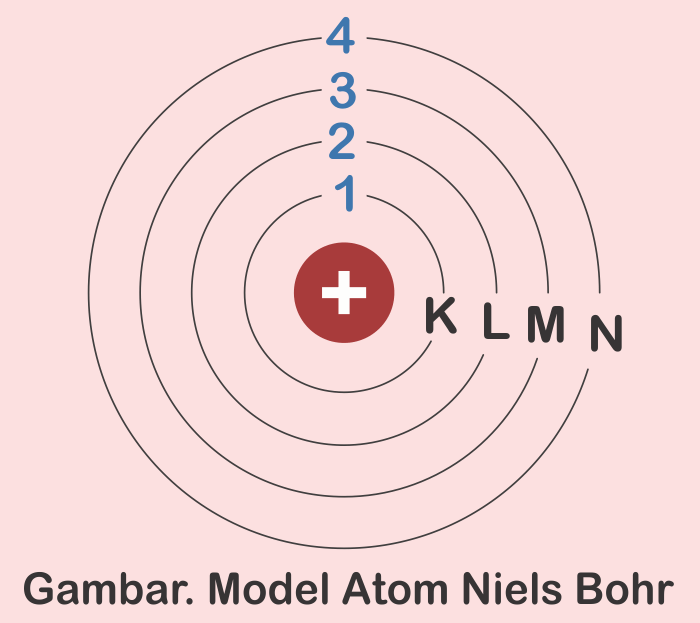
Cara Menentukan Elektron Valensi Siswapedia
Elektron yang terletak di petala terluar dinamakan lektron valens. Bilangan elektron menentukan sifat kimia satu unsur. Unsur yang mempunyai bilangan elektron valens yang sama menunjukkan sifat kemia yang sama. Contoh: Berapakah bilangan elektron valens bagi natrium, 11 Na; oksigen, 8 O; Karbon, 12 C dan Kalsium, 20 Ca. Jawapan:

Konfigurasi Elektron Dan Nomor Atom Unsur Yang Benar Untuk Unsur Unsur My XXX Hot Girl
Sebelum lanjut, kalau elo ingin review materi tentang penomoran sebuah atom hingga penulisan konfigurasi elektron, elo bisa cek artikel Zenius yang berjudul Struktur Atom - Materi Kimia Kelas 10 ini, ya.. Oke. Jumlah empat elektron valensi ini spesial karena artinya atom karbon mempunyai kekhasan dapat membentuk empat ikatan kovalen untuk mencapai keadaan stabil yang menyerupai gas mulia.
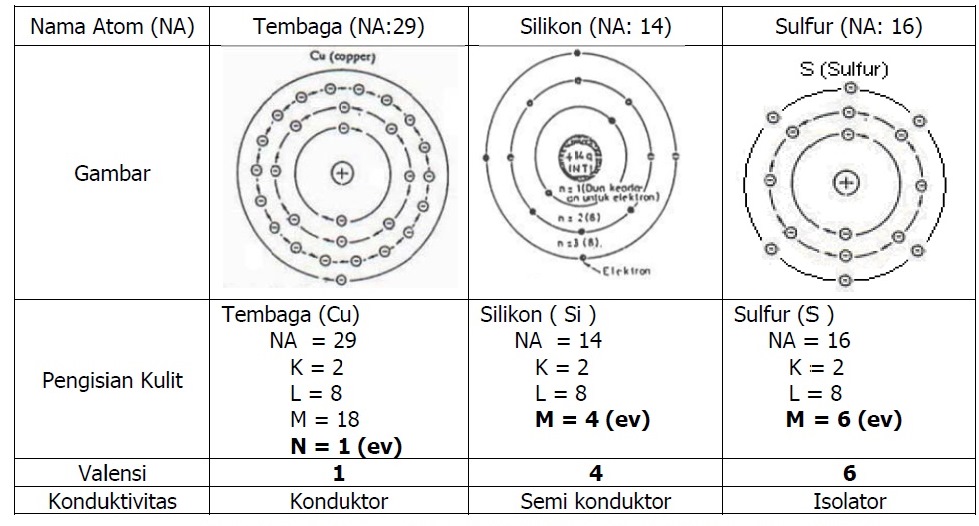
Teori Elektron Mekanik Alat Berat
Mengetahui cara mencari jumlah elektron valensi dalam atom tertentu adalah keterampilan penting untuk ahli kimia karena informasi ini menentukan jenis ikatan kimia yang dapat dibentuknya. Untungnya, yang Anda butuhkan untuk mencari elektron valensi hanyalah tabel periodik unsur biasa. Bagian 1.
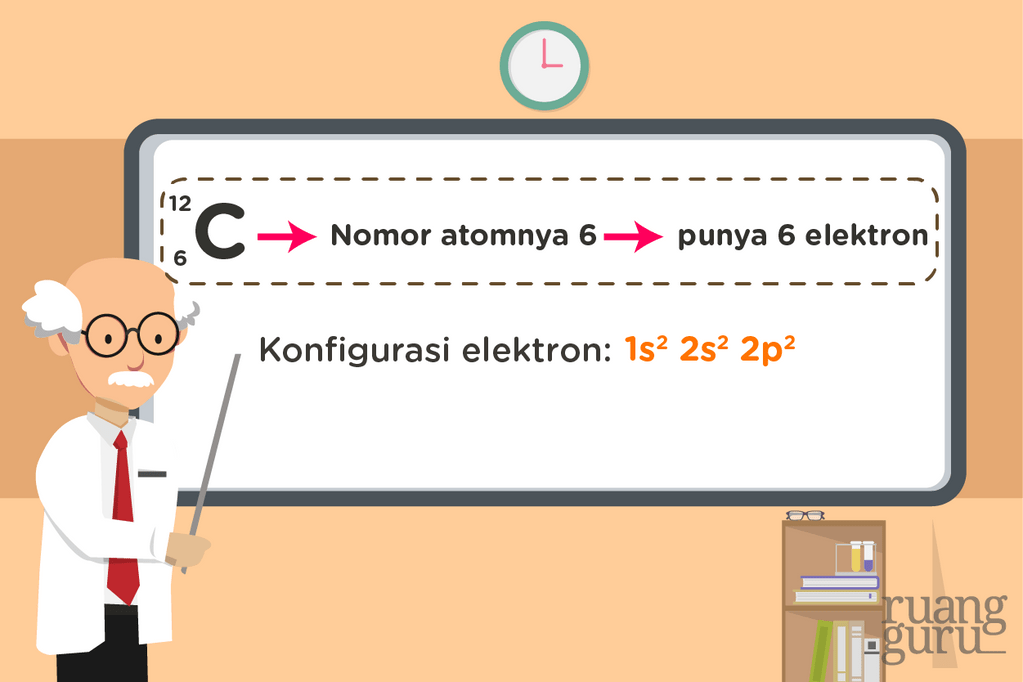
Memahami Konfigurasi Elektron dan Diagram Orbital Lebih Mudah Kimia Kelas 10
Atom karbon dapat membentuk ikatan kovalen tunggal, rangkap, membentuk rantai karbon yang panjang lurus, bercabang maupun melingkar. Kekhasan Atom Karbon. Atom karbon mempunyai empat elektron valensi; Atom karbon (C ) memiliki karakteristik yang khas dengan nomor atom 6 konfigurasi elektron, yakni kemampuan dalam membentuk rantai C yang panjang.
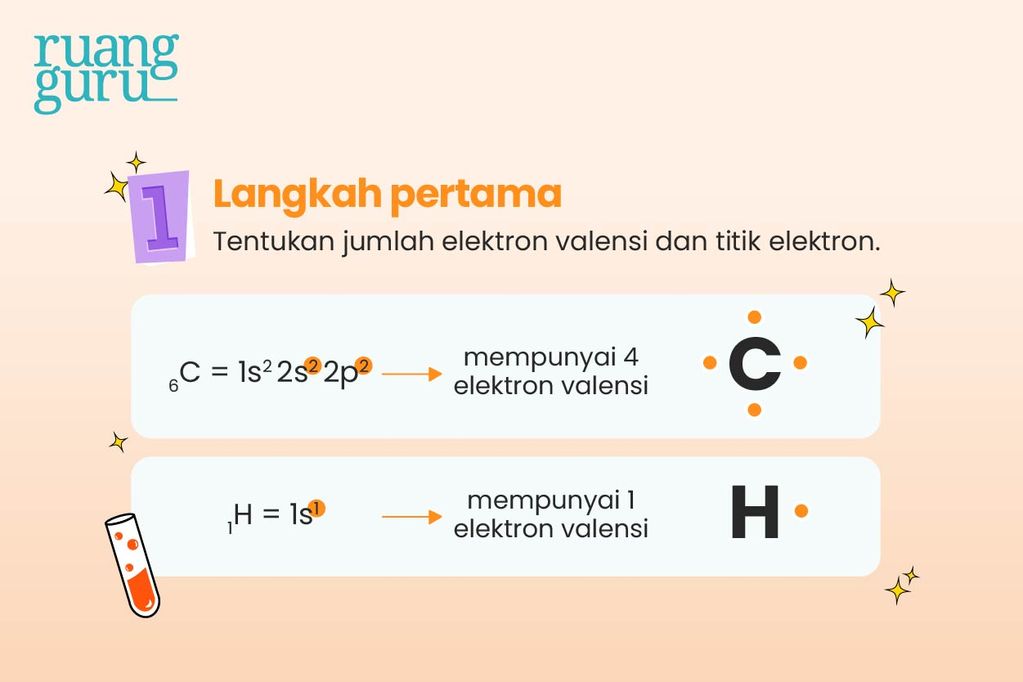
Konsep Struktur Lewis dalam Ikatan Kovalen & Cara Menggambarnya Kimia Kelas 10
Karbon memiliki valensi 4 karena 4 elektron dapat diterima untuk mengisi orbital 2p . Valensi Umum. Atom unsur dalam kelompok utama tabel periodik dapat menampilkan valensi antara 1 dan 7 (karena 8 adalah oktet lengkap).. Bilangan oksidasi merupakan indikator yang lebih baik untuk keadaan elektron suatu atom karena memiliki besaran dan tanda.

Gambar berikut menunjukkan susunan elektron pada senyawa
Kekhasan atom karbon. 1. Atom karbon mempunyai nomor atom 6, dengan empat elektron valensi. Keempat elektron valensi membentuk pasangan elektron bersama dengan atom lain membentuk ikatan kovalen. Keempat elektron valensi ini dapat digambarkan sebagai tangan ikatan. 2.

Konfigurasi Elektron dalam Tabel Periodik (Kimia SBMPTN, UN, SMA) YouTube
Elektron valensi karbon merupakan bagian integral dari kimia organik modern, dengan kemampuan karbon untuk membentuk ikatan kovalen dengan elemen lain. Artikel ini akan membahas mendalam tentang pentingnya elektron valensi dalam kimia organik serta pengaruhnya pada interaksi molekul di dalam sistem biologis.